微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在一定温度下,固定容积的容器中加入a mol A和b mol B,发生
反应:A(g)+2B(g) 2C(g)一段时间后达到平衡,生成n mol C。则下列说法中不正确的是(?)
2C(g)一段时间后达到平衡,生成n mol C。则下列说法中不正确的是(?)
A.再充入少量A,平衡向正反应方向移动,但K值不变
B.起始时刻和达到平衡后容器中的压强之比为(a+b)∶(a+b-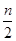 )
)
C.当2v正(A)=v逆(B)时,反应一定达到平衡状态
D.充入惰性气体(如Ar)增大压强,平衡向正反应方向移动
参考答案:D
本题解析: D、充入惰性气体(如Ar)增大压强,反应中各组分的浓度并没有发生变化,平衡不移动,错误。
本题难度:一般
2、选择题 在一定温度下,向容积不变的密闭容器中充入a mol NO2,发生如下反应:2NO2(g)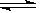
N2O4(g);ΔH < 0。达平衡后再向容器中充入a mol NO2,再次达到平衡后,与原平衡比较,下
列叙述不正确的是(?)。
A.NO2的体积分数减小
B.NO2的转化率提高
C.NO2的质量分数增大
D.反应放出的总热量大于原来的2倍
参考答案:C
本题解析:略
本题难度:简单
3、填空题 一氧化碳是一种重要的化工原料.
(1)高炉炼铁中发生的反应之一是:FeO(s)+CO(g)
Fe(s)+CO2(g),△H=-1kJ/mol.温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比将______(填“增大”、“减小”或“不变”).
已知1100℃时,该反应平衡常数K=0.263,现测得高炉中(CO2)=0.025mol/L,c(CO)=0.1mol/L,此时该反应______.
A.向正反应向向进行?B.处于平衡状态?C.向逆反应方向进行
(2)合成氨工业中需将原料气中的CO变成CO2除去.在密闭密器中将CO和H2O混合加热到800℃,达到下列平衡:
CO(g)+H2O(g)?CO2(g)+H2(g)?K=1.0,若平衡时n(H2O)/n(CO)=1,则CO转化为CO2的转化率为______.
(3)用CO和H2经如下两步反应制得甲酸甲醛:CO+2H2→CH3OH,CO+CH3OH→HCOOCH3已知反应①中CO的转化率为80%,反应②中两种反应物的转化率均为85%,则2.52tCO最多可制得甲酸甲醛多少吨?(写出计算过程).
参考答案:(1)反应放热,升高温度平衡向逆反应方向移动,则平衡常数应减小,(CO2)=0.025mol/L,c(CO)=0.1mol/L,
Q=0.0250.1=0.25<0.263,反应向正反应方向进行,
故答案为:减小;A;
(2)若平衡时n(H2O)/n(CO)=1,根据反应方程式可知,起始时H2O和CO物质的量相等,设H2O和CO的物质的量都为1mol
平衡时转化xmolCO,
? ?CO(g)+H2O(g)?△?.??CO2(g)+H2(g)
起始(mol):1? 1? 0? 0
转化(mol):x? x?x? x
平衡(mol):1-x? 1-x? x? x
则x2(1-x)2=1,
x=0.5,
则CO转化为CO2的转化率为0.51×100%=50%,
故答案为:50%;
(3)n(CO)=2.52×106g28g/mol=9×104mol,
设用于制备甲醇的CO物质的量为x,用于和甲醇反应的CO为y,
则
本题解析:
本题难度:一般
4、简答题 在一定条件下,将N2和H2的混合气体100ml通入密闭容器中,达平衡时,容器内的压强比反应前减少1/5,又测得此时混合气体的平均分子量为9.试求
(1)原混合气体中N2和H2各多少毫升?
(2)H2的转化率为多少?
参考答案:(1)设原混合气体中N2的体积为x,H2的体积为y,反应中转化的N2的体积为a,则x+y=100mL ①,
N2+3H2 ?2NH3 △V
1 3 2 2
a 3a 2a
反应后气体的体积减小了2a,根据容器内的压强比反应前减少1/5,则达到平衡状态时气体的物质的量比反应前减少了15,2ax+y=15②,将①带人②解得,a=10mL,
根据三段式:N2 +3H2?2NH3
反应前:x y0
体积变化10mL30mL 20mL
平衡:x-10 y-30mL 20mL
相同条件下,气体摩尔体积相同,设为Vm,根据质量守恒定律及反应后气体的体积可得,混合气体的平均分子量为:28×xVm+2×yVmx+y-20Vm=9 ③,
由③化简有19x-7y+180=0 ④
由①④联立,解得x=20mL,y=80mL,
答:原混和气体中有N220mL,H280mL;
(2)反应消耗10mL氮气,同时消耗了30mL氢气,所以氢气的转化率为:30mL80mL×100%=37.5%,
答:H2的转化率为37.5%.
本题解析:
本题难度:一般
5、选择题 对于可逆反应:2A(g)+B(g)  ?2C(g) △H <0,下列各图中正确的是
?2C(g) △H <0,下列各图中正确的是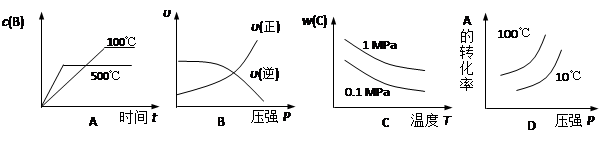
参考答案:C
本题解析:考查可逆反应中的图像识别。根据反应的方程式可知,正反应是体积减小的、放热的可逆反应,所以升高温度,平衡向逆反应方向进行,B的浓度应该是增大的,A的转化率应该是降低的,选项A和D都不正确;增大压强,平衡向正反应方向进行,正逆反应速率均是增大的,C的体积分数是增大的,所以选项B不正确,C正确,答案选C。
本题难度:一般