微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关反应限度的叙述正确的是( )
A.使用催化剂,可降低反应的活化能,加快反应速率,改变反应限度
B.依据焓判据:NH4HCO3受热分解可自发进行
C.大多数化学反应在一定条件下都有一定的限度
D.FeCl3与KSCN反应达到平衡时,向其中滴加KCl溶液,则溶液颜色变深
2、填空题 (8分)2009年“ 六・五”世界环境日,中国主题是“减少污染――行动起来”,这向世界传达了建设环境友好型社会的理念。已知反应:
六・五”世界环境日,中国主题是“减少污染――行动起来”,这向世界传达了建设环境友好型社会的理念。已知反应:
①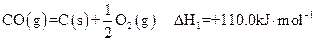
②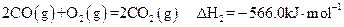
请回答下列问题:
(1)反应①的熵变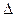 S (填“>”或“<”)0。
S (填“>”或“<”)0。
(2)有人建议,汽车尾气中的CO可用催化加热分解的方法来消除(反应①),这一方案在理论上是否可行? (填“可行”或“不可行”)。
(3)反应②中的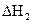 是不是CO的燃烧热? (填“是”或“
是不是CO的燃烧热? (填“是”或“ 不是”)。
不是”)。
(4)煤炭的充分燃烧也是建设环境友好型社会的一个重要方面,12 g C(s)完全燃烧生成CO2(g)时,放出的热量为 kJ(依 据反应①、②计算)。
据反应①、②计算)。
3、选择题 试验证明,多数能自发进行的反应是放热反应。下列叙述中正确的是
[? ]
A.所有的放热反应都是自发进行的
B.所有的自发反应都是放热的
C.焓变是影响反应是否具有自发性的一种重要因素
D.焓变是决定反应是否具有自发性的判据
4、选择题 下列叙述不正确的是
A.16gCH4与18gNH+4所含的原子数相等
B.16O原子和18O原子属于同一种元素的不同核素
C.非自发反应在任何条件下都不能发生
D.熵增加且放热的反应一定是自发反应
5、选择题 将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),使其达到分解平衡:NH2COONH4(s)  2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
温度/℃
| 15.0
| 20.0
| 25.0
| 30.0
| 35.0
|
平衡总压强/kPa
| 5.7
| 8.3
| 12.0
| 17.1
| 24.0
|
平衡气体总浓度/10-3mol/L
| 2.4
| 3.4
| 4.8
| 6.8
| 9.4
|
下列有关叙述正确的是
A.该可逆反应达到平衡的标志之一是混合气体平均相对分子质量不变
B.因该反应熵变(△S)大于0,焓变(△H)大于0,所以在低温下自发进行
C.根据表中数据,计算15.0℃时的分解平衡常数约为2.0×10-9(mol・L-1)3
D.达到平衡后,若在恒温下压缩容器体积,氨基甲酸铵固体的质量减小