��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����˵����ȷ���ǣ�������
A������ѹǿ������������ӣ���ѧ��Ӧ����һ������
B�������¶ȣ�����Ӱٷ������ӣ���ѧ��Ӧ����һ������
C������Ӽ��������ķ��Ӽ����ײΪ��Ч��ײ
D�����뷴Ӧ�ʹ����Ӱٷ������ӣ���ѧ��Ӧ��������
�ο��𰸣�A������ѹǿ��ʹŨ���������Ũ�����ӣ���ѧ��Ӧ����������A����
B�������¶ȣ�����Ӱٷ������ӣ���ѧ��Ӧ����һ���ܹ�����B��ȷ��
C������Ӽ��������ķ��Ӽ����ײ��ֻ���ܷ�����Ӧ����ײ������Ч��ײ����C����
D�����뷴Ӧ�����Ӱٷ������䣬��������������ӣ���ѧ��Ӧ��������D����
��ѡB��
���������
�����Ѷȣ���
2������� ijʵ��С������ȡ����ͭ��֤������ͭ�ܼӿ�����صķֽ⣬����������ʵ�飺
��һ����ȡ����ͭ
�ٳ�ȡ2gCuSO4?5H2O��ϸ�����ձ�����10mL����ˮ�ܽ⣻
��������CuSO4��Һ����μ���NaOH��Һ��ֱ�����ٲ���������Ȼ�����û����ת�Ƶ���������������ȫ����Ϊ��ɫ��
�۽���������û������ˡ�ϴ�ӣ����ɺ���ϸ���ã�
�ش��������⣺
��1������ʵ�鲽������Ҫʹ�ò���������______����ʵ����ţ�
������֤������ͭ�ܼӿ�����صķֽⲢ��������̵Ĵ�Ч�����бȽ�
����ͼװ�ý���ʵ�飬ʵ��ʱ��������25mL����Ϊ����������Ӱ��ʵ������ؾ��Ѻ��ԣ�����������£�
| ʵ����� | KClO3���� | ������������ | ��������
��
1.2g
����������
��
1.2g
CuO?0.5g
��
1.2g
MnO2?0.5g
|
�ش��������⣺
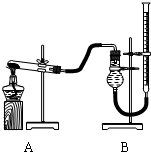
��2������ʵ���еġ��������ݡ�ָ______��
��3����Ҫ֤��ʵ����и�������ռ���������O2���ɴ������ռ��������õ��ɼм�סB���齺�ܣ���ȥ������ϵ�����Ƥ����______��
��4��Ϊ̽��CuO��ʵ������Ƿ�������ã��貹������ʵ�飨����д�������������
a��______��b��CuO�Ļ�ѧ������û�иı䣮
�ο��𰸣���1�����ܽ�������ò��������裬�ӿ��ܽ��ٶȣ������ò�����ת�ƹ��壻�����ò���������Һ�壮
�ʴ�Ϊ���٢ڢ�
��2��֤������ͭ�ܼӿ�����صķֽ⣬����������̵Ĵ�Ч�����бȽϣ��Ա�ʵ��һ��Ҫ���Ʊ�������ʵ����Ӧ�����������������������������ͭ��������̵�������ȣ��ɱ���������ɵ������25mL�����������õ�ʱ�䣮
�ʴ�Ϊ������25mL���������ʱ��
��3��������������ȼ�ص㣬���������ķ���Ϊ��ȡһ�������ǵ�ľ�������������ڣ��ɿ����ɼУ���ľ���Ƿ�ȼ��
�ʴ�Ϊ��ȡһ�������ǵ�ľ�������������ڣ��ɿ����ɼУ���ľ���Ƿ�ȼ��
��4���������ܸı仯ѧ��Ӧ�ٶȣ������������ͻ�ѧ���ʲ��䣬�ʻ�Ӧ��������ͭ�������Ƿ�ı䣮
�ʴ�Ϊ��CuO��������û�иı�
���������
�����Ѷȣ�һ��
3��ѡ���� ��Ӧ2A(g)? ?2B(g)��C(g)?�SH> 0���ﵽƽ��ʱ��Ҫʹ�淴Ӧ���ʽ��ͣ�A��Ũ������Ӧ��ȡ�Ĵ�ʩ��
?2B(g)��C(g)?�SH> 0���ﵽƽ��ʱ��Ҫʹ�淴Ӧ���ʽ��ͣ�A��Ũ������Ӧ��ȡ�Ĵ�ʩ��
A����ѹ
B������
C����ѹ
D������B��Ũ��
�ο��𰸣�B
�����������Ӧ���������ġ����ȵĿ��淴Ӧ�����Լ�ѹƽ��������Ӧ�����ƶ���A����ȷ�������¶ȣ���ƽ�����淴Ӧ�����ƶ���A��Ũ������B��ȷ��CD�������淴Ӧ���ʣ�����ȷ����ѡB��
�����Ѷȣ�һ��
4��ѡ���� ����ͼ��ʾ��ƽ��������X������������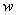 ���ڲ�ͬ��ѹǿ�£����¶ȣ�T���仯����������������ĸ�ƽ����ϵ�У�X���Դ����ú��߱��������ʣ���Ӧ�и����ʾ�Ϊ���壩��?����
���ڲ�ͬ��ѹǿ�£����¶ȣ�T���仯����������������ĸ�ƽ����ϵ�У�X���Դ����ú��߱��������ʣ���Ӧ�и����ʾ�Ϊ���壩��?����
A��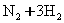

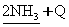
B��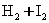

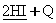
C��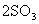


D��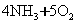

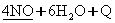
�ο��𰸣�D
�����������ѧƽ���е�ͼ����Ҫ����ѧ���Ի�ѧƽ���ƶ�ԭ�������⡣ͼ�����¶ȵ����ߣ�X�������������٣�˵��ƽ�����淴Ӧ�����ƶ����淴Ӧ�����ȷ�Ӧ������ӦΪ���ȷ�Ӧ�������¶Ȳ��䣬����ѹǿ��X������������С��ƽ�����淴Ӧ�����ƶ����淴Ӧ�Ƿ�������С�ķ�Ӧ���ۺ��ٻ�õó��𰸡�
�����Ѷȣ���
5��ѡ���� ���д�ʩ��Ϊ�˽��ͻ�ѧ��Ӧ���ʵ��ǣ�������
A��ʳƷ���ڱ���������
B����ҵ�����ô����������
C���ϳɰ���ҵ��ʹ�ô���
D���ڼ��������£���������ԭ����ͭ
�ο��𰸣�A��ʳƷ���ڱ��������أ��¶ȵͣ���Ӧ���ʽ��ͣ���Aѡ��
B����ҵ�����ô��������������Ӧ��Ũ������Ӧ���ʼӿ죬��B��ѡ��
C���ϳɰ���ҵ��ʹ�ô��������ͷ�Ӧ����Ļ�ܣ���Ӧ���ʼӿ죬��C��ѡ��
D���ڼ��������£���������ԭ����ͭ���¶����ߣ���Ӧ���ʼӿ죬��D��ѡ��
��ѡA��
���������
�����Ѷȣ�һ��