| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《化学平衡》考点巩固(2017年最新版)(六)
参考答案:D 本题解析:A、B项:平衡常数只有温度有关,故错;C项:化学平衡是动态平衡,反应没有停止,故错。故选D。 本题难度:一般 3、选择题 一定量的化合物A放入容积恒定的容器中,在一定条件下发生如下反应: 参考答案:A 本题解析:略 本题难度:一般 4、填空题 研究NOx(氮的氧化物)SO2、CO等大气污染气体的测量及处理具有重要意义。 参考答案:(1)-234.0(2分) 本题解析:(1)由图示知该反应为放热反应,故该反应焓变△H=-(368.0-134.0)kJ/mol=-234.0kJ、mol。(2)①v(CO2)=0.9mol÷(2L×l0min)=0.045mol/(L・min);②固体浓度视为常数,不计入平衡常数表达式,因此可利用反应方程式直接写出该反应的平衡常数表达式;③因正反应是气体体积减少的放热反应,因此可采取加压或增加CO的浓度来提高正反应速率且同时提高SO2的转化率。(3)利用题给反应条件知,每产生22.4 L标准状况下CO2,必有2mol氮的氧化物气体被吸收且混合气体的质量为88 g(放出CO2的质量与溶液增加质量的和),设88 g混合气体中含有NO、NO2的物质的量分别为。xmol、ymol,利用分析,结合题中数据可得:x+y=2、30x+46y=88,两式联立解得x="0.25" mol、y=1.75mol,故混合气体中V(NO):V(NO2)=n(NO):n(NO2)=0.25:1.75=1:7。 本题难度:一般 5、简答题 (的0ww?漳州g模)纳米氧化镁具有特殊的热、光、电、力学和化学等性能,有广泛的应用前景.如e是利用海水制备纳米氧化镁的流程e.
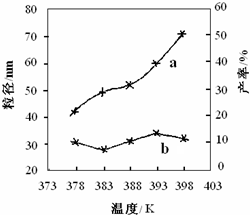 参考答案:(1)由于Ksp[Mg(OH)2]=c(Mg2+)?c2(OH-)=1.l×10-11,当溶液手c(Mg2+)=10-3mol?L-1,开始沉淀需要OH-浓度为c(OH-)= 本题解析: 本题难度:一般 |
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:高中化学知识点总结《影响化学反.. | ||