| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《化学平衡》考点巩固(2017年最新版)(八)
参考答案: 本题解析::(1)根据题给化学方程式结合平衡常数表达式的书写原则写出上述反应的平衡常数表达式为:c4(H2O)/c4(H2);(2)①根据题给图像分析,与曲线a比较,曲线b缩短了达平衡的时间,氢气的平衡浓度未发生变化,则曲线b改变的条件为使用催化剂;②与曲线a比较,曲线c缩短了达平衡的时间,氢气的平衡浓度减小,则曲线c改变的条件为升高温度; 温度升高,达平衡时间缩短,平衡时H2浓度减少,说明升高温度平衡向正反应方向移动。该反应的△H>0;(3)①该温度下,向2L盛有1.42g Na2SO4的密闭容器中通入H2,5min后测得固体质量为1.10g,固体质量减少0.32g,利用差量法计算,则该时间范围内参加反应氢气的物质的量0.02mol,根据v=△n/V△t计算,则该时间范围内的平均反应速率v(H2)=0.002mol/(L.min);②A、该反应为反应前后气体物质的量不变的反应,容器内压强不随反应的进行而变化,不能作为平衡标志,错误;B、容器内气体密度随反应的进行而变化,密度不变已达平衡,正确;C、达平衡后c(H2)和c(H2O)不一定相等,错误;D、v正(H2)=v逆(H2O),说明反应已达平衡,正确;答案选B、D。 本题难度:一般 3、选择题 2SO2(g)+O2(g)
A.乙中SO3的平衡转化率为 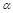 1=20% 1=20% B.平衡时,丙中c(SO3)是甲中的2倍 C.平衡时, 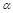 3< 3<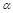 1 1 D.该温度下,平衡常数的值为400 参考答案:CD 本题解析:对于甲,由于SO2的转化率是80%,所以平衡时各种物质的物质的量分别是:n(SO2)=0.08mol;n(O2)=0.08mol;n(SO3)=0.32mol;所以在该温度下的化学平衡产生K= 本题难度:困难 4、填空题 (12分)在一定条件下,存在如下反应:2SO2(g)+ O2 (g) | |||||||||||||||||||||||||||||||||
参考答案:(12分)
(1)(1分)
6.减小、减小、增大 (各1分,共3分)(3)15-20min和25-30min (2分)
(4)增大O2浓度(通入O2)(1分) AB(2分)
(5)中(1分) Kb=10-9/(a-0.01)mol・L-1.(单位不算分,2分)
本题解析:略
本题难度:困难
5、选择题 实验证明:若用电解熔融KCl制钾,发现钾熔于熔融KCl中难分离,且电解过程中容易发生爆炸事故等。因而工业不用电解熔融KCl制钾,而用金属钠与KCl共熔置换制钾:
Na(l)+KCl(l) NaCl(l)+K(g) △H>0。 下面是四种物质的熔沸点:
NaCl(l)+K(g) △H>0。 下面是四种物质的熔沸点:
| | K | Na | KCl | NaCl |
| 熔点/℃ | 63.6 | 97.8 | 770 | 801 |
| 沸点/℃ | 774 | 882.9 | 1500 | 1413 |
参考答案:
本题解析:
本题难度:一般
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:高中化学知识点总结《影响化学反.. | ||