�о�������H2O2�ֽ����ʵ�Ӱ��
�ο��𰸣�AD
���������ѡ��A����ȷ����Ϊ�ڼ���������Һ֮ǰû�м������������к����ᣬ���ܷ���������Ӧ��Ҫ̽��������˫��ˮ�ֽ����ʵ�Ӱ�죬���Թ���˫��ˮ��Ũ��Ӧ������ȵģ�����ѡ��D����ȷ��ѡ��BC��ȷ����ѡAD��
�����Ѷȣ�һ��
2��ʵ���� Ӱ�컯ѧ��Ӧ���ʵ����غܶ࣬ij������ȤС����ʵ��ķ�������̽����
ʵ��һ����������Cu��Fe��Mg�Ͳ�ͬŨ�ȵ����ᣨ0.5mol/L��2mol/L��18.4mol/L�������ʵ�鷽�����о�Ӱ�췴Ӧ���ʵ����ء�
(1)��ͬѧ�о���ʵ�鱨�����±���
ʵ?��?��?��
| ��?��
| ��?��
| �ٷֱ�ȡ�������2 mol/L�������Թ��У�
�ڷֱ�Ͷ���С����״��ͬ��Cu��Fe��Mg��
| ��Ӧ������
Mg>Fe>Cu
| ��Ӧ�������Խ���ã���Ӧ����Խ�졣
|
��ͬѧ��ʵ��Ŀ�����о�____________�Է�Ӧ���ʵ�Ӱ�죻���ݿ��Ʊ�������Ҫ�ó���ȷ��ʵ����ۣ�������Ƶ�ʵ�������DZ���______________������ͬ��
(2)��ͬѧΪ�˸���ȷ���о�Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죬������ͼװ�ý��ж���ʵ�顣��ɸ�ʵ��Ӧѡ�õ�ʵ��ҩƷ��_____________��Ӧ�òⶨ��ʵ��������________________________��
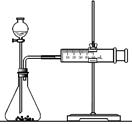
ʵ�������֪2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2�����ڸ������������Һ�Ͳ�����Һ��Ӧʱ�����ֿ�ʼһ��ʱ�䣬��Ӧ���ʽ�������Һ��ɫ�����ԣ�������ͻȻ��ɫ����Ӧ�������Լӿ졣
(1)�������ʵ������ijͬѧ��ΪKMnO4��H2C2O4��Ӧ�Ƿ��ȷ�Ӧ��������Һ�¶����ߣ���Ӧ���ʼӿ졣��Ӱ�컯ѧ��Ӧ���ʵ����ؿ�����IJ��뻹������________ ______��Ӱ�졣
(2)����ʵ��֤����IJ��룬�����Ը��������Һ��������Һ�Լ��⣬����Ҫѡ����Լ����������______��
A�������? B��������? C��ˮ? D���Ȼ���
�ο��𰸣���12�֣�
ʵ��һ��(1)��Ӧ�ﱾ�������ʶԷ�Ӧ���ʵĹ�ϵ����2�֣�
�¶���ͬ����2�֣�
(2)Mg(��Fe)��0.5mol/L�����2mol/L�����2�֣�
�ⶨһ��ʱ������������������߲ⶨһ���������������ʱ�䣩����2�֣�
ʵ�����(1)����(�������̻�Mn2+�Ĵ�����)����2�֣�
(2)B��2�֣�
���������ʵ��һ��(1)���ݱ��е���Ϣ�ó���ͬѧ��ʵ��Ŀ�����о���Ӧ�ﱾ�������ʶԷ�Ӧ���ʵĹ�ϵ�Է�Ӧ���ʵ�Ӱ�졣�¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ��ϴʸ��ݿ��Ʊ�������Ҫ�ó���ȷ��ʵ����ۣ�������Ƶ�ʵ�������DZ����¶���ͬ��
(2)����װ��ͼ���Եõ�����ͨ��������������������о�Ũ�ȶԷ�Ӧ���ʵ�Ӱ�졣�ʸ�ʵ��Ӧѡ�õ�ʵ��ҩƷ��Mg(��Fe)��0.5mol/L�����2mol/L���ᡣӦ�òⶨ��ʵ��������Ӧ�òⶨ��ʵ�����ݡ�
ʵ�����(1)�Ի�ѧ��Ӧ����Ӱ�������Ǵ������ʲ��뻹�����Ǵ�����Ӱ�졣
(2)ѡ��������������Լ������������ѡB��
������Ӱ�컯ѧ��Ӧ���ʵ�����������¶ȡ�Ũ�ȡ�ѹǿ�������⣬���кܶ����ؿ��Ըı䷴Ӧ���ʣ������䡢���������绡�����⡢ǿ�ų���������ĥ����Ӧ�������С����ɢ���ʡ��ܼ��ȣ���֮����Ӧ��ϵ���������������п��ܸı䷴Ӧ���ʣ��������ֻ��Ӱ�췴Ӧ���ʣ�������ѧ��Ӧ���ʵ������ʱ��������ʡ�
�����Ѷȣ�һ��
3������� ijѧ����0.1��10��25�L3������������99.5%����Ƭ���ᷴӦ��ȡH2��ʵ��������±���
| 1min | 2min | 5min | 15min | 20min
3mol/L?HCl
��������
�϶�����
��������
��Ӧ����
��Ƭ�ľ�
1.5mol/L?H2SO4 | ������������ֻ���������ݣ�
|
��1��д����Ƭ���ᷴӦ�����ӷ���ʽ______��
��2����Ӧ1-15min�ڣ���������ķ�Ӧ�����ӿ죬��ԭ����______��
��3��������Ƭ����������ᷴӦ����IJ��죬����˼�������������²��룺
����һ��______���������______��
�ο��𰸣���1����Ƭ���ᷴӦ2Al+6HCl=2AlCl3+3H2�������ӷ���ʽΪ��2Al+6H+�T2Al3++3H2�����ʴ�Ϊ��2Al+6H+�T2Al3++3H2����?
��2����Ƭ���ᷴӦΪ���ȷ�Ӧ����Ӧ�����¶����ߣ���ѧ��Ӧ���ʼӿ죬�ʴ�Ϊ����Ӧ�����¶����ߣ���ѧ��Ӧ���ʼӿ죻
��3������������������Ӳ�ͬ��������Cl-�Ը÷�Ӧ�дٽ����ã�SO42-�Ը÷�Ӧ���������ã��ʴ�Ϊ��Cl-�Ը÷�Ӧ�дٽ����ã�SO42-�Ը÷�Ӧ���������ã�
���������
�����Ѷȣ�һ��
4������� ���ܱ������з������з�Ӧ��I2��g��+H2��g��?2HI��g����H��0����ʼʱ��n��H2��=a?mol��n��I2��=b?mol��ֻ�ı�����г��������������������䣬�Խ���ѧ��Ӧ���ʵĸı䣨����������С�����䡱��������Ӧ�ı���
| ��� | ��Ӧ���� | ��Ӧ����
��
�������
______
��
�ٳ���a?mol?H2
______
��
�������ݻ�����Ϊԭ��2��
______
��
�����ݻ����䣬ͨ��b?mol?Ne��g��
______
�ο��𰸣����������������Ӧ�������ʴ�Ϊ������?
���ٳ���a?molH2����Ӧ��Ũ������ѧ��Ӧ�������ʴ�Ϊ������
�۽������ݻ�����Ϊԭ��2�����൱�ڼ�Сѹǿ����Ӧ���ʼ�С���ʴ�Ϊ����С��
�������ݻ����䣬ͨ��b?mol?Ne��g������Ӧ��ϵ�и����ʵ�Ũ�Ȳ��䣬��Ӧ���ʲ��䣬�ʴ�Ϊ�����䣮
���������
�����Ѷȣ�һ��
5��ѡ���� �����������Һ��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ��Na2S2O3+H2SO4=Na2SO4+SO2��+S��+H2O�����и���ʵ�������ȳ��ֻ��ǵ���
[? ]
������Ӧ�¶�/�桡Na2S2O3��ҺV/mL c/(mol��L-1)��ϡH2SO4V/mLc/(mol��L-1)��H2OV/mL
A.������25����������������5��0.1������������������10��0.1��������������5
B.������25����������������5��0.2������������������5��0.2��������������10
C.������35����������������5��0.1������������������10��0.1��������������5
D.������35����������������5��0.2������������������5��0.2��������������10
�ο��𰸣�D
���������
�����Ѷȣ�һ��
|
|