微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知稀H2SO4的浓度相等,有下列两种装置如图,下列说法正确的是( )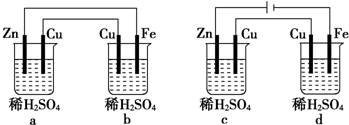
A.a、b均为原电池
B.c、d均为电解池
C.b池中Fe极反应为Fe-2e-═Fe2+
D.d池中Cu极反应为4OH--4e-═O2↑+2H2O
参考答案:因失电子能力Zn>Fe,则a为原电池,b为电解池,c、d都外接电源,都为电解池,
A.a为原电池,b为电解池,故A错误;
B.c、d都外接电源,都为电解池,故B正确;
C.b为电解池,Fe极反应为2H++2e-═H2↑,故C错误;
D.d中Cu为阳极,被氧化,电极反应为Cu-2e-═Cu2+,故D错误.
故选B.
本题解析:
本题难度:一般
2、填空题 如下图所示装置:
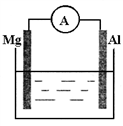
(1)若烧杯中溶液为稀硫酸,则观察到的现象为_________。两极反应式为:正极_________; 负极___________。该装置将______能转化为_________能。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为__________,总反应方程式为___________。
参考答案:(1)镁逐渐溶解,铝极上有气泡冒出,电流表指针发生偏转;正极:2H++2e-=H2↑;负极:Mg-2e-=Mg2+?;化学能;电能
(2)Al;2Al+2NaOH+2H2O=2NaAlO2+3H2↑
本题解析:
本题难度:一般
3、选择题 根据图所示装置,下列说法不正确的是( )

选项
| 开关状态
| 溶液A
| 电极B
| 说明
|
A
| 打开K1,闭合K2
| NaCl
| 石墨
| 正极反应:O2+2H2O+4e-=4OH-
|
B
| 打开K1,闭合K2
| NaCl
| Zn
| 铁制品保护:牺牲阳极的阴极保护法
|
C
| 打开K2,闭合K1
| CuSO4
| Cu
| 铁表面镀铜
|
D
| 打开K2,闭合K1
| CuSO4
| 粗铜
| 电解法精炼铜
|
?
参考答案:D
本题解析:电解法精炼铜时阴极材料应为精铜,D项错误。
本题难度:一般
4、选择题 如图所示的Cu?Zn原电池,下列叙述正确的是
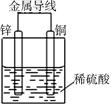
A.氢离子在负极得电子
B.锌为负极,发生氧化反应
C.铜为负极,铜片上有气泡产生
D.电子从铜极流向锌极
参考答案:B
本题解析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。锌比铜活泼,据此可知,锌是负极,铜是正极,溶液中的氢离子在正极放电,所以选项B正确,答案选B。
点评:该题是高考中的常见题型,属于基础性试题的考查,难度不大。该题的关键是明确原电池的工作原理,有利于培养学生的逻辑推理能力。
本题难度:简单
5、填空题 (1)如下图所示,组成一种原电池.试回答下列问题(灯泡功率合适):
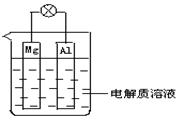
①电解质溶液为稀H2SO4时上述装置中灯泡亮,此时Al电极上发生反应的电极反应式为: ___;
②电解质溶液为NaOH溶液时,灯泡______(填“亮”或“不亮”, 填“亮”做a题,填“不亮”做b题)。
a.若灯泡亮,则Mg电极上发生的电极反应式为:_______________;
Al电极上发生反应的电极反应式为:_______________;
b.若灯泡不亮,其理由为:________________________。
(2)原电池原理的应用之一是可以设计原电池。请利用反应“Cu+2Fe3+ =2Fe2+ +Cu2+ ”设制一个原电池(正极材料用碳棒)则该电池的负极材料是__________,若导线上转移电子1.5 mol,则溶解铜的质量是__________。另外的重要应用是实验室在用锌与稀硫酸反应制备氢气时,可向溶液中滴加少量硫酸铜溶液。其作用是: ______________________________。
(3)氢氧燃料电池(电解质为KOH溶液,惰性材料作电极)负极反应的电极反应式为:______________________________。
参考答案:(1)①2H+ + 2e- = H2↑;
②亮 a. 6H2O + 6e- = 6OH- + 3H2↑;2Al – 6e- + 8OH- =2AlO2- + 4H2O。
(2)Cu;48g;形成了Zn—Cu原电池,加快了化学反应的速率(注:必须强调形成Zn—Cu原电池,否则不得分);(3)H2 +2 OH- - 2e-=2H2O
本题解析:(1)①分析题给装置图,当电解质溶液为稀H2SO4时上述装置中灯泡亮,则形成原电池,镁较活泼,作原电池的负极,Al片作原电池的正极,电极反应式:2H+ + 2e- = H2↑;②电解质溶液为NaOH溶液时,Al片作负极,Mg片作正极,灯光亮,Mg电极上发生的电极反应式为a. 6H2O + 6e- = 6OH- + 3H2↑;Al电极上发生反应的电极反应式为:2Al – 6e- + 8OH- =2AlO2- + 4H2O;(2)结合Cu+2Fe3+ =2Fe2+ +Cu2+知,铜片发生氧化反应,负极材料是Cu片,电极反应式为Cu-2e- =Cu2+ ,若导线上转移电子1.5 mol,则溶解铜的质量是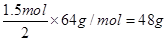 ,实验室在用锌与稀硫酸反应制备氢气时,可向溶液中滴加少量硫酸铜溶液的作用是形成了Zn—Cu原电池,加快了化学反应的速率;(3)氢氧燃料电池(电解质为KOH溶液,惰性材料作电极)负极反应的电极反应式为H2 +2 OH- - 2e-=2H2O。
,实验室在用锌与稀硫酸反应制备氢气时,可向溶液中滴加少量硫酸铜溶液的作用是形成了Zn—Cu原电池,加快了化学反应的速率;(3)氢氧燃料电池(电解质为KOH溶液,惰性材料作电极)负极反应的电极反应式为H2 +2 OH- - 2e-=2H2O。
本题难度:一般