��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ƣ�NaN3������ɫ���Ӿ��壬�����»�������ܷ���ǿ�ұ�ը�����ٷֽ���Ƶ��ʺ͵�������������ȫ�����еijɷ�֮һ�������й�˵����ȷ����
A��NaN3��ֻ�������Ӽ�
B��1molNaN3��ȫ�ֽ������Բ���33.6LN2
C��NaN3���ٷֽ�ʱ��NaN3���������������ǻ�ԭ��
D�������£�NaN3��ѧ�����ȶ�����װ���������ر�˵��ע������
�ο��𰸣�C
���������NaN3��Na+��N3�����ɵ����ӻ����N3���е�Ԫ���뵪Ԫ��֮�仹���ڹ��ۼ�����Aѡ�����������ɵã�2NaN3 2Na+3N2������������N2��NaN3��ϵ��֮�ȵ������ʵ���֮�ȣ���1mol NaN3��ȫ�ֽ������Բ���1.5molN2������ȱ���¶Ⱥ�ѹǿ������Ħ�������һ����22.4L/mol�������������һ����33.6L����Bѡ���������2NaN3
2Na+3N2������������N2��NaN3��ϵ��֮�ȵ������ʵ���֮�ȣ���1mol NaN3��ȫ�ֽ������Բ���1.5molN2������ȱ���¶Ⱥ�ѹǿ������Ħ�������һ����22.4L/mol�������������һ����33.6L����Bѡ���������2NaN3 2Na+3N2������Ԫ�ػ��ϼ۽��ͣ���Ԫ�ػ��ϼ����ߣ���NaN3�������������ǻ�ԭ������Cѡ����ȷ������NaN3�ڸ��»�������ܹ�����ǿ�ұ�ը�������Ҫ˵����ȫ��ʾ��־����Dѡ�����
2Na+3N2������Ԫ�ػ��ϼ۽��ͣ���Ԫ�ػ��ϼ����ߣ���NaN3�������������ǻ�ԭ������Cѡ����ȷ������NaN3�ڸ��»�������ܹ�����ǿ�ұ�ը�������Ҫ˵����ȫ��ʾ��־����Dѡ�����
�����Ѷȣ�һ��
2������� ��12�֣�X��Y��Z��WΪ����������ͬ�����������ӻ���ӣ�����X��5��ԭ�Ӻˣ���Щ����һ��������������ת����ϵ��ͼ�в��ַ�Ӧ����P��Ӧ��������ȥ����
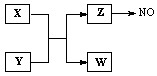
��1��Z ��NO��Ӧ�Ļ�ѧ����ʽ�ǣ�?
Һ̬ Z��ˮ�ĵ������ƣ����д��ڵĵ�������ͬ����������?��
��2��ʵ�����м���Z�Ļ�ѧ�Լ��������ǣ�
?
| ?��ѧ�Լ�
| ?����
|
����һ
| ?
| ?
|
������
| ?
| ?
|
��3���ɹ���X��Y������Ԫ������ɵ�һ�����ӻ����������Ԫ��ԭ����֮��Ϊ2��4��3�������ӻ�������?����д��ѧʽ����
��4��һ�������£�Z��һ�����������������Ӧ�����������ֺ��ȶ��IJ�����ж���������Z�Ļ������20 mL�ڸ������·�Ӧ��ʵ�ʲμӷ�Ӧ�Ķ���������Z��2 mL����ԭ���������Z������������������?��
�ο��𰸣���12�֣�
��1�� ? NH2����NH4+
? NH2����NH4+
��2��
?
?��ѧ�Լ�
?����
����һ
��ʪ��ĺ�ɫʯ����ֽ���飨1�֣�
��ֽ��Ϊ��ɫ��1�֣�
������
պ��Ũ����IJ��������飨1�֣�
�а������ɣ�1�֣�
��3��NH4NO3��
��4��2�s3��7:3
���������������Ҫ���������ṹ�����������ʼ����飻������ԭ��Ӧ�����֪ʶ��
��1�����볣����10���������������������֪����XΪNH4+��YΪOH����ZΪNH3��WΪH2O��
��4��4NH3 + 3NO2 =2N2 + 6H2O
��μӷ�Ӧ��NH3Ϊa ml����μӷ�Ӧ��NO2Ϊ3a/4����a-3a/4=2��a=8��
���Բμӷ�Ӧ��NH3Ϊ8 ml��NO2Ϊ6ml�����ڶ��߹�20 ml�����������
NH3������NH3Ϊ14 ml��NO2Ϊ6 ml�����������Ϊ7:3
NO2������NH3Ϊ8 ml��NO2Ϊ12 ml�����������Ϊ2:3
�����Ѷȣ�һ��
3��ѡ���� ��26.4 g��NH4��2SO4��������Ca(OH)2��ϼ��ȣ��ų�������ȫ��������39.2 g��H3PO4��Һ���գ����ɵ����ǣ�?��
A��(NH4)3PO4
B��NH4H2PO4
C��(NH4)2HPO4
D��(NH4)3PO4��NH4H2PO4
�ο��𰸣�B
�������������NH3Ϊ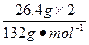 ="0.4" mol��H3PO4Ϊ
="0.4" mol��H3PO4Ϊ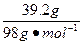 ="0.4" mol������NH3��H3PO4�����ʵ���֮��Ϊ1��1,������NH4H2PO4��
="0.4" mol������NH3��H3PO4�����ʵ���֮��Ϊ1��1,������NH4H2PO4��
�����Ѷȣ���
4������� ��10�֣����亽�������õ����⻯���£�N2H4����ȼ�ϡ��Իش������й����⣺
��1��N2H4ȼ��ʱ��NO2�����������������Ӧ���ɵ�����ˮ������
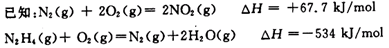
��N2H4��NO2��Ӧ���ɵ�����ˮ�������Ȼ�ѧ����ʽΪ?��
��2�������¡�������KOH��Һ��ɼ���ȼ�ϵ�أ���Ԫ�ر�������ֻ���ɵ�������д���õ�ع���ʱ�����ĵ缫��Ӧ?����ع���ʱ��?��pH���ߡ�
��3����ͳ�Ʊ��µķ���������NaClO����NH3���Ƶ��µ�ϡ��Һ���÷�Ӧ�Ļ�ѧ����ʽ?��
��4�������£�N2H6Cl2����һ����Ҫ�Ļ���ԭ�ϣ��������ӻ����������ˮ����Һ�����ԣ�ˮ��ԭ����NH4Cl���ơ�д�������µ�һ��ˮ�ⷴӦ�����ӷ���ʽ?��
�ο��𰸣�
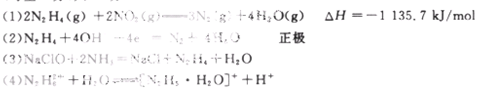
�����������1������������ʽ���ӵã�N2H4��NO2��Ӧ���ɵ�����ˮ�������Ȼ�ѧ����ʽΪ
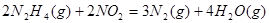 ��
�� ��
��
��2����ع���ʱ�����ĵ缫��ӦΪ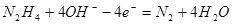 ����ع���ʱ������PH���ߣ�
����ع���ʱ������PH���ߣ�
��3����ͳ�Ʊ��µķ���������NaClO����NH3���Ƶ��µ�ϡ��Һ���÷�Ӧ�Ļ�ѧ����ʽΪ��

��4�� ?
?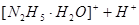
�����Ѷȣ���
5��ѡ���� �»�����Ȫ9��20�յ磺���ҹ��������Ƶġ�������ϵ�����ػ�����й�������������ع��ߣ���1996��10������������������366�γɹ����䡣��ij����ƽ����е�ȼ����Һ̬ƫ������[(CH3)2N��NH2]����������N2O4�������ķ�Ӧ��дΪ��(CH3)2N��NH2��2N2O4===3N2����2CO2����4H2O���������й�˵������ȷ����(����)
A���������˲�䣬�ݳ�����ɫ������NO2
B��ƫ������[(CH3)2��N��NH2]���������[CH3NH��NH��CH3]�е㲻��ͬ
C��ÿ����3 mol������ת�Ƶ��ӵ����ʵ���Ϊ16 mol
D��������ɴ������б��ڵ����ϸ�����������ʵ��
�ο��𰸣�D
�����������N2O4?2NO2�����ݳ��ĺ���ɫ������NO2��A����ȷ��ƫ��������������£���Ϊͬ���칹�壬���۷е㲻��ͬ��B����ȷ����Ӧ������ÿ����3 mol������ת��16 mol���ӣ�C����ȷ����������ɴ������д���ʧ��״̬������ʵ��������Խ��У�D�����
�����Ѷȣ�һ��