微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 114号元素的一种同位素是由俄罗斯科学家合成的,存在时间只有30s,其质量数为289,该原子的中子数与电子数之差为
A.61
B.114
C.175
D.289
参考答案:A
本题解析:根据质量数=质子数+中子数,可得中子数为289-114=175,质子数=电子数=114,可得中子数与电子数只差为175-114=61,选A。
本题难度:一般
2、选择题 已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是
A.原子半径:A>B>D>C
B.单质的还原性:A>B>D>C
C.原子序数:d>c>b>a
D.离子半径:C>D>B>A
参考答案:D
本题解析:A为镁,B为钠,C为氮,D为氟。电子层数越多,半径越大,电子层数相同时,半径随原子序数的增大而减小,半径越小,其对应的氧化性,非金属性,酸性,热稳定性就越强,半径越大,其对应的还原性,金属性,碱性就越强,因此答案选D
本题难度:一般
3、填空题 (10分)第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。
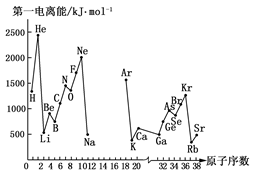
请回答以下问题:
(1)认真分析上图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小(最小)范围为________<Al<________(填元素符号)。
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是________。
(3)上图中第一电离能最小的元素在周期表中的位置是________。
(4)根据对角线规则,Be、Al元素最高氧化物的水化物性质相似,它们都具有________,
参考答案:(1)Na Mg? (2)从上到下依次减小? (3)第五周期 ⅠA族? (4)两性
本题解析:(1)金属性越强,第一电离能越小。同主族自左向右金属性逐渐降低,第一电离能逐渐增大。但由于镁元素的3s轨道是全充满状态,稳定性强,所以第一电离能大于Al的,即Al的第一电离能的大小(最小)范围为An<Al<Mg。
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是从上到下依次减小。
(3)根据图像中的数据可知,第一电离能最小的是Rb,位于第五周期第ⅠA族。
(4)Be、Al两种元素处于对角线位置,所以元素最高氧化物的水化物性质相似,它们都具有两性。
点评:该题是中等难度的试题,试题注重基础和能力的双向考查。该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。
本题难度:一般
4、选择题 下列叙述中,金属a的活泼性肯定比金属b的活泼性强的是 (? )?
A.a原子的最外层电子数比B原子的最外层电子数少
B.a原子电子层数比b原子的电子层数多
C.1mol a 从酸中置换H+生成的H2比b从酸中置换H+生成的H2 要容易
D.常温时,b能从水中置换出氢,而a不能
参考答案:C
本题解析:金属活动性强弱的判断依据有,与水或酸反应置换氢气的难易程度、活动性强的单质能置换活动性弱的单质、最高价氧化物水化物的碱性的强弱、构成原电池时的负极材料比正极材料活泼等,A、B不作为判断金属活动性的依据,错误;D、常温时,b能从水中置换出氢,而a不能,说明b比a活泼,错误;C、a 从酸中置换H+生成的H2比b从酸中置换H+生成的H2 要容易,说明a比b活泼,正确,所以答案选C。
本题难度:一般
5、选择题 常温下,将pH=1的硫酸溶液平均分成两等份,一份加入适量水,另一份加入与该硫酸溶液物质的量浓度相同的氢氧化钠溶液,两者pH都升高了1,则加入的水和氢氧化钠溶液的体积比为( )
A.5:1
B.6: 1
C.10:1
D.11:1
参考答案:B
本题解析:设每份硫酸溶液体积都为V,每份溶液中c(H+)=0.1mol/L。
一份加水pH升高1,可得: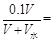 0.01;
0.01;
另一份加入与硫酸等浓度氢氧化钠溶液pH升高1,可得: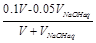 =0.01。
=0.01。
由以上二式解得水和氢氧化钠溶液体积比为6:1。
点评:pH=-lgc(H+)。
本题难度:简单