微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各组离子在碱性条件下可以大量共存,而在强酸性条件下能发生氧化还原反应的是
[? ]
A.Cu2+、Fe2+、NO3-、Cl-
B.K+、Mg2+、HCO3-、SO42-
C.Na+、K+、S2-、SO42-
D.Ba2+、Na+、I-、Cl-
参考答案:C
本题解析:
本题难度:一般
2、选择题 下列说法错误的是
A.某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性
B.等物质的量浓度的醋酸与醋酸钠溶液中水电离产生的c(OH-)前者小于后者
C.沉淀溶解达到平衡时,溶液中溶质的离子浓度不一定相等,但保持不变
D.水的离子积只与温度有关,向水中加入酸、碱或盐一定会影响水的电离平衡
参考答案:D
本题解析:
试题分析:A、碱能使石蕊试液变蓝色,因此某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性,A正确;B、醋酸是弱酸,抑制水的电离,醋酸钠溶液中CH3COO-水解,促进水的电离,因此等物质的量浓度的醋酸与醋酸钠溶液中水电离产生的c(OH-)前者小于后者,B正确;C、在一定温度下,当难溶强电解质溶于水形成饱和溶液时,溶解速率和生成沉淀速率相等的状态,因此沉淀溶解达到平衡时,溶液中溶质的离子浓度不一定相等,但保持不变,C正确;D、酸或碱一定会影响水的电离平衡,但盐不一定影响,只有能水解的盐才能影响,不水解的盐不影响,例如硫酸钠不能影响水的电离平衡,D不正确,答案选D。
本题难度:一般
3、填空题 (15分)某无色溶液中可能含有NH4+、K+、Al3+、HCO3―、Cl―、MnO4―、SO42―等离子中的几种离子。
①经实验可知溶液明显呈酸性,且焰色反应呈现出紫色。
②取10mL该溶液于试管中滴加Ba(NO3)2溶液,加稀硝酸酸化后过滤得到0.03mol白色沉淀,向滤液中加入AgNO3溶液未见沉淀产生。
③另取少量该溶液于试管中,滴加NaOH溶液产生白色沉淀,当沉淀增加到一定量后开始产生气体,最后沉淀完全溶解。
(1)该溶液中一定不含有?(填离子的化学式)离子,一定含有的离子有?(填离子的化学式);
(2)在这些不存在的离子中,有一种离子在酸性环境中和碱性环境中都不能存在,试写出该离子与酸反应的离子方程式:?;
(3)为确定上述溶液中所含的各种离子的物质的量,取100mL上述溶液并向其中加入Na2O2固体,产生的沉淀和气体与所加Na2O2固体物质的量的关系曲线如图Ⅰ:
?
①该溶液中焰色反应呈现紫色的离子的物质的量为:?mol,
②写出n(Na2O2)=0.2mol时反应的总离子方程式:?;
(4)将0.1mol明矾晶体与等物质的量的某无水盐晶体X混合后溶解于水中,所得溶液与上述溶液所含离子种类完全相同。若向该溶液中加入Ba(OH)2溶液,所得沉淀的物质的量与所加入Ba(OH)2的物质的量的关系如图Ⅱ:
?
试根据图像推断①X的化学式:?,②图像中A点溶液中的离子成分和物质的量分别是:?;
参考答案:(1)HCO3―、Cl―、MnO4―(2分),K+、NH4+、Al3+、SO42―(2分);
(2)HCO3―+H+=CO2↑+H2O(2分);
(3)①0.1(2分)
②Al3++NH4++2Na2O2+H2O=Al(OH)3↓+NH3↑+O2↑+4Na+(2分);
(4)①(NH4)2SO4 (2分);
②0.1mol K+、0.2mol NH4+、0.15mol SO42―(3分)。
本题解析:根据题意和实验现象说明一定无HCO3―、Cl―、MnO4―;一定含有的K+、NH4+、Al3+、SO42―离子。
本题难度:一般
4、选择题 某黄色溶液中可能含有下列离子:K+,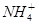 ,Fe3+,Ba2+,
,Fe3+,Ba2+,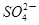 ,Cl-,S2-,为检验其成分,先对溶液进行初步分析.下列判断不正确的是
,Cl-,S2-,为检验其成分,先对溶液进行初步分析.下列判断不正确的是
A.溶液中存在大量Fe3+
B.溶液中可能存在大量Ba2+
C.溶液中不存在S2-
D.溶液可能呈强碱性
参考答案:D
本题解析:因某溶液为黄色,所以肯定含Fe3+,A 正确,Ba2+和Fe3+能共存,所以可能含有大量的Ba2+,B 正确。Fe3+具有强的氧化性,不能有还原性的离子,C正确,溶液不可能呈强碱性,因Fe3+与OH-不能大量共存,D 错。
本题难度:简单
5、选择题 在指定环境中,下列各组离子一定可以大量共存的是
①pH试纸变成深蓝色的溶液中:SO32-、S2O32-、Na+
②含有大量S2-的溶液中:Na+、ClO-、Cl-、CO32-
③AlCl3溶液中:K+、SiO32-、NH4+、NO3-
④中性溶液中:Cu2+、Fe3+、SO42-、Cl-
⑤加入铝粉放出氢气的溶液:Na+、Cl-、NH4+、NO3-
⑥在含有大量HCO3-的溶液中:K+、Na+、AlO2-、Br-
A.①③④
B.只有①
C.②④⑤
D.①④⑥
参考答案:B
本题解析:①pH试纸变成深蓝色的溶液为碱性溶液,共存,正确;②S2-被ClO-氧化不能共存,错误;③AlCl3与SiO32-双水解不能大量共存,错误;④Cu2+、Fe3+只能存在酸性溶液中,错误;⑤加入铝粉放出氢气的溶液可以是酸溶液,也可以是碱溶液,强碱性条件下NH4+不能共存,错误;⑥HCO3-和AlO2-反应生成氢氧化铝和碳酸根离子不能大量共存,错误。
本题难度:一般