微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 某化学研究性学习小组拟采用粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)制取无水氯化铜并测定样品中氧化铜的质量分数,其实验流程如图所示:
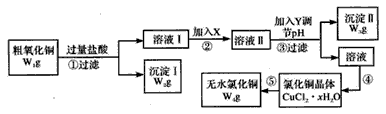
实验过程中的pH调节为:
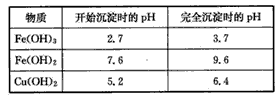
请回答以下问题:
(1)步骤①、③过滤操作中,除用到仪器:铁架台(带铁圈)、漏斗、烧杯外,还需要使用的仪器用品有________。
(2)步骤①中发生的离子反应方程式为________、____。
(3)步骤②溶液I中加入试剂X可以是____(填下列试剂的编号)。
A.氢氧化钠
B.氯水
C.碱式碳酸铜
D.氧化铜
(4)步骤③中将溶液pH调节到的范围是____。
(5)步骤⑤要得到无水氯化铜,需要在干燥的HCl气流中加热CuCl2・xH2O,其原因是____ 。
(6)经检测,CuCl2・xH2O中含水28. 6%,则CuCl2・xH2O中x的值为____。
(7)若步骤④中80%的氯化铜转入晶体,其余各步转化都是完全的,请根据流程图中表示的质量数据,写出 样品中氧化铜质量分数的计算式。
2、选择题 下列有关实验现象的描述不正确的是?
[? ]
A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 ?
B.把铁放入稀硫酸中,加几滴氯化铜溶液,产生气泡速率加快 ?
C.溴水加入到淀粉碘化钾溶液中,溶液变蓝? ?
D.乙烯通入到高锰酸钾溶液中,溶液变成紫色
3、选择题 下列实验不能达到目的的是
[? ]
A.往酸性KMnO4溶液中通入乙烯验证乙烯能够发生氧化反应
B.加热氯化铵与氢氧化钙固体混合物制取氨气
C.用电解饱和食盐水的方法制取氯气
D.除去FeCl2溶液中的Fe3+ ,可用足量Cu单质将Fe3+还原成Fe2+ ,再过滤出去多余的铜
4、简答题 黄铁矿(主要成分为FeS2)是我国大多数硫酸厂制取硫酸的主要原料.某化学学习小组对某黄铁矿石进行如下实验探究.[实验一]测定硫元素的含量.
Ⅰ、将m1g该黄铁矿样品放入如图1所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全.石英管中发生反应的化学方程式为:4FeS2+11O2
2Fe2O3+8SO2.
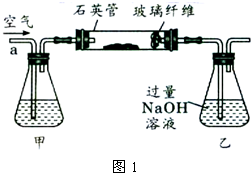
Ⅱ、反应结束后,将乙瓶中的溶液进行如图2所示处理.
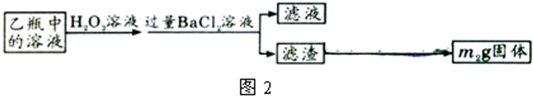
[实验二]测定铁元素的含量.
Ⅲ、测定铁元素含量的实验步骤如图3所示.
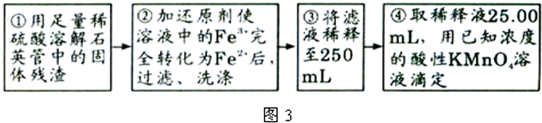
问题讨论:
(1)Ⅰ中,甲瓶内所盛试剂是______溶液.乙瓶内发生反应的离子方程式有:______、______.
(2)Ⅱ中的滤渣在称量前还应进行的操作是______.
(3)Ⅱ中,所加H2O2溶液(氧化剂)需足量的理由是______.
(4)④中取稀释液25.00ml需用的仪器是______.Ⅲ的步骤③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有______(画出其简易装置图).
(5)该黄铁矿中硫元素的质量分数为______.
5、选择题 关于如图所示实验装置及说法中正确的是( )

A.用图①所示实验可比较硫、碳、硅三种元素的非金属性强弱
B.用图②所示实验装置排空气法收集CO2气体
C.用图③可以检验火柴燃烧生成的SO2气体
D.用图④提取海带中的碘