微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知:Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16 ,Ksp(Ag2CrO4)=2.0×10-12,则下列难溶盐的饱和溶液中,大小顺序正确的是(?)
A.AgCl>AgI> Ag2CrO4
B.AgCl> Ag2CrO4>AgI
C.Ag2CrO4>AgCl>AgI
D.Ag2CrO4>AgI>AgCl
参考答案:C
本题解析:AgCl溶液中c(Ag+)=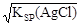 =
= ×10-5,AgI溶液中c(Ag+)=
×10-5,AgI溶液中c(Ag+)=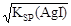 =
= 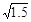 ×10-8,Ag2CrO4溶液中c(Ag+)=
×10-8,Ag2CrO4溶液中c(Ag+)=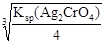 =
= ×10-4,所以Ag+浓度从大到小的顺序是Ag2CrO4>AgCl>AgI。答案选C。
×10-4,所以Ag+浓度从大到小的顺序是Ag2CrO4>AgCl>AgI。答案选C。
点评:本题的关键是不能直接用Ksp的大小来判断溶液中离子浓度的大小。
本题难度:一般
2、选择题 自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO4溶液,向地下深层渗透,遇到难溶的ZnS或PbS,慢慢转变为铜蓝(CuS)。下列分析正确的是?
[? ]
A.CuS的溶解度大于PbS的溶解度
B.原生铜的硫化物具有还原性,而铜蓝没有还原性
C.CuSO4与ZnS反应的离子方程式是Cu2++S2-===CuS↓
D.整个过程涉及的反应类型有氧化还原反应和复分解反应
参考答案:D
本题解析:
本题难度:一般
3、选择题 已知下表数据:
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3
Ksp(25℃)
8.0×10-16
2.2×10-20
4.0×10-38
完全沉淀时的pH范围
≥9.6
≥6.4
3~4
|
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不正确的是( )
A.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
B.该溶液中c(SO42-):[c(Cu2+)]+c(Fe2+)+c(Fe3+)]>5:4
C.向该溶液中加入适量氯水,并调节pH到3~4后过滤,可获得纯净的CuSO4溶液
D.在pH=5的溶液中Fe3+不能大量存在
参考答案:A.从表格中可以看出,Fe(OH)3的Ksp是最小的,所以它最先出现沉淀,故A正确;
B.因为Cu2+、Fe2+、Fe3+对应的碱全是弱碱,所以这三种离子在溶液中都会发生水解,因此它们的物质的量会减少,故B正确;
C.加入氯水,可以把亚铁离子全氧化成三价,但它的还原产物Cl-肯定还在溶液中,而且在调节pH时加入的试剂也会在溶液中有所保留,所以得到的溶液中不可能只含CuSO4一种溶质,故C错误;
D.在pH=5的溶液中c(H+)=10-5moL/L,c(Fe3+)=4×10-38(1×10-5)3mol/L=4×10-13mol/L,Fe3+不能大量存在,故D正确.
故选C.
本题解析:
本题难度:一般
4、选择题 下列液体均处于25℃,有关叙述正确的是
[? ]
A.某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐
B.pH=4的NH4Cl溶液,溶液中c(H+)>c(OH-),且c(H+)/c(OH-)=1×106
C.AgCl在相同物质的量浓度的CaCl2和NaCl溶液中的溶解度相同
D.冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离度、pH均先增大后减小
参考答案:B
本题解析:
本题难度:一般
5、选择题 某温度下,Fe(OH)3(S)、Cu(OH)2(S)分别在溶液中达到沉淀溶解平衡后,改变溶液,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是
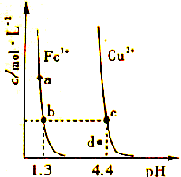
[? ]
A.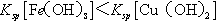
B.加适量固体可使溶液由点变到点
C.c、d两点代表的溶液中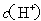 与
与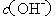 乘积相等
乘积相等
D.Fe(OH)3、Cu(OH)2分别在b、c两点代表的溶液中达到饱和
参考答案:B
本题解析:
本题难度:一般