| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点讲解《难溶电解质的溶解平衡》高频试题特训(2017年最新版)(三)
F. 移取25.00ml含SO2的水溶液于250ml锥形瓶中,用0.0100mol/L KMnO4标准溶液滴定至终点。按上述操作方法重复滴定2―3次。 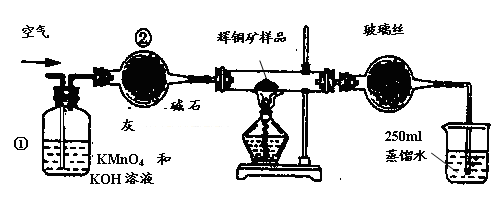 试回答下列问题: (1)装置①的作用是_________________;装置②的作用是____________________。 (2)假定辉铜矿中的硫全部转化为SO2,并且全部被水吸收,则操作F中所发生反应的化学方程式为?,当产生_______________________________的现象时可判断滴定已经达到终点。 (3)若操作F的滴定结果如下表所示,则辉铜矿样品中Cu2S的质量分数是_________。
(4)本方案设计中由一个明显的缺陷影响了测定结果(不属于操作失误),你认为是?(写一种既可)。 (5)已知在常温下FeS 的 Ksp= 6 . 25 × 10 -18, H2S 饱和溶液中 c (H+)与 c (S2-)之间存在如下关系: c2 (H+) ・c(S2-) =" 1" . 0×10-22。在该温度下,将适量 FeS 投入硫化氢饱和溶液中,欲使溶液中c(Fe2+)为 lmol/L,应调节溶液的c(H十)为__________。 5、选择题 已知,常温下,Ksp(AgCl)=1.8×10-10(mol/L)2,Ksp(AgI)=8.3×10-17(mol/L)2,下列叙述中,正确的是 | |||||||||||||||||||
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:高考化学知识点整理《有关氧化还.. | ||