| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ�㽲�⡶ˮ�ĵ���ƽ�⡷���߲��ԣ�2017�����°棩(��)
�ο��𰸣�B �������������ͬ��Ũ�ȣ���ĵ��볣��Խ��˵��������Խǿ������ɿ���֪��Ka(HCN)= 6.2��10-10 mol��L��1��Ka(HF)= 6.8��10-4 mol��L��1��Ka(CH3COOH)= 1.8��10-5 mol��L��1����Ka(HNO2)= 6.4��10-6mol��L��1��HF�ĵ��볣�����������������ǿ���������ε�ˮ��̶Ƚ�С����pH��С�����Ա���Ĵ�ΪB�� �����Ѷȣ�һ�� 2��ѡ���� �ڳ����£�pH = 9��NaOH��Һ��CH3COONa������Һ�У�������ˮ���������OH������Ũ�ȷֱ�Ϊa��b����a��b�Ĺ�ϵΪ |
�ο��𰸣�B
�������������������ǿ�����ˮ�ĵ��룬����ˮ���������OH������Ũ��Ϊ10��9mol/L����������ǿ�������Σ�ˮ��ٽ�ˮ�ĵ��룬����ˮ���������OH������Ũ��Ϊ10��5mol/L������a��b�Ĺ�ϵ��a=10-4b����ѡB��
���㣺��������ζ�ˮ�ĵ���ƽ��Ӱ����й��жϺͼ���
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣���������ǿ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ��������Ĺؼ�����ȷ������������Ӱ��ˮ�ĵ���ƽ��ģ�����������ѧ�������������������ѧ���Ĵ���������
�����Ѷȣ�һ��
3������� ��Ҫ��д�����з���ʽ��
NaHSO4���뷽��ʽ��______
NaHCO3���뷽��ʽ��______
HClO���뷽��ʽ��______
NH3?H2O���뷽��ʽ��______
Na2Sˮ�����ӷ���ʽ��______
AlCl3ˮ�����ӷ���ʽ��______��
�ο��𰸣�NaHSO4Ϊǿ����ʣ����뷽��ʽΪNaHSO4�TNa++H++SO42-��
NaHCO3Ϊǿ����ʣ����뷽��ʽΪNaHCO3�TNa++HCO3-��
HClOΪ������ʣ����뷽��ʽΪHClO?H++ClO-��
NH3?H2OΪ������ʣ����뷽��ʽΪNH3?H2O?NH4++OH-��
Na2Sˮ�����ӷ���ʽΪS2-+H2O?HS-+OH-��HS-+H2O?H2S+OH-��
AlCl3ˮ�����ӷ���ʽΪAl3++3H2O?Al��OH��3+3H+��
�ʴ�Ϊ��NaHSO4�TNa++H++SO42-��NaHCO3�TNa++HCO3-��HClO?H++ClO��NH3?H2O?NH4++OH-��S2-+H2O?HS-+OH-��HS-+H2O?H2S+OH-��Al3++3H2O?Al��OH��3+3H+��
���������
�����Ѷȣ�һ��
4��ѡ���� �����£�99mL0.1mol/L�������101mL0.05mol/L����������Һ��Ϻ���Һ��c(H+)Ϊ(�����ǻ��ʱ������仯)
A��0.5��(10-8+10-10)mol/L
B��(10-8+10-10)mol/L
C��(1��10-14-5��10-5)mol/L
D��1��10-11 mol/L
�ο��𰸣�D
���������������ͼ������֪�����������ǹ����ģ����Է�Ӧ��OH����Ũ��Ϊ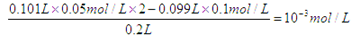 ������������Ũ����10��11mol/L��ѡD��
������������Ũ����10��11mol/L��ѡD��
���㣺�����������Һ��������Ũ�ȵļ��㡣
�����Ѷȣ�һ��
5��ѡ���� ���в����У���ʹ����ƽ��H2O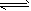 H++OH-�����ƶ�����Һ�����Ե���
H++OH-�����ƶ�����Һ�����Ե���
[? ]
A. ��ˮ�м���NaHSO4��Һ
B. ��ˮ�м���Al2(SO4)3����
C. ��ˮ�м���Na2CO3��Һ
D. ��ˮ���ȵ�100�棬ʹpH=6
�ο��𰸣�B
���������
�����Ѷȣ�һ��
|
||
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | ||
| ��һƪ���߿���ѧ֪ʶ���ܽᡶ��ѧʵ���.. | ||
| �����Ŀ |