微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 X、Y、V、W是常见的短周期元素,它们在周期表里的位置如下图所示.V、W的最简单的气态氢化物M、N混合时有白烟生成,M是碱性气体.请回答以下问题:
(1)W的原子结构示意图为______.
(2)常温常压下,将a?L?M气体和b?L?N气体通入水中,若所得溶液的pH=7,则a______b(填“>、=、<”)
(3)二氧化钛(TiO2)与X的单质、Y的单质在高温下反应,生成由两种元素组成的两种化合物,该反应的化学方程式为______.
(4)联氨(N2H4)也叫肼,是火箭的燃料写出肼的结构式______,用次氯酸钠溶液氧化M能得到肼的稀溶液,写出反应的离子方程式______.
(5)含X元素的一种化合物A与Y的最高价氧化物B之间有右图的转化关系,若D为白色沉淀,则如图转化的离子方程式为______.?
?
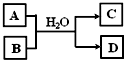
参考答案:V、W的最简单的气态氢化物M、N混合时有白烟生成,M是碱性气体,则M为NH3,N为HCl,所以V为N元素,W为Cl元素,根据四种元素在周期表中的位置可知,Y为C元素,X为Al元素,则
(1)W为Cl元素,原子序数为17,原子核外有3个电子层,最外层电子数为7,则原子结构示意图为
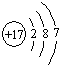
,
故答案为:
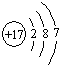
;
(2)M为NH3,N为HCl,如二者等物质的量混合物,则恰好反应生成NH4Cl,为强酸弱碱盐,溶液呈酸性,若所得溶液的pH=7,氨气应过量,故答案为:>;
(3)Y为C元素,X为Al元素,与二氧化钛(TiO2)在高温下反应生成的两种化合物为Al2O3和TiC,反应的化学方程式为3TiO2+4Al+3C??高温?.?2Al2O3+3TiC,
故答案为:3TiO2+4Al+3C??高温?.?2Al2O3+3TiC;
(4)联氨(N2H4)中N原子与其它三个原子成键,达到8电子稳定结构,结构式为
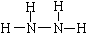
,次氯酸钠溶液氧化NH3能得到肼的离子方程式为ClO-+2NH3=N2H4+Cl-+H2O,
故答案为:
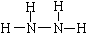
;ClO-+2NH3=N2H4+Cl-+H2O;
(5)含X元素的一种化合物A与Y的最高价氧化物B(CO2)之间发生反应,生成白色沉淀D为Al(OH)3,为AlO2-溶液与CO2的反应,反应的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-或2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-,
故答案为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-或2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-.
本题解析:
本题难度:一般
2、推断题 下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。 常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为金属单质。反应①②均为工业上 的重要反应。
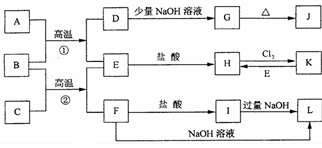
请回答下列问题:
(1)D的电子式为____。
(2)K的化学式为____。
(3)写出B与C高温反应生成E和F的化学方程式:___。
(4)写出D与J的稀溶液反应生成G的离子方程式___。
参考答案:(1) 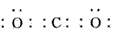
(2)FeCl3
(3)Fe2O3+2Al Al2O3+2Fe
Al2O3+2Fe
(4)CO2+CO32-+H2O==2HCO3-
本题解析:
本题难度:一般
3、简答题 X、Y、Z三种短周期元素,两两之间能组成5种化合物A、B、C、D、E;X、Y、Z三种元素可组成化合物F.已知:化合物A、B、C中原子个数比都为1:1;B为淡黄色固体,C、E常温下均为无色液体;A是化学式为XZ的离子化合物,A与E反应生成F和一种气体;D是化学式为X2Y的离子化合物,D的阴、阳离子具有相同的电子层结构且与E分子所含电子数相等.请回答下列问题:
(1)X元素的名称是______,它在周期表中的位置______.
(2)X、Y、Z的原子半径从大到小的顺序是(用元素符号表示)______
(3)写出F的电子式______
(4)已知X单质、A、B、D均为固体,分别与E反应都生成同一种物质,其中X单质、A、B分别与E的反应均是氧化还原反应.请写出X单质、B分别与E反应的化学方程式
______,______;
B中含有的化学键是______;
(5)请写出由化合物C制取Y的单质反应的化学方程式______.
参考答案:(1)B为淡黄色固体可推测为Na2O2,三种元素中有Na和O.C、E常温为液体,推测为H2O2和H2O,可知三种元素还包括H.A为XZ的离子化合物,可知A为NaH,X为Na,Y为O,Z为H.则A为NaH,B为Na2O2,C为H2O2,D为Na2O,E为H2O,F为NaOH.故X元素的名称是:钠.它在周期表中的位置:第三周期第IA族.故答案为:钠;第三周期第IA族;
(2)同周期从左到右半径逐渐减小,同主族从上到下逐渐增大,X、Y、Z的原子半径从大到小的顺序是(用元素符号表示):Na>O>H,故答案为:Na>O>H;
(3)F的化学式:NaOH.F的电子式:
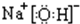
,故答案为:
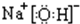
;
(4)X为Na,B为Na2O2,E为H2O,X单质、B分别与E反应的化学方程式:2Na+2H2O=4NaOH+H2↑、2Na2O2+2H2O=4NaOH+O2↑,B是过氧化钠,含有钠离子和过氧根离子.故含离子键,过氧根离子内两个氧原子间是非极性键,故答案为:2Na+2H2O=4NaOH+H2↑;2Na2O2+2H2O=4NaOH+O2↑;离子键和非极性键;
(5)C为H2O2,Y为O,反应的化学方程式:2H2O2?
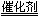
2H2O+O2↑,故答案为:2H2O2?
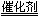
2H2O+O2↑.
本题解析:
本题难度:一般
4、简答题 (8分)近年来,某些轻元素的含氢化合物及其复合体系作为氢源受到广泛关注。化合物A(XYH2)和B(XH)都是具有潜在应用价值的释氢材料。A受热分解生成固体化合物C并放出刺激性气体D,D可使湿润的pH试纸变蓝。A和B混合可优化放氢性能。研究发现,该混合体系的放氢反应分三步进行:
2A =" C" + D?⑴
D + B =" A" + H2?⑵
C + B =" E" + H2?⑶
将A和B按1∶2的摩尔(物质的量)比混合,在催化剂作用下,所含的氢全部以氢气放出,失重10.4%。
A、C、E均能水解生成F和D。G是由X和Y组成的二元化合物,其阴离子是二氧化碳的等电子体,G分解生成E和一种无色无味的气体I。写出A、B、C、D、E、F、G和I的化学式。
参考答案:(8分)
A.LiNH2? B.LiH? C.Li2NH? D.NH3
E.Li3N? F.LiOH? G.LiN3? I.N2
本题解析:略
本题难度:一般
5、填空题 (12分)根据下列框图关系填空。已知反应①、③是工业生产中的重要反应,D、E常温下为气体、X常温下为五色液体,H与E相对分子质量之间的关系为:Mr(H)-Mr(E)=34,又知C的焰色反应呈黄色。
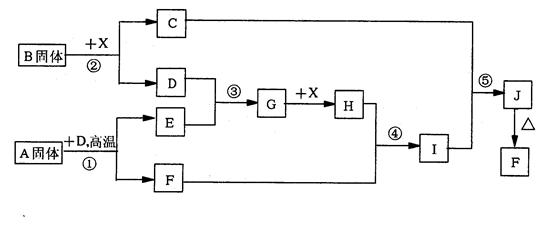
(1)化合物B中所包含的化学键有___________________
(2)反应④的离子方程式:________________________________
反应⑤的化学方程式:________________________________
(3)已知每生成16gE,放出106.5kJ热量,则反应①的热化学方程式为:
参考答案:______________________________________?(1)离子键、非极性键(或共价键)?
(2)Fe203+6H+=2Fe3++3H20,? Fe2(S04)3+6NaOH =2Fe(OH)3↓+3Na2S04
(3)FeS2(s)+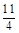 ?02=
?02=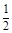 Fe2O3 (s) +2SO2(g);△H=-852kJ/mol
Fe2O3 (s) +2SO2(g);△H=-852kJ/mol
(未注明状态扣1分,写成FeS给2分)
本题解析:本题是无机框图题,根据是找准突破点。C的焰色反应呈黄色,说明含有钠元素。X是液体,所以X是水。反应①、③是工业生产中的重要反应,因此可能是工业制取硫酸的,即A是FeS2,D是氧气,F是氧化铁,E是SO2。所以B是过氧化钠,C是氢氧化钠,G是三氧化硫,H是硫酸,则I是硫酸铁,J是氢氧化铁。
本题难度:一般