��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1���ƶ��� A��B��C��D��E���ֻ����������ij�ֶ����ڳ���Ԫ�أ����ǵ�ת����ϵ��ͼ��ʾ������AΪ������Һ��CΪ���ܵİ�ɫ���壬E��������ˮ����ȡA��Һ���գ���ɫ��ӦΪdz��ɫ(����ɫ�ܲ���)��

(1)д����ѧʽ��A________��B________��C________��D________��E________��
(2)д�����з�Ӧ�����ӷ���ʽ��
A��B___________________�� A��D_______________________
�ο��𰸣�(1)KAlO2��Al(OH)3��Al2O3��AlCl3��NaAlO2
(2)AlO2-��CO2��2H2O===Al(OH)3����HCO3-��AlO2-��4H+===Al3+��2H2O
���������
�����Ѷȣ�һ��
2������� ��10�֣�ÿ��2�֣���֪Cr(OH)3�ڼ��Խ�ǿ����Һ�н�����[Cr(OH)4]�D�����Ļ������ж�������+6�۸���ǿ�����ԣ��䶾����+3�۸����Ե�100������ˣ�����Ժ����ķ�ˮ���д������ɲ����������ַ�����
��ԭ�������Խ�������FeSO4�Ƚ�+6�۸���ԭ��+3�۸���
�����������£�

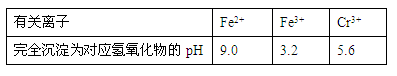
�й�������ȫ������pH���±���
��1��д��Cr2O72����FeSO4��Һ�����������·�Ӧ�����ӷ���ʽ________________________________________________________��
��2���ں�����ˮ�м���FeSO4���ٵ���pH��ʹFe3+��Cr3+�����������������
���ڲ������п����ڵ�����ҺpH���Լ�Ϊ��_____________������ţ���
A��Na2O2? B��Ca(OH)2? C��Ba(OH)2? D��NaOH
��ʱ������Һ��pH��Χ��____________������ţ���ѡ�
A��12��14? B��10��11? C��6��8? D��3��4
��3�����������4.0��10-3mol��L-1��AgNO3��4.0��10-3mol��L-1��K2CrO4��Һ���������Ag2CrO4������Ksp(Ag2CrO4)=9.0��10-12������д����ʾAg2CrO4�ܽ�ƽ��ķ���ʽ��2�֣�������Ҫд��������Ag2CrO4����ԭ��ļ�����̣�2�֣���
�ο��𰸣���ÿ��2�֣��ܼ�10�֣�
��1��Cr2O72�� + 6Fe2+ +14H+ ="=" 2Cr3+ + 6Fe3+ + 7H2O��
��2��B?C
��3��Ag2CrO4 (s)  ?2Ag+(aq) + CrO42��(aq)
?2Ag+(aq) + CrO42��(aq)

�������������1�������������л�ԭ�ԣ�Cr2O72-��ǿ�����ԣ������ܷ���������ԭ��Ӧ�����������ӱ����������������ӣ�Cr2O72-����ԭΪCr3+����Ӧ����ʽΪCr2O72-+6Fe2++14H+�T2 Cr3++6Fe3++7H2O��
�ʴ�Ϊ��Cr2O72-+6Fe2++14H+�T2 Cr3++6Fe3++7H2O��
��2��A��Na2O2��ǿ�����ԣ��ܰ�Cr3+������Cr6+���Ӷ��ò���Cr��OH��3���ʴ���
B��Ca��OH��2�� D��NaOHʹFe3+��Cr3+�������������������û�����������������ɣ�����ȷ��
C��Ba��OH��2������������ܲ������ᱵ�������������ʣ��ʴ���
�ں�����ˮ�м���FeSO4���ٵ���pH��ʹFe3+��Cr3+�������������������û������������������������Һ��PHӦ����5.6С��9������B��ȷ��
�ʴ�Ϊ��B��C��
���������⿼�������ӷ���ʽ����д���ѶȲ���ע�����е�ͼʾ�ͱ������ṩ����Ϣ����������������������Ϣ����Ĺؼ���
�����Ѷȣ���
3��ѡ���� X��Y��Z��W��Ϊ��ѧ��ѧ�ij������ʣ�һ������������֮������ͼת����ϵ�������������ԣ�������˵������ȷ���ǣ�������
A����W�ǵ���������Z��Һ������FeCl2��Һ
B����W���������ƣ���X��Z���ܷ�Ӧ����Y
C����X�ǽ���þ����W������ǿ�����Եĵ���
D����XΪ�״�����X��Z����Է��������������14
