微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、推断题 下图是元素周期表的一部分,A、B、C均为短周期元素,A、C两种元素的原子核外电子数之和等于B的质子数,B的原子核内质子数和中子数相等。回答
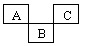
(1)写出元素符号:A__________;B__________;C___________。
(2)C的原子结构示意图:____________;B的最高价氧化物对应水化物的化学式为____________。
(3)A的氢化物的水溶液显____________(填“酸”或“碱”)性。
参考答案:(1)A:N;B:S;C:F
(2)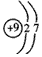 ; H2SO4
; H2SO4
(3)碱
本题解析:
本题难度:一般
2、简答题 A、B、C、D均为中学化学中常见的物质,它们之间转化关系如图1(部分产物已略去):

试回答:
(1)若D是具有氧化性的单质,则属于主族的金属A为______(填元素符号)
(2)若D是金属,C溶液在储存时应加入少量D,其理由是(用必要的文字和离子方程式表示)______;D在潮湿的空气中易发生吸氧腐蚀,写出腐蚀时原电池正极的电极反应式______.
(3)若A、B、C为含同一种金属元素的无机化合物,在溶液中A和C反应生成B.请写出B转化为C的所有可能的离子方程式______.化合物B经过一系列反应可以得到单质E,将一定质量的Mg和E的混合物投入500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图2所示.则固体混合物中Mg的质量为______;NaOH溶液的物质的量浓度为______.
参考答案:(1)若D是具有氧化性的单质,A为主族的金属,A为钠、D为氧气、B为氧化钠、C为过氧化钠,符合转化关系,
故答案为:Na;
(2)若D是金属,由转化关系可知,D为变价金属,A具有强氧化性,可推知A为氯气、D为Fe,、B为FeCl2、C为FeCl2,则:
FeCl2溶液在储存时应加入少量Fe,其理由是:加入少量铁,发生反应2Fe2++Fe=3Fe3+,防止Fe2+被氧化为Fe3+,
Fe在潮湿的空气中易发生吸氧腐蚀,原电池正极的电极反应式为:O2+2H2O+4e-=4OH-,
故答案为:加入少量铁,发生反应2Fe2++Fe=3Fe3+,防止Fe2+被氧化为Fe3+;O2+2H2O+4e-=4OH-;
(3)若A、B、C为含同一种金属元素的无机化合物,在溶液中A和C反应生成B,应含有Al元素,可推知A为偏铝酸盐、D为强酸、B为氢氧化铝、C为铝盐(或者A为铝盐、D为强碱、B为氢氧化铝、C为偏铝酸盐),则:
B转化为C的所有可能的离子方程式为:Al(OH)3+3H+=Al3++3H2O或Al(OH)3+OH-=AlO2-+2H2O;
化合物Al(OH)3经过一系列反应可以得到单质E为Al,将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体,待反应完全后,向所得溶液中加入NaOH溶液,
由图可知,200~240mL为氢氧化铝与氢氧化钠反应,可知n[Mg(OH)2]=0.15mol,根据Mg元素守恒可知:m(Mg)=0.15mol×24g/mol=3.6g,
沉淀最大时为氢氧化镁、氢氧化铝,故n[Al(OH)3]=0.35mol-0.15mol=0.2mol,根据电荷守恒可知,20~200mL消耗氢氧化钠的物质的量等金属提供电子物质的量,故n(NaOH)=0.15mol×2+0.2mol×3=0.9mol,则c(NaOH)=0.9mol0.2L-0.02L=5mol/L,
故答案为:Al(OH)3+3H+=Al3++3H2O或Al(OH)3+OH-=AlO2-+2H2O;3.6g;5mol/L.
本题解析:
本题难度:一般
3、推断题 由两种元素组成的化合物A存在如下图所示的转化关系(部分产物及反应条件已略去)。已知:E为红棕色气体,F、H为金属单质,J为黑色非金属单质。L露置于空气中时,由白色最终转化为红褐色,B与F反应时可生成C,也可生成G。试回答下列问题
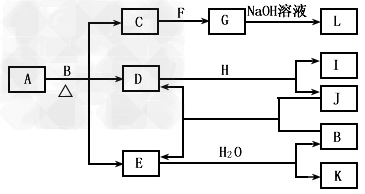
(1)物质K的名称是__________;I的晶体属于____________晶体;
(2)已知A中两种元素原子成最简整数比,且金属元素与非金属元素的质量比为14∶1,则A的化学式为____________。
(3)写出L露置于空气中时,由白色最终转化为红褐色的化学方程式:___________。
(4)写出G与B的稀溶液反应的离子方程式?__________________。
(5)写出A与B反应的化学方程式______________________,若各步反应都看成是进行完全的,则当生成a?mol物质L时,需要A?____________mol。
参考答案:(1)一氧化氮;离子
(2)Fe3C
(3)4Fe(OH )2+ O2 + 2H2O==4Fe(OH)3
(4)3Fe2++4H++NO3-==3Fe3++NO↑+2H2O
(5)Fe3C + 22HNO3==3Fe(NO3)3 + CO2↑+ 13NO2↑+ 11H2O;2a/9或(0.22a)
本题解析:
本题难度:一般
4、推断题 (14分)下图所示物质(部分产物和反应条件未标出)中,只有A是单质,常温下B和C呈气态,且B是导致酸雨的大气污染物,D是氧化物,W是淡黄色固体。
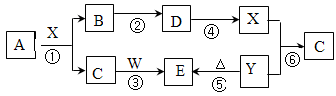
据此回答下列问题:
(1)B、C、D的化学式分别为:B?、C?、D?;从物质分类角度,上图所给物质中属于钠盐的是?(填写化学式)。
(2)上图所给物质在6个反应中只做还原剂的有?(填写化学式)。
(3)上图反应中不属于氧化还原反应的有?(填写序号)。
(4)写出A和X反应的化学方程式?;若生成的B在标准状况下的体积为22.4L,则参加反应的A的物质的量为?,反应中转移的电子数目为?。
(5)请写出C和W反应的化学方程式:?。
(6)请写出X和 Y反应的离子方程式:?。
参考答案:(1)SO2? CO2? SO3(各1分)? Na2CO3、NaHCO3 ?(全部选对得1分)
(2)C、SO2?(全部选对得1分)
(3)④ ⑤ ⑥(全部选对得1分)
(4)C+2H2SO4(浓) CO2↑+2SO2↑+2H2O(2分);0.5mol? 1.204×1024(各1分)
CO2↑+2SO2↑+2H2O(2分);0.5mol? 1.204×1024(各1分)
(5)2Na2O2+2CO2=2Na2CO3+O2(2分)
(6)H++HCO3-=CO2↑+H2O(2分)
本题解析:由题意“B是导致酸雨的大气污染物,D是氧化物,W是淡黄色固体”可推知B为二氧化硫,D为三氧化硫,X为硫酸,W为过氧化钠,再由“只有A是单质,常温下B和C呈气态,”可推知C为二氧化碳。则E为碳酸钠,Y为碳酸氢钠,A为碳。
(1)SO2? CO2? SO3? Na2CO3、NaHCO3 ?
(2)整个过程只有①②③属于氧化还原反应,①中C做还原剂,②中二氧化硫做还原剂,③中过氧化钠既做氧化剂又做还原剂。
(3)④ ⑤ ⑥属于非氧化还原反应。
(4)A和X反应为C与浓硫酸反应,方程式为:C+2H2SO4(浓) CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
根据方程式可知生成1mol二氧化硫需反应0.5molC,转移电子数为2mol即2NA。
(5)C和W反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2
(6)请写出X和 Y反应的离子方程式:H++HCO3-=CO2↑+H2O
点评:本题不难,根据题目的信息,结合所掌握的物质的特性,可推出相关物质。
本题难度:困难
5、选择题 已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X不可能是( )
| 选项 | W | X
A
盐酸
Na2CO3溶液
B
Cl2
Fe
C
CO2
Ca(OH)2溶液
D
NH3?H2O
AlCl3溶液
|
A.A
B.B
C.C
D.D