| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学必备知识点《热化学方程式》试题强化练习(2017年最新版)(二)
参考答案:D 本题解析:n(气体)= 5mol,由于n(CH4):n(H2)= 4:1,所以n(CH4)= 4mol; n(H2)= 1mol。(①+③×2)整理可得CH4(g)+2O2(g)→CO2(g)+2H2O(;) ΔH=- (Q1+2Q3)kJ/mol;由于含有4mol的甲烷,所以燃烧放出热量是0.4(Q1+2Q3)kJ;②+③×2整理可得2H2(g)+O2(g) == 2H2O(l) ΔH=- (Q2+2Q3)kJ/mol;由于含有1mol的氢气,所以燃烧放出热量是0.5(Q2+2Q3)kJ;因此体积比为4:1的甲烷和H2的混合气体112L(标准状况下),经完全燃烧后恢复到常温,则放出的热量为4(Q1+2Q3)kJ+0.5 (Q2+2Q3)kJ=4Q1+0.5Q2+9Q3 KJ。故选项是D。 本题难度:一般 2、选择题 已知下列反应的热化学方程式:6C(s)+5H2(g)+3N2(g)+9O2(g)===2C3H5(ONO2)3(l) ΔH1 |
参考答案:A
本题解析:已知:①6C(s)+5H2(g)+3N2(g)+9O2(g)
本题难度:一般
3、填空题 甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:
高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:
CH4(g)+CO2(g)=2CO(g)+2H2(g)ΔH=+260 kJ/mol
已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ/mol
则CH4与O2反应生成CO和H2的热化学方程式为 。
参考答案:2CH4(g)+O2(g)=2CO(g)+4H2(g)ΔH=-46 kJ/mol
本题解析:利用盖斯定律求未知反应的热化学方程式,将第1个反应×2+第2个反应得:
2CH4(g)+O2(g)=2CO(g)+4H2(g);ΔH=-46 kJ/mol
本题难度:一般
4、选择题 有三个热化学方程式:其中Q1、Q2、Q3的大小关系为( )
①2H2?(g)+O2?(g)=2H2O?(g)+Q1?kJ;
②2H2?(g)+O2?(g)=2H2O?(l)+Q2?kJ;
③H2?(g)+
| 1 2 |
参考答案:B
本题解析:
本题难度:一般
5、选择题 0. 096 kg碳完全燃烧可放出3 134.4 kJ热量,以下对此反应的热化学方程式中书写正确的是?
[? ]
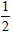 O2 (g)=CO( g) △H=-391.8kJ・mol-1
O2 (g)=CO( g) △H=-391.8kJ・mol-1 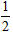 O2(g)=CO(g) △H=+391.8 kJ・mol-1
O2(g)=CO(g) △H=+391.8 kJ・mol-1参考答案:C
本题解析:
本题难度:一般
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:高考化学知识点总结《化学平衡》.. | ||