微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 过二硫酸钾(K2S2O8)是一种无色结晶,不溶于乙醇,有强氧化性,易分解。实验室制备过二硫酸钾可通过低温电解KHSO4认溶液得到。
实验步骤如下:
步骤1.称取40gKHSO4溶解90mL蒸馏水,倒入大试管,试管浸在冰水浴中(装置见图9),并冷却到5℃以下。
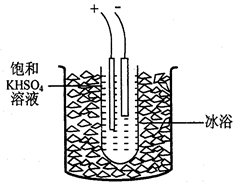
步骤2电解2h,每隔约半小时补一次冰
步骤3.将沉淀收集在漏斗中,直接用乙醇和乙醚洗涤和过滤
步骤4.干燥、称重
步骤5.回收乙醚和乙醇
(1)电解总反应的化学方程式为?。
(2)电解过程中,阳极产生微量且能使湿润的KI-淀粉变蓝的有色单质气体,该气体可能是(填化学式)。
(3)步骤2每隔半小时要向大烧杯添加冰块,其原因是?。
(4)步骤5回收乙醇、乙醚时采用的操作方法是?。
(5)取得到的样品0.2500g溶于30mL水,加4gKI,塞住瓶塞,振荡,静止15min,加入1mL冰醋酸,再用cmol・L- 1Na2S2O3溶液滴定。(S2O82- +3I- =2SO42- +I3-;I3- I2+I-;2S2O32-+I2=2I- + S4O62-)
I2+I-;2S2O32-+I2=2I- + S4O62-)
①溶解时,加入KI后需塞住瓶塞,其目的是?。
②本实验所用的指示剂为?。
③若本次滴定消耗Na2SO3溶液VmL,由本次结果计算,样品中K2S2O8的纯度为(用含c、V的代数式表示)。
(6)分析化学上检验Mn2+在Ag+催化下K2S2O8溶液将Mn2+氧化为紫色的MnO4-,该反应的离子方程式为 。
参考答案:
(1)2KHSO4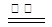 K2S2O8 + H2↑
K2S2O8 + H2↑
(2)O3
(3)降低水温,保证电解过程中温度在5℃以下
(4)蒸馏
(5)①防止I-被氧化,造成偏大的误差?②淀粉溶液③54cV%
(6)2Mn2++5S2O82- +8H2O 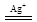 2MnO4- +10SO42- +16H+
2MnO4- +10SO42- +16H+
本题解析:(1)电解KHSO4溶液,SO42-失电子生成S2O82-,H+得电子生成H2。(2)阳极为阴离子放电,生成能氧化I-的气体,且为有色,则应为O3,可理解成OH-放电生成O2,O2在放电条件下进一步转化为O3。(3)由信息知,过二硫酸钾易分解,故需要在低温下生成。(4)乙醇和乙醚为相互溶解的有机物,可利用两者沸点不同而蒸馏分开。(5)I-易被氧化,如空气中的O2,故实验中需要封密。淀粉与I2显蓝色,该实验中当I2被消耗时,蓝色会褪去,从指示反应的终点。由方程式找出关系式:
K2S2O8~I3- ~I2~2S2O32-
270? 2
m(K2S2O8)? cV10-3
w(K2S2O8)= m(K2S2O8)/0.25 =54cv%。
(6)Mn由+2价升到+7价,S由+7降到+6,根据得失电子守恒配平反应,再由电荷守恒确定出产物中有H+,最后由H原子守恒,确定反应物中还有H2O,并配平。
本题难度:一般
2、实验题 某研究小组探究SO2和Fe(NO3)3溶液的反应。
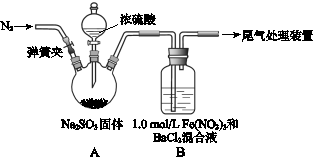
已知: 1.0 mol・L-1的Fe(NO3)3溶液的pH=1,请回答:
(1)装置A中反应的化学方程式是?。
(2)为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是?。
(3)装置B中产生了白色沉淀,其成分是?,说明SO2具有?性。
(4)分析B中产生白色沉淀的原因:
观点1:?_____________________________;
观点2:SO2与Fe3+反应;
观点3:在酸性条件下SO2与NO3-反应;
①若观点2正确,装置B中反应的离子方程式是?。
②只需将装置B中的 Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验,即可证明观点3是否正确,应选择的试剂是(填序号)?。
a.0.1 mol・L-1稀硝酸?
b.1.5 mol・L-1 Fe(NO3)2溶液
c.6.0 mol・L-1 NaNO3和0.2 mol/L盐酸等体积混合的溶液
参考答案:(12分)
(1)Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O(2分)
(2)打开弹簧夹,向装置中通入一段时间的N2,关闭弹簧夹(2分)
(3)BaSO4(1分)?还原性(1分)
(4)观点1:SO2和Fe3+、酸性条件下NO3-都反应(2分)
①SO2+2Fe3++Ba2++2H2O=BaSO4↓+2Fe2++4H+(2分;可分两步写,各1分)
②c(2分)
本题解析:(1)装置A中的反应是制取SO2,方程式为:Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O。
(2)反应前要充入N2,排除装置A中的空气,反应对实验的干扰。
(3)硝酸具有氧化性,白色沉淀为BaSO4,说明SO2具有还原性。
(4)经过分析,各个观点,得出观点1是SO2和Fe3+、酸性条件下NO3-都反应。
①Fe3+把SO2氧化,离子方程式是SO2+2Fe3++Ba2++2H2O=BaSO4↓+2Fe2++4H+。
②Fe(NO3)3中有Fe3+,a错;NO3-在酸性条件下有氧化性,b错。故选c。2制备 Fe3+、NO3-的氧化性
点评:本题考查的是SO2制备和Fe3+、NO3-的氧化性的相关知识,题目难度较大,要求学生熟悉所实验的内容及原理,能够考查同学们进行分析问题、解决问题的能力。
本题难度:一般
3、填空题 (1)用18mol・L-1的硫酸配制1.00 mol・ 的硫酸100mL。若实验仪器有:
的硫酸100mL。若实验仪器有:
A.100mL量筒、B.托盘天平、C.玻璃棒、D.50mL容器瓶、E. 10mL量筒、
F.胶头滴管、G. 50mL烧杯、H. 100mL容量瓶。
实验时应选用仪器是?(填 字母);
字母);
(2)在容量瓶的使用方法 中,下列操作不正确的是?(填字母);
中,下列操作不正确的是?(填字母);
A.使 用容量瓶前检查其是否漏水。
用容量瓶前检查其是否漏水。
B.容量瓶用蒸馏水洗净后,再用待配溶液洗涤。
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近刻度线1―2cm处,用胶头滴管滴加蒸馏水到刻度线。
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近刻度线1―2cm处,用胶头滴管滴加蒸馏水到刻度线。
E.盖好瓶盖,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动多次
(3)浓H2SO4稀释时应该?
?;
(4)若实验遇到下列情况,对硫酸溶液的物质的量浓度有何影响?(填“偏高”、“偏低”或“不变”)
①稀释硫酸后的烧杯未洗涤:?;
②未经冷却趁热将溶液注入容量瓶中:?;
③摇匀后发现液面低于刻度线再加水:?;
④容量瓶中原有少量蒸馏水:?。
参考答案:实验时应选用仪器是? CEFGH?(填字母);
(2)? BCD?;
(3)浓H2SO4稀释时应该是浓硫酸沿着烧杯内壁倒入盛有水量水的烧杯中? ?
?
并用玻璃棒搅拌
(4)① 偏低?;
②?偏高;
③?偏低?;
④:?不变?。
本题解析:略
本题难度:简单
4、实验题 (15分)利用有机反应R-H+Cl2 R-Cl(液)+HCl(气)制取副产品盐酸的设想己成为现实。请根据所给模拟装置图回答下列问题:
R-Cl(液)+HCl(气)制取副产品盐酸的设想己成为现实。请根据所给模拟装置图回答下列问题:
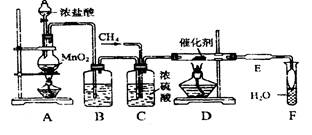
(1)装置B中盛放的溶液是?
其作用是?。
(2)写出C装置的三种功能:
①?;
②?;
③?;
(3)玻璃管D中所放石棉碎块的作用是??
玻璃管E中所放碘化钾的作用是?
(4)F中导管末端做成“膨大”形的作用是?
(5)①点燃A处酒精灯,②点燃D处酒精灯,③通入CH4,这三种操作的先后顺序是
__________? ___(依次填代号)
参考答案:
(1)饱和氯化钠溶液;除去Cl2中混有HCl(各2分,共4分)
(2)除去水蒸气(干燥Cl2和CH4);使Cl2和CH4充分混合;观察气体流速控制 气体流量。(使Cl2和CH4按一定配比混合)(各1分共3分)
(3)增大接触面积使Cl2充分反应;除去Cl2 (各2分共4分)
(4)防倒吸 (2分)
(5)③②①(2分)
本题解析:略
本题难度:简单
5、选择题 下列实验能成功的是 ?( ? )
A.将乙酸和乙醇混合加热制乙酸乙酯
B.用CuSO4溶液和过量NaOH溶液混合,然后加入几滴乙醛,加热
C.CH3CH2Br中滴加AgNO3溶液观察是否有浅黄色沉淀,判断卤代烃的类型
D.苯和浓溴水反应制溴苯
参考答案:B
本题解析:A中还缺少浓硫酸和加热条件;C中溴乙烷不能电离出银离子,和硝酸银不反应;D中应该是液溴且还需要催化剂,所以正确的答案选B。
点评:该题是中等难度的试题,也是高考中的常见题型,试题难易适中,注重基础和能力的双向考查。有利于培养学生严谨、规范的实验设计和逻辑推理能力。
本题难度:简单