��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��֪25�桢101kPaʱ��һЩ���ʵ�ȼ����Ϊ��
| ��ѧʽ | CO��g�� | H2��g�� | CH3OH��l��
��H/��kJ?mol-1��
-283.0
-285.8
-726.5
|
��ش��������⣺
��1��д����������CH3OH��l����ȫȼ�յ��Ȼ�ѧ����ʽ��______��
��2�����ݸ�˹������ɷ�Ӧ���Ȼ�ѧ����ʽ��CO��g��+2H2��g���TCH3OH��l����H=______��
�ο��𰸣���1��ȼ���ȵĸ����25�桢101kPaʱ��1mol��ȼ����ȫȼ�������ȶ���������ʱ�ų�����������ʱSӦת��ΪSO2��CӦת��Ϊ������̼��HӦת��ΪҺ̬ˮ��
�ʡ�H�T-726.5kJ?mol-1ָ����1molCH3OH��l����ȫȼ�����ɶ�����̼��Һ̬ˮʱ�ķ�Ӧ�ȣ�
��CH3OH��l����ȫȼ�յ��Ȼ�ѧ����ʽ��CH3OH��l��+32O2��g���TCO2��g��+2H2O��l����H=-726.5KJ?mol-1
�ʴ�Ϊ��CH3OH��l��+32O2��g���TCO2��g��+2H2O��l����H=-726.5KJ?mol-1
��2��COȼ�յ��Ȼ�ѧ����ʽ��CO��g��+12O2��g���TCO2��g����H=-283.0kJ?mol-1 ��
H2ȼ�յ��Ȼ�ѧ����ʽ��2H2��g��+O2��g���T2H2O��l����H=-285.8��2 kJ?mol-1 ��
CH3OHȼ�յ��Ȼ�ѧ����ʽ��CH3OH��l��+32O2��g���TCO2��g��+2H2O��l����H=-726.5 kJ?mol-1 ��
����+��+��-�ۣ��ɵã�CO��g��+2H2��g���TCH3OH��l����H=-128.1KJ?mol-1
�ʴ�Ϊ��-128.1KJ?mol-1
���������
�����Ѷȣ�һ��
2������� ��1������ʯ[��Ҫ�ɷ�Ca5��PO4��3F]�ڸ������Ʊ����ף�P4�����Ȼ�ѧ����ʽΪ��4Ca5��PO4��3F��s����21SiO2��s����30C��s��=3P4��g����20CaSiO3��s����30CO��g����SiF4��g������H
��������Ӧ�У����������������________��
����֪��ͬ�����£�
4Ca5��PO4��3F��s����3SiO2��s��=6Ca3��PO4��2��s����2CaSiO3��s����SiF4��g������H1
2Ca3��PO4��2��s����10C��s��=P4��g����6CaO��s����10CO��g������H2
SiO2��s����CaO��s��=CaSiO3��s������H3
�æ�H1����H2�ͦ�H3��ʾ��H����H��____________��
��2�������գ���H2O2��H2SO4�Ļ����Һ���ܳ�ӡˢ��·�������ĩ�е�ͭ����֪��
��Cu��s����2H����aq��=Cu2����aq����H2��g����H1����64.39 kJ��mol��1
��2H2O2��l��=2H2O��l����O2��g����H2����196.46 kJ��mol��1
��H2��g����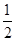 O2��g��=H2O��l����H3����285.84 kJ��mol��1
O2��g��=H2O��l����H3����285.84 kJ��mol��1
��H2SO4��Һ�У�Cu��H2O2��Ӧ����Cu2����H2O���Ȼ�ѧ����ʽΪ_________________________________________________________________��
�ο��𰸣���1�����Ʋ������ڦ�H1��3��H2��18��H3
��2��Cu��s����H2O2��l����2H����aq��=Cu2����aq����2H2O��l������H����319.68 kJ��mol��1
�����������1����CaSiO3Ϊ�����ijɷ�֮һ���Ӷ�ȷ��������;���ڸ��ݸ�˹����֪��H����H1��3��H2��18��H3��
��2�����Ȼ�ѧ����ʽ�٣�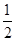 ���ڣ��۵ã�
���ڣ��۵ã�
Cu��s����2H����aq����H2O2��l��=Cu2����aq����2H2O��l��
��H����H1��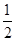 ����H2����H3����64.39 kJ��mol��1��
����H2����H3����64.39 kJ��mol��1��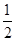 ������196.46 kJ��mol��1��������285.84 kJ��mol��1������319.68 kJ��mol��1��
������196.46 kJ��mol��1��������285.84 kJ��mol��1������319.68 kJ��mol��1��
�����Ѷȣ�һ��
3��ѡ���� �����Ȼ�ѧ����ʽ��д��ȷ���ǣ� ? ��
A��2SO2+O2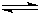 2SO3����H=-196.6kJ/mol
2SO3����H=-196.6kJ/mol
B��N2��g��+2O2��g���T2NO2��g������H=+67.7kJ/mol
C��C��s��+O2��g���TCO2��g������H=+393.5kJ/mol
D��H2O��l���TH2��g����+ O2��g��������H=+285.8kJ
O2��g��������H=+285.8kJ
�ο��𰸣�B
���������
�����Ѷȣ���
4��ѡ���� ��֪��25�棬101kPa�£�1g����C8H18ȼ�����ɶ�����̼��Һ̬ˮʱ�ų�48��40kJ��������ʾ������Ӧ���Ȼ�ѧ����ʽ��ȷ����
[? ]
A��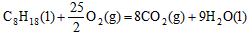 ����H����5518kJ/mol
����H����5518kJ/mol
B��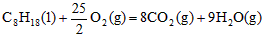 ����H����48��40kJ/mol
����H����48��40kJ/mol
C��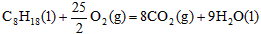 ����H��+5518kJ/mol
����H��+5518kJ/mol
D��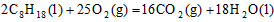 ����H��+11036kJ/mol
����H��+11036kJ/mol
�ο��𰸣�A
���������
�����Ѷȣ���
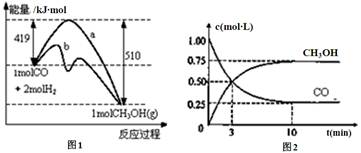
5������� ��ҵ����CO����ȼ�ϼ״���һ���¶Ⱥ��ݻ������·�����Ӧ��CO(g)+2H2(g) CH3OH(g)��ͼ1��ʾ��Ӧ�е������仯��ͼ2��ʾһ���¶��£������Ϊ1L���ܱ������м���2mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯��
CH3OH(g)��ͼ1��ʾ��Ӧ�е������仯��ͼ2��ʾһ���¶��£������Ϊ1L���ܱ������м���2mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯��
��ش��������⣺
��1���ڡ�ͼ1���У����� (�a����b��)��ʾʹ���˴�����û��ʹ�ô���ʱ���ڸ��¶Ⱥ�ѹǿ�����·�ӦCO(g)+2H2(g) CH3OH(g)�ġ�H= ��
CH3OH(g)�ġ�H= ��
��2������˵����ȷ����
A����ʼ�����CO�����ʵ���Ϊ1mol
B������CO��Ũ�ȣ�H2��ת���ʻ�����
C��������ѹǿ�㶨ʱ����Ӧ�ﵽƽ��״̬
��3���ӷ�Ӧ��ʼ������ƽ�⣬v(CO)= ���ﵽƽ��ʱ��c(H2)= �����¶���CO(g)+2H2(g)  CH3OH(g)�Ļ�ѧƽ�ⳣ��Ϊ ���ﵽƽ��������������������䣬���������ѹ��Ϊ0.5L����ƽ�� �ƶ� (�������������)��
CH3OH(g)�Ļ�ѧƽ�ⳣ��Ϊ ���ﵽƽ��������������������䣬���������ѹ��Ϊ0.5L����ƽ�� �ƶ� (�������������)��
��4����֪CH3OH(g)��3/2O2(g)��CO2(g)��2H2O(g)����H����193kJ/mol
��֪H2O(l)= H2O(g)����H����44 kJ/mol����д��32g��CH3OH(g)��ȫȼ������Һ̬ˮ���Ȼ�ѧ����ʽ ��
�ο��𰸣���1��b -91kJ/mol ��2��ABC��3��0.075mol/(L��min) 0.5mo/L 12 ����4��CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ��H=-281kJ/mol(3��)
�����������1������ͼ���֪��b���������ϵͣ���bΪ�������������ͼ���֪��H=419kJ/mol-510kJ/mol=-91kJ/mol����2������ͼ��2��֪����ʼ�Ǽ���CO��Ũ��Ϊ1mol/L��10min��ﵽƽ�⣬ƽ��ʱCO��ת����Ϊ��1mol/L-0.25mol/L��/1mol/L��100%=75%������CH3OH��Ũ��Ϊ0.75mol/L��Aѡ����ȷ��Bѡ�������������ԭ����֪������CO��Ũ�ȣ�H2��ת���ʽ�����Cѡ����ڷ�Ӧ�ﻯѧ������֮�Ͳ����ڲ��������֮�Ϳ�֪����������ѹǿ�㶨ʱ����Ӧ�ﵽƽ��״̬����ѡ��A��B��C����3��v(CO)=��1mol/L-0.25mol/L��/10min=0.075mol/(L��min)������CO(g)+2H2(g) CH3OH(g)��֪������n(CO):n(H2)=1:2��������H2�����ʵ���Ϊ0.75mol��2=1.5mol���ﵽƽ��ʱʣ��H2�����ʵ���Ϊ2mol-1.5mol=0.5mol����Ũ��Ϊ 0.5mo/L�����¶��»�ѧƽ�ⳣ��Ϊ0.75/0.52��0.25=12����Ӧ�ﻯѧ������֮�ʹ��ڲ��������֮�ͣ�ѹ�������ƽ��������Ӧ�����ƶ�����4��32gCH3OHΪ1mol��������H2OΪ2mol����H2O(l)= H2O(g)����H����44 kJ/mol�����Ȼ�ѧ����ʽΪ��CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ��H=-281kJ/mol��
CH3OH(g)��֪������n(CO):n(H2)=1:2��������H2�����ʵ���Ϊ0.75mol��2=1.5mol���ﵽƽ��ʱʣ��H2�����ʵ���Ϊ2mol-1.5mol=0.5mol����Ũ��Ϊ 0.5mo/L�����¶��»�ѧƽ�ⳣ��Ϊ0.75/0.52��0.25=12����Ӧ�ﻯѧ������֮�ʹ��ڲ��������֮�ͣ�ѹ�������ƽ��������Ӧ�����ƶ�����4��32gCH3OHΪ1mol��������H2OΪ2mol����H2O(l)= H2O(g)����H����44 kJ/mol�����Ȼ�ѧ����ʽΪ��CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ��H=-281kJ/mol��
���㣺��ѧƽ��ͼ���Ȼ�ѧ����ʽ��д����ѧƽ�ⳣ�����顣
�����Ѷȣ�����