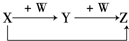|
高考化学知识点归纳《无机综合与推断》高频试题预测(2017年最新版)(六)
2017-03-02 23:50:51
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 X、Y、Z、W有如图所示的转化关系,则X、W可能是①C、O2 ②AlCl3、NaOH ③Fe、HNO3 ④S、O2( )
A.①②③
B.①②
C.③④
D.①②③④
| 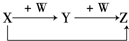
参考答案:A
本题解析:
本题难度:一般
2、推断题 甲、乙、丙、丁是原子序数不超过20的元素组成的物质(单质或化合物),且存在如下转化关系,甲+乙→丙+丁
回答下列问题:
(1)转化关系中所涉及的反应为非氧化还原反应,且乙为水时:
①丙为可燃性气体,分子的空间构型为直线形结构。写出实验室制备丙的化学方程式______________。

②若甲是由N和Cl元素组成的化合物,其分子结构模型如上图所示,丙具有漂白性。则甲中Cl元素的化合价是___________。
(2)转化关系中所涉及的反应为氧化还原反应,且乙为水时:
①若甲可用于防毒面具、潜艇等常用的供氧剂,写出发生反应的化学方程式是___________________
②若丙和丁都是可燃性气体,其中丙是丁业炼铁过程中的还原剂。写出甲+乙→丙+丁的化学方程式是
___________________
③若甲是由N和O元素组成的气态物质,呈红棕色。将3.36g Fe加到一定量丙溶液中,收集到1.12 L气体丁(已折算为标准状况),则反应的离子方程式是________________________ 。(用一个离子方程式表示)
参考答案:(1)①CaC2+2H2O→Ca(OH)2+HC CH↑;②+1 CH↑;②+1
(2)①2Na2O2+2H2O=4NaOH+O2↑;②C+H2O CO+H2;③6Fe+5NO3-+2OH-=3Fe3++3Fe2++5NO↑+10H2O CO+H2;③6Fe+5NO3-+2OH-=3Fe3++3Fe2++5NO↑+10H2O
本题解析:
本题难度:一般
3、填空题 C、D、G、I均为短周期元素形成的单质,D、G、I为常见非金属气态单质。D元素的原子的最外层电子数是次外层电子数的3倍,C、G同周期,且原子最外层电子数相差4,它们的简单离子电子层结构不同。相互间有如下转化关系:
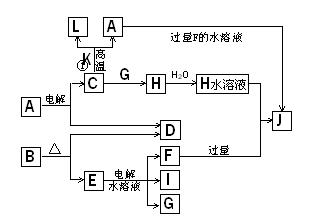
请填空:
(1)? D与I能形成 原子个数比为1:1的共价化合物,请写出其分子式:?; 原子个数比为1:1的共价化合物,请写出其分子式:?;
(2)L是目前应用最广泛的金属,用碳棒作阳极,L作阴极,写出电解E水溶液的化学式:?。
(3)化合物K 中含有组成单质L的元素,且该元素的质量分数为70%。反应①的化学方程式是?,引发该反应的操作是?
(4)写出A+F → J的离子方程式:?。
参考答案:(1)H2O2(2分)
(2) 2KCl+2H2O 2KOH+ H 2KOH+ H 2↑+Cl2↑ (3分) 2↑+Cl2↑ (3分)
(3) Fe2O3 +2Al 2Fe + Al2O3(3分) 2Fe + Al2O3(3分)
在混合物上加少量KClO3,插上Mg条并将其点燃(3分)
(4)Al2O3+2OH-===2AlO2-+H2O (3分)
本题解析:略
本题难度:一般
4、填空题 A~G各物质间的关系如下图,其中B、D为气态单质。

请回答下列问题:(①中MnO2作催化剂,②中MnO2作氧化剂)
(1)物质C和E的名称分别为________________、__________________;
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式为_____________;若只能在加热情况下进行,则反应物A应为_____________;
(3)反应②的化学方程式:_______________________________________;
(4)新配制的F溶液应加入_____________以防止其转化为G。检验G溶液中阳离子的常用试剂是_____________,实验现象为____________________________。
参考答案:(1)浓盐酸、四氧化三铁;(2)2H2O2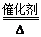 2H2O + O2↑ ; KClO3 2H2O + O2↑ ; KClO3
(3)MnO2 + 4HCl(浓) MnCl2 + Cl2↑+ 2H2O?(4) 铁粉 , KSCN溶液?溶液变为血红色 MnCl2 + Cl2↑+ 2H2O?(4) 铁粉 , KSCN溶液?溶液变为血红色
本题解析:①中MnO2作催化剂可知:A为H2O2或KClO3;B为O2;E为Fe3O4 , ②中MnO2作氧化剂可与C制气体D且C还与Fe3O4反应生成F和G的混合溶液。可确定:C为浓盐酸;D为Cl2;而G为FeCl3、F为FeCl2。(1)物质C和E的名称分别为浓盐酸、四氧化三铁。(2)进行反应①,若能在常温下进行,A是H2O2其化学方程式为2H2O2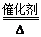 2H2O + O2↑;若只能在加热情况下进行,则反应物A应为KClO3。(3)反应②的化学方程式: MnO2 + 4HCl(浓) 2H2O + O2↑;若只能在加热情况下进行,则反应物A应为KClO3。(3)反应②的化学方程式: MnO2 + 4HCl(浓) MnCl2 + Cl2↑+ 2H2O.(4)Fe2+有强的还原性,容易被被空气氧化成Fe3+而变质。因此常加入铁粉将变质的Fe3+还原回Fe2+.反应的离子方程式为:2Fe3++Fe=3Fe2+.Fe3+的检验方法是向待测溶液中加入KSCN溶液,若溶液变为血红色,就证明含有Fe3+.或加入NaOH溶液,若产生红褐色的沉淀。就证明含有Fe3+.2 、Cl2的实验室制法Fe3+的检验等知识。 MnCl2 + Cl2↑+ 2H2O.(4)Fe2+有强的还原性,容易被被空气氧化成Fe3+而变质。因此常加入铁粉将变质的Fe3+还原回Fe2+.反应的离子方程式为:2Fe3++Fe=3Fe2+.Fe3+的检验方法是向待测溶液中加入KSCN溶液,若溶液变为血红色,就证明含有Fe3+.或加入NaOH溶液,若产生红褐色的沉淀。就证明含有Fe3+.2 、Cl2的实验室制法Fe3+的检验等知识。
本题难度:一般
5、实验题 A.B.C.D.E为含同一种元素的常见物质。C物质只由一种元素组成,在1个C分子中形成共价键的电子数与分子中所含电子数之比为3∶7。C和E均可与氧气在一定条件下反应生成A。请回答以下问题:?
(1)常温下将气体B通入水中发生反应,生成A和D,则该反应的离子方程式?。
(2)写出E与氧气反应生成A的化学方程式?。
(3)D和E生成的化合物在某温度下加热分解,同时生成两种氧化物。且在此过程中,若有0.5 mol该化合物完全反应,转移电子数为2 mol。写出该反应的化学方程式?。
(4)下图所示是进行木炭与D浓溶液反应,并检验生成的气体和反应的热效应的实验装置,它具有无污染.现象明显等特点。具支试管A中所盛固体下层是无水CaCl2(作载体不参加反应),上层是红热的木炭。实验时慢慢将D浓溶液滴到木炭上,反应即开始进行且能长时间剧烈反应。①写出木炭与D浓溶液反应的化学方程式?。

②该反应为?(填“吸热”或“放热”)反应。
③试管B内出现的现象为?。
④在实验临近结束时,发现滴管中的D浓溶液难以滴下。若想再滴入几滴D浓溶液使木炭反应完全,最简单的办法是?。
参考答案:(1)3NO2+H2O=2H++2NO-3+NO?(2)4NH3+5O2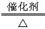 4NO+6H2O 4NO+6H2O
(3)NH4NO3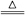 2H2O+N2O↑? 2H2O+N2O↑?
(4)①C+4HNO3(浓) 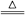 CO2↑+4NO2↑+2H2O CO2↑+4NO2↑+2H2O
②放热? ③试管内有红棕色气体生成,石灰水变浑浊
④摇动试管B,使上部的气体溶于石灰水
本题解析:略
本题难度:简单
|