微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 阿伏加德罗常数约为6.02×1023mol-1,下列叙述中正确的是
A.1molO2参加反应,一定得4×6.02×1023个电子
B.7.5g?SiO2晶体中含有硅氧键数为0.5×6.02×1023
C.2.24L?CH4中含有的原子数为0.5×6.02×1023
D.250mL?2mol/L的氨水中含有NH3?H2O的分子数为0.5×6.02×1023
参考答案:B
本题解析:分析:A.有氧气参加的反应,不一定得4×6.02×1023个电子;
B.7.5g二氧化硅的物质的量=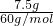 =0.125mol,一个硅原子含有4个硅氧键;
=0.125mol,一个硅原子含有4个硅氧键;
C.气体摩尔体积与温度和压强有关,标况下,气体摩尔体积是22.4L/mol;
D.一水合氨是弱电解质,在水溶液里存在部分电离.
解答:A.O2+2Na Na2O2,该反应中1molO2参加反应,得2×6.02×1023个电子,故A错误;
Na2O2,该反应中1molO2参加反应,得2×6.02×1023个电子,故A错误;
B.7.5g二氧化硅的物质的量=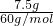 =0.125mol,一个硅原子含有4个硅氧键,所以7.5g?SiO2晶体中含有硅氧键数为0.125mol×4×6.02×1023/mol=0.5×6.02×1023,故B正确;
=0.125mol,一个硅原子含有4个硅氧键,所以7.5g?SiO2晶体中含有硅氧键数为0.125mol×4×6.02×1023/mol=0.5×6.02×1023,故B正确;
C.温度和压强未知导致气体摩尔体积未知,所以无法计算甲烷的物质的量,从而无法得出甲烷中原子个数,故C错误;
D.一水合氨是弱电解质,在水溶液里存在部分电离,所以250mL?2mol/L的氨水中含有NH3?H2O的分子数小于0.5×6.02×1023,故D错误;
故选B.
点评:本题以阿伏伽德罗常数为载体考查氧化还原反应、未知结构、弱电解质等知识点,易错点是B,明确二氧化硅结构特点是解B选项关键,为易错点.
本题难度:简单
2、选择题 下列溶液氯离子的物质的量浓度与200mL?1mol?L-1AlCl3溶液中氯离子的物质的量浓度相等的是
A.150mL?3?mol?L-1氯酸钠溶液
B.75mL?3mol?L-1氯化钙溶液
C.150mL?3?mol?L-1氯化钾溶液
D.100mL?3mol?L-1氯化镁溶液
参考答案:C
本题解析:分析:根据溶液中氯离子的物质的量浓度=盐的浓度×化学式中氯离子个数,据此分析解答;
解答:50mL?1mol?L-1的AlCl3溶液中Cl-物质的量浓度是3mol/L,
A、150mL?3?mol?L-1氯酸钠溶液中c(ClO3-)=3mol?L-1×1=2mol/L;
B、75mL?3mol?L-1氯化钙溶液中c(Cl-)=3mol?L-1×2=6mol/L;
C、150mL?3?mol?L-1氯化钾溶液中c(Cl-)=3?mol?L-1×1=3mol/L;
D、100mL?3mol?L-1氯化镁溶液中c(Cl-)=3mol?L-1×2=6mol/L;
故选:C;
点评:本题考查了溶液中氯离子物质的量浓度的计算,难度不大,溶液中氯离子的物质的量浓度为盐的浓度与化学式中离子个数的积.
本题难度:困难
3、选择题 下列说法正确的是
A.NaOH的摩尔质量为40?g
B.1?mol?02 的质量与它的相对分子质量相等
C.1?mol?OH-的质量为17 g?mol-1?
D.氖气的摩尔质量(单位g?mol-1)在数值上等于它的相对原子质量
参考答案:D
本题解析:分析:A、摩尔质量是单位物质的量的 物质的质量;单位是g/mol;
B、1 mol 02 的质量与它的相对分子质量数值上相等;
C、质量单位是g;
D、氖气是单原子分子,它的摩尔质量在数值上等于它的相对原子质量.
解答:A、NaOH的摩尔质量为40 g/mol,故A错误;
B、1 mol 02 的质量数值上与它的相对分子质量相等,故B错误;
C、1 mol OH-的质量为17 g,故C错误;
D、氖气是单原子分子,氖气的摩尔质量(单位g?mol-1)在数值上等于它的相对原子质量,故D正确;
故选 www.91exAm.orgD.
点评:本题考查了摩尔质量的概念和计算应用,理解概念的实质和数值确定,单位判断是解题关键,题目较简单.
本题难度:一般
4、选择题 下列溶液中与100mL0.1mol/L(NH4)2SO4溶液中NH4+离子浓度相同的是
A.10mL1mol/L(NH4)2SO4溶液
B.50mL0.2mol/LNH4Cl溶液
C.10mL0.2mol/L(NH4)2SO4溶液
D.200mL0.1mol/LNH4NO3溶液
参考答案:B
本题解析:分析:根据物质的化学式及物质的物质的量浓度来计算NH4+的物质的量浓度,并注意离子的浓度取决于物质的物质的量浓度,而与体积无关系.
解答:100mL0.1mol/L(NH4)2SO4溶液中NH4+离子浓度为c(NH4+)=0.2mol/L.
A、10mL1mol/L(NH4)2SO4溶液,c(NH4+)=2c[(NH4)2SO4)]=2mol?L-1;
B、50mL0.2mol/LNH4Cl溶液,c(NH4+)=c(NH4Cl)=0.2mol?L-1;
C、10mL0.2mol/L(NH4)2SO4溶液,c(NH4+)=2c[(NH4)2SO4)]=0.4mol?L-1;
D、200mL0.1mol/LNH4NO3溶液,c(NH4+)=c(NH4NO3)=0.1mol?L-1;
故选:B.
点评:本题考查一定物质的量浓度溶液中所含微粒的物质的量浓度,所含微粒的物质的量浓度与所取溶液的体积大小无关.
本题难度:困难
5、选择题 下列各物质中所含氢原子个数与3.2gO2分子数相同的物质是
A.0.2gNH3
B.6.02×1023个H2SO4分子
C.0.1molHCl分子
D.标准状况下1.12LCH4
参考答案:C
本题解析:分析:利用n= 来计算氧气的物质的量,再利用n=
来计算氧气的物质的量,再利用n= 、n=
、n= 、n=
、n= 及物质的构成来计算氢原子的物质的量,若氢原子的物质的量与氧气的物质的量相等,则个数相同.
及物质的构成来计算氢原子的物质的量,若氢原子的物质的量与氧气的物质的量相等,则个数相同.
解答:3.2gO2的物质的量为 =0.1mol,
=0.1mol,
A、氨气的物质的量为 =0.012mol,氢原子的物质的量为0.012mol×3=0.036mol,故A错误;
=0.012mol,氢原子的物质的量为0.012mol×3=0.036mol,故A错误;
B、H2SO4分子的物质的量为 =1mol,氢原子的物质的量为1mol×2=2mol,故B错误;
=1mol,氢原子的物质的量为1mol×2=2mol,故B错误;
C、0.1molHCl分子中氢原子的物质的量为0.1mol×1=0.1mol,故C正确;
D、标准状况下甲烷的物质的量为 =0.5mol,氢原子的物质的量为0.5mol×4=2mol,故D错误;
=0.5mol,氢原子的物质的量为0.5mol×4=2mol,故D错误;
故选C.
点评:本题考查学生利用n= 、n=
、n= 、n=
、n= 及物质的构成进行的简单计算,明确氢原子的个数与氧分子数相同,即选项中氢原子的物质的量与氧气的物质的量相等是解答本题的关键.
及物质的构成进行的简单计算,明确氢原子的个数与氧分子数相同,即选项中氢原子的物质的量与氧气的物质的量相等是解答本题的关键.
本题难度:困难