微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。某工程师为了从废液中回收铜,重新获得FeCl3溶液,设计了下列实验步骤:
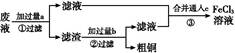
写出一个能证明还原性Fe比Cu强的离子方程式:?。
该反应在上图步骤?中发生。请根据上述反应设计一个原电池,在方框中画出简易装置图(标出电极名称、电极材料、电解质溶液)。
上述过程回收的铜是粗铜,为了获得更纯的铜必须进行电解精炼。写出电解精炼时阳极材料及主要的电极反应式?。
参考答案:Fe+Cu2+=Fe2++Cu ①
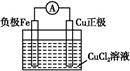
粗铜,Cu-2e-=Cu2+
本题解析:根据题干信息可知废液应为FeCl3、CuCl2、FeCl2的混合溶液,加入的试剂a为Fe,发生反应为:Fe+2Fe3+=3Fe2+、Fe+Cu2+=Cu+Fe2+,经①过滤后,滤渣是Fe与Cu的混合物,再加入过量的b(盐酸)发生反应:Fe+2HCl=FeCl2+H2↑,经②过滤后滤液主要是FeCl2溶液,将合并后的溶液中通入c(Cl2),发生主要反应为:2Fe2++Cl2=2Fe3++2Cl-。Fe+Cu2+=Fe2++Cu可以证明Fe比Cu还原性强,该反应在步骤①中发生。将Fe+Cu2+=Fe2++Cu设计成原电池,Fe作负极,比Fe不活泼的Cu作正极即可,电解质溶液是含Cu2+的溶液。电解精炼铜时,粗铜作阳极,精铜作阴极。
本题难度:一般
2、选择题 自然界中存在一种尖晶石,化学式为MgAl2O4,它晶莹剔透,非常美观,可以作为宝石。已知该尖晶石中混有一定量的Fe2O3。取该矿石粉末样品11.36 g,恰好能与200 mL一定浓度的盐酸反应,则该盐酸的浓度可能是( )
A.2.00 mol・L-1
B.2.80 mol・L-1
C.3.30 mol・L-1
D.3.50 mol・L-1
参考答案:B
本题解析:略
本题难度:简单
3、填空题 (1)在Fe(OH)3胶体中逐滴加入HI稀溶液,会出现一系列变化:
①先出现红褐色沉淀,原因是:_______________;
②随后沉淀溶解,溶液呈黄色,写出此过程反应的离子方程式:_______________;
③最后溶液颜色加深,原因是:_______________,此过程的离子方程式是:_______________;
④如用稀盐酸代替HI稀溶液,能出现上述哪些相同的实验现象:_______________(写序号)。
(2)2.00gC2H2气体完全燃烧生成液态水和CO2气体,放出99.6kJ的热量,写出该反应燃烧的热化学反应方程式___________________________;
参考答案:(1)①:加入电解质,使胶体凝聚;②:Fe(OH)3+3H+=Fe2++3H2O;③:有I2生成;
2Fe3++2I-=2Fe2++I2;④:①②
(2)C2H2(g)+5/2O2(g)→2CO2(g)+H2O(l);△H=-1294.8kJ/mol
本题解析:
本题难度:一般
4、选择题 在自然界中以游离态存在的金属是
[? ]
A.铁
B.金
C.钠
D.铝
参考答案:B
本题解析:
本题难度:简单
5、选择题 下列关于金属的叙述中正确的是
A.所有的金属都是固态的
B.金属具有导电性、导热性和延展性
C.金属原子只有还原性,其阳离子只有氧化性
D.金属元素在自然界中都是以化合态存在的
参考答案:B
本题解析:考查金属的性质
A:汞在常温下为液态
B:正确
C:金属阳离子也可呈现还原性,例如亚铁离子
D:非常不活泼的金属,例如金就可以以游离态的单质状态存在
故答案为B
本题难度:简单