微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法不正确的是( )
A.充电电池充电时,发生电解池反应;放电时,发生原电池反应
B.电镀时,应将镀层金属与电源正极相连
C.电解饱和NaCl溶液时,阳极上放出黄绿色气体的同时还产生大量的氢氧化钠
D.利用电化学原理保护金属主要有两种方法,分别是牺牲阳极的阴极保护法和外加电流的阴极保护法
参考答案:C
本题解析:电解饱和NaCl溶液时,阳极产生氯气,阴极产生氢气和NaOH,所以C错误,其余选项均正确。
点评:电解中最关键的是准确判断出电极上离子的放电顺序。在判断电解产物时,首先判断阳极电极材料。如果是活性电极,则电极本身失去电子。如果是惰性电极,则溶液中的阴离子失去电子。而阴极是溶液中的阳离子得到电子,所以需要熟练记住常见离子的放电顺序。
本题难度:一般
2、选择题 下列各个装置中能组成原电池的是
[? ]
A.
B.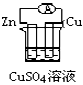
C.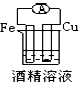
D.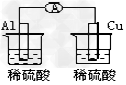
参考答案:B
本题解析:
本题难度:简单
3、填空题 (8分)
如图所示,是原电池的装置图( 为电流表)。请回答:
为电流表)。请回答:
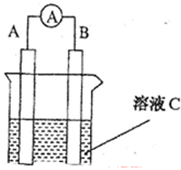
(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且做负极,则A电极上发生的电极反应式为 ;反应进行一段时间后溶液C的pH将 (填“升高”“降低”或“基本不变”)。
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如上图所示的原电池装置,则A(负极)极材料为 ,B(正极)极材料为 ,溶液C为 。
(3)若C为NaOH溶液,A电极材料为Al,B电极材料为Mg,负极上发生的电极反式为 。
参考答案:(1)2H++2e-==H2↑;升高
(2)Cu 石墨(合理即可) FeCl3溶液;
(3)Al-3e-+4OH-=AlO-2+2H2O.
本题解析:(1)铁作负极,则该原电池反应是铁与稀硫酸置换氢气的反应,所以正极反应是氢离子得电子生成氢气,电极反应式为2H++2e-==H2↑;溶液中氢离子放电,导致溶液中氢离子浓度减小,pH升高;
(2)Cu+2Fe3+=Cu2++2Fe2+设计成如上图所示的原电池装置,根据方程式中物质发生的反应类型判断,Cu发生氧化反应,作原电池的负极,所以A材料是Cu,B极材料是比Cu不活泼的导电物质如石墨、Ag等即可。溶液C中含有Fe3+,如FeCl3溶液;
(3)若C为NaOH溶液,A电极材料为Al,B电极材料为Mg,则Al与氢氧化钠溶液反应,则Al作负极,电极反应式为Al-3e-+4OH-=AlO-2+2H2O.
考点:考查对原电池反应原理的应用,电极的判断,电解质溶液的选择,电极反应式的书写
本题难度:困难
4、选择题 关于如图所示①、②两个装置的评价正确的是

选择
| 叙 述
| 评价
|
A
| 装置名称:①电解池,②原电池
| 错误
|
B
| 硫酸浓度变化:①增大,②减小
| 错误
|
C
| 电极反应式:①阳极:4OH--4e-====2H2O+O2↑
②正极:Zn-2e-====Zn2+
| 正确
|
D
| 离子移动方向:①H+向阴极移动 ②H+向正极移动
| 正确
|
?
参考答案:D
本题解析:A、装置①外加了电源,为电解池,装置②形成Zn、Cu原电池,叙述正确;B、电解稀硫酸实质是电解水,所以装置①中硫酸浓度增大,装置②的总反应为:Zn+H2SO4=ZnSO4+H2↑,硫酸浓度减小,叙述正确;C、电解硫酸溶液的阳极为OH?失电子:4OH--4e-=2H2O+O2↑,原电池的正极为H+得电子:2H++2e?=H2↑,叙述错误;D、电解池电解质溶液中阳离子向阴极移动,原电池电解质溶液中阳离子向正极移动,正确。
本题难度:一般
5、选择题 家庭生活中所用的铁锅,在下列哪种情况下最容易生锈
A.用水洗涤后烘干
B.用水洗涤后未擦干
C.炒过菜未洗涤
D.加满水的
参考答案:B
本题解析:
本题难度:一般