| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点归纳《盐类水解的原理》高频试题预测(2017年最新版)(二)
参考答案:D 本题解析:根据NH4+ +H2O 本题难度:一般 2、选择题 下列各式中属于正确的水解反应的是( ? ) 参考答案:B 本题解析: 本题难度:一般 3、选择题 等体积、等物质的量浓度的NaCl和NaF溶液中,阴阳离子总数相比 ( ) |
参考答案:B
本题解析:
正确答案:B
NaF是强碱弱酸盐,F++H2O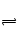 HF+OH
HF+OH
本题难度:一般
4、填空题 某盐或“类盐”的化学式为XmYn最简结构,将一定量的该盐溶于足量的水时:
(1)若m≠n,测得溶液的pH为5,则该盐与水反应的离子方程式可能为__________________。
(2)若m≠n,测得该盐溶液的pH为9,则该盐与水反应的离子方程式可能为__________________。
(3)若m≠n,X、Y为同周期的短周期元素,XmYn溶于水时,既有白色沉淀,又有无色气体放出,则溶于水的化学方程式为__________________。
(4)若m≠n,X、Y为不同周期的短周期元素,XmYn溶于水时,既有白色沉淀,又有无色气体放出,则溶于水的化学程式为。__________________。
(5)若X、Y为同主族元素,且m=n,则该物质溶于水的化学方程式为__________________。溶于水后溶液呈碱性,如__________________;溶于水后溶液呈酸性,如__________________。
参考答案:
(1)Xn++nH2O X(OH)n+nH+
X(OH)n+nH+
(2)Ym-+H2O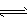 HY(m-1)-+OH-
HY(m-1)-+OH-
(3)Al2S3+6H2O=2Al(OH)3↓+3H2S↑
(4)Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑ ,Al4C3+12H2O=4Al(OH)3↓+3CH4↑
(5)NaH+H2O=NaOH+H2↑,KH+H2O=KOH+H2↑,BrCl+H2O=HBrO+HCl,
IBr+H2O=HIO+HBr ;NaH、KH;BrCl、IBr
本题解析:
本题难度:一般
5、选择题 将0.1mol下列物质置于1L水中,充分搅拌后,溶液中阴离子数最多的是:( )
A.KCl
B.Mg(OH)2
C.Na2CO3
D.MgSO4
参考答案:C
本题解析:氢氧化镁难溶于水,阴离子数量最少。由于碳酸钠溶于水发生水解反应,方程式为CO32-+H2O HCO3-+OH-,根据方程式可知,消耗1mol阴离子,产生2mol阴离子,所以C中最多。答案选C。
HCO3-+OH-,根据方程式可知,消耗1mol阴离子,产生2mol阴离子,所以C中最多。答案选C。
考点:盐类的水解
点评:本题主要考查盐类水解的应用,但需要注意的就是如果固体难溶,则其离子在水溶液中一定最少。
本题难度:简单
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:高考化学知识点归纳《工业生产其.. | ||