微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 实验室制备下列气体时,只能用排水法收集的是( )
A.H2
B.SO2
C.NO2
D.NO
参考答案:A.氢气和水不反应,所以可以用排水法收集,在常温下和氧气不反应,密度比空气小,所以也可以用向下排空气法收集,故A错误;
B.SO2能和水反应,所以不能用排水法收集,和氧气不反应,密度比空气大,可以用向上排空气法收集,故B错误;
C.二氧化氮能和水反应生成硝酸和一氧化氮,所以不能用排水法收集,二氧化氮和氧气不反应,密度比空气大,可以用向上排空气法收集,故C错误;
D.NO和氧气反应,所以不能用排空气法收集,和水不反应且难溶于水,所以只能用排水法收集,故D正确;
故选D.
本题解析:
本题难度:简单
2、实验题 (14分)某学校探究性学习小组对消毒液次氯酸钠(NaClO)的制备与性质等进行了探究。
甲同学:为制备消毒液,探究并制作了一种家用环保型消毒液(NaClO溶液)发生器,设计了如图所示的装置,用石墨作电极电解饱和氯化钠溶液。
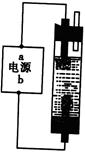
请完成下列问题:若通电时,为使生成的Cl2被完全吸收,制得有较强杀菌能力的消毒液,则电源的a电极名称为?极(填“正”、“负”、“阴”或“阳”);装置溶液中反应生成NaClO的离子方程式为:?。
乙同学:从某超市中查询到某品牌消毒液包装说明的部分内容,摘录如下:
主要有效成份为次氯酸钠,有效氯含量8000-10000mg/L。可用于各类家居用品、餐具、棉织衣物等的消毒,对彩色织物可能有褪色作用。切勿用于丝绸、毛、尼龙、皮革、油漆表面,勿用于铝、铜、碳钢制品。本品须密封,置阴凉暗处保存。
请完成以下实验探究过程:
I.阅读材料,根据学过的知识判断问题?
(1)室温条件下,该消毒液(NaClO)的不显中性的原因是(用离子方程式表示)
_____________________。
(2)该消毒液还具有的化学性质是_________(填序号)。
A.强氧化性? B.强还原性? C.不稳定性? D.漂白性? E.弱酸性
(3)从该消毒液的保存要求分析,导致其失效的主要原因是(用化学方程式表示)
_?。
II.确定要研究的问题
该消毒液对碳钢制品的腐蚀原理。
III.设计方案,实施探究
(1)用烧杯取少量样品,将一颗光亮的普通碳钢钉放入烧杯,浸泡一段时间。
预期的实验现象是_________________________________。
(2)为了进一步探究铁钉在该漂白剂(NaClO)溶液中的腐蚀原理,丁同学设计了如下图实验装置,写出碳(C)极上发生的电极反应式:?。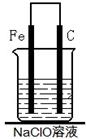
参考答案:甲:负(1分)Cl2+2OH-===Cl-+ClO-+H2O(2分)
乙:I.(1)ClO-+H2O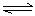 HClO+OH- (2分)
HClO+OH- (2分)
(2)A、D(2分)2NaClO+CO2+H2O=Na2CO3+2HClO(2分)? 2HClO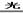 2HCl+O2↑(2分)
2HCl+O2↑(2分)
III.(1)钢钉表面有红褐色物质生成(2分)
(2)ClO-+2e-+H2O=Cl-+2OH-(2分)
本题解析:电解NaCl溶液生成氢氧化钠、氢气和氯气,氯气与氢氧化钠反应生成次氯酸钠,次氯酸钠因为水解显碱性。次氯酸钠具有强氧化性和漂白性。如果接触到空气中CO2,就会生成HClO,HClO分解就会使消毒液失效。将碳钢铁钉浸在次氯酸钠中,会发生电化学腐蚀。其中铁为负极,碳为正极。铁失电子,因为次氯酸根离子的强氧化性,次氯酸根离子得电子生成Cl―。
本题难度:简单
3、实验题 (10)按要求完成硝酸钾晶体的制备实验:
步骤
| 操作
| 具体操作步骤
| 现象解释结论等
|
?
①
| 溶解
| 取20克NaNO3和17克KCl溶解在35ml水中,加热至沸,并不断搅拌。
| 固体溶解
|
②
| 蒸发
| 继续加热搅拌,使溶液蒸发浓缩。
| 有?a?晶体析出。
|
③
| 热过滤
| 当溶液体积减少到约原来的一半时,迅速趁热过滤
| 滤液中的最主要成分为?b?。
|
④
| 冷却
| 将滤液冷却至室温。
| 有晶体析出。
|
 ⑤ ⑤
| ?
| 按有关要求进行操作
| 得到初产品硝酸钾晶体
|
⑥
| ?
| 将得到的初产品硝酸钾晶体溶于适量的水中,加热、搅拌,待全部溶解后停止加热,使溶液冷却至室温后抽滤。
| ?
得到纯度较高的硝酸钾晶体
|
⑦
| ?
检验
| 分别取⑤、⑥得到的产品,配置成溶液后分别加入1滴1mol/l的HNO3和2滴0.1mol/l的AgNO3
| 可观察到⑤、⑥产品中出现的现象分别是⑤产品中产生白色沉淀,⑥产品中无明显现象。
|
(1)把上述各步骤中的内容补充完整:a: b: ?
(2)写出步骤③趁热过滤的目的?,步骤⑥的操作名称?,步骤⑦中产生白色沉淀的离子方程式?
(3)步骤⑥的抽滤装置如图所示,仪器A的名称?,该装置中的错误之处是?;抽滤完毕或中途需停抽滤时,应先?,然后?。
参考答案:(1)NaCl;? KNO3
(2)防止因温度降低而析出硝酸钾晶体;重结晶;Ag++ Cl-= AgCl↓
(3)?布氏漏斗;布氏漏斗的颈口斜面未朝向抽滤瓶的支管口;断开连接安全瓶与抽气装置间的橡皮管;关闭抽气装置的水龙头
本题解析:(1)氯化钠的溶解度小,蒸发浓缩首先写出氯化钠,即a是氯化钠。硝酸钾的溶解度受温度影响大,所以降低温度时氯化钠析出,则b是硝酸钾。
(2)步骤③趁热过滤的目的防止因温度降低而析出硝酸钾晶体。为了得到纯净的硝酸钾晶体,需要重结晶。氯离子能和银离子反应生成氯化银沉淀,方程式为Ag++ Cl-= AgCl↓。
(3)根据仪器结构特点可知,A是布氏漏斗,抽滤时布氏漏斗的颈口斜面未朝向抽滤瓶的支管口,所以该处是错误的。抽滤完毕或中途需停抽滤时,应先断开连接安全瓶与抽气装置间的橡皮管,然后再关闭抽气装置的水龙头。
本题难度:一般
4、选择题 实验室干燥二氧化碳时应选用的干燥剂是
A.生石灰
B.NaOH固体
C.浓H2SO4
D.稀H2SO4
参考答案:C
本题解析:考点定位分析:本题的考点是根据浓硫酸或烧碱的性质确定所能干燥的气体,二氧化碳的化学性质。根据浓硫酸或烧碱的性质确定所能干燥的气体,就是指在利用浓硫酸或烧碱的吸水性来干燥气体时,还要注意被干燥的气体不能够与浓硫酸或烧碱发生反应,才能用浓硫酸或烧碱来干燥,否则,该气体就不能用它浓硫酸或烧碱来干燥。
解答过程分析:选择干燥剂时要求干燥剂不能和被干燥的物质反应,二氧化碳属于酸性氧化物,能和碱反应。
A、生石灰是氧化钙,与水反应生成氢氧化钙后能吸收二氧化碳,不能选用,此项错误;
B、氢氧化钠固体属于碱,能和二氧化碳反应生成碳酸钠和水,故不能选用,此项错误;
C、浓硫酸不和二氧化碳反应,可选用浓硫酸干燥二氧化碳气体,此项正确;
D、稀硫酸没有吸水性,不能干燥二氧化碳,此项错误。故选C
试题总结评价:呈碱性的干燥剂不能干燥酸性气体和酸性氧化物气体,酸性干燥剂不能干燥呈碱性的气体。
本题难度:简单
5、选择题 下列实验操作中正确的是
A.制取溴苯:将铁屑、溴水、苯混合加热
B.实验室制取硝基苯:先加入浓硫酸,再加苯,最后滴入浓硝酸
C.鉴别甲苯和苯:向甲苯和苯中分别滴入酸性KMnO4溶液,振荡,观察是否褪色
D.检验卤代烃中的卤原子:加入NaOH溶液共热,再加AgNO3溶液,观察沉淀的颜色
参考答案:C
本题解析:A不正确,应该用液溴;B不正确,应该是先加入浓硝酸,再加入浓硫酸,最后加入苯;D不正确,加入硝酸银溶液之前,应该先加入硝酸酸化,答案选C。
点评:该题是中等难度的试题,也是高考中的常见题型。化学实验常用仪器的使用方法和化学实验基本操作是进行化学实验的基础,对化学实验的考查离不开化学实验的基本操作,该类试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。
本题难度:简单