��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ����ά�Ƽ�������140�������ʷ��Ϊ��ʱ������������ã����й��ĺ����Ƽȡ��������ά������������������ʾ��
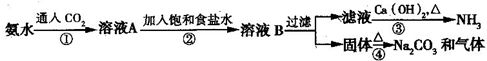
����ά����ʵ��������������ʳ�ε�������ֻ��70%���Ҹ���ƷCaCl2û�к��ʵ���;������Ⱦ������
1940���ҹ���ѧ�Һ�°���������������飬�ֲ�������ά���ļ���ȱ�ݣ����ԸĽ���ʳ�������ʸߴ�96%���õ��˴�����Ȼ�����ֲ�Ʒ������Ϊ�������Ƽ�����˷����Ļ���ԭ�����£�
����30��50��ı���ʳ��ˮ�У���ͨ�백�������ͣ���ͨ��CO2���Ӷ��õ�̼�����Ƴ�����
�ڹ��ˣ����������ȶ��ò�Ʒ��
������Һ�м���ϸʳ��ĩ�������¶�Ϊ10��15�棬ʹNH4Cl���������ˣ�����ΪNH4Cl��Ʒ����ҺΪ����ʳ��ˮ��
��ش��������⣺
��1��д�������ı���NaCl��Һ��ͨ��CO2 ʱ������Ӧ��������ѧ����ʽ��______��
��2��������NaCl��Һ��ͨ��CO2 ��NaHCO3��ԭ����______��Ҳ���ܲ�������NaCl��Һ��ͨ��CO2����ͨ��NH3�ķ�����NaHC03 ��ԭ����______��
��3��д��������ά�����������У�����CaCl2 �Ļ�ѧ��Ӧ����ʽΪ______��
��4���ں����Ƽ�У�______�����������ƣ�����ѭ�����ã�
��5�������Ƽ������ά����ȣ����ŵ���______����дһ�����ɣ���
�ο��𰸣���1���ڱ���NaCl��Һ��ͨ�����������Ժ���ͨ��CO2ʱ���������·�Ӧ��NH3+CO2+H2O=NH4HCO3��NH4HCO3+NaCl=NH4Cl+NaHCO3��������NaHCO3�ܽ����С������NaHCO3�ľ���������
�ʴ�Ϊ��NH3+CO2+H2O=NH4HCO3��NH4HCO3+NaCl=NH4Cl+NaHCO3����
��2��H2CO3���Ա���������CO2��NaCl����Ӧ��������NaCl��Һ��ͨ��CO2 ��NaHCO3��
��CO2��NaCl��Һ���ܽ�Ƚ�С������NaHCO3̫�ٲ���ᾧ����������Ҳ���ܲ�������NaCl��Һ��ͨ��CO2����ͨ��NH3�ķ�����NaHC03 ��
�ʴ�Ϊ��H2CO3���Ա���������CO2��NaCl����Ӧ��CO2��NaCl��Һ���ܽ�Ƚ�С������NaHCO3̫�ٲ���ᾧ������
��3��������ά�����������У��������ƺ���η�Ӧ���ɰ�����ͬʱ�����Ȼ��ƣ���Ӧ�ķ���ʽΪ2NH4Cl+Ca��OH��2=CaCl2+2NH3��+2H2O��
�ʴ�Ϊ��2NH4Cl+Ca��OH��2=CaCl2+2NH3��+2H2O��
��4�����������ȿ����ɶ�����̼�����˺�õ���ҺΪ����ʳ��ˮ������ѭ�����ã�
�ʴ�Ϊ��������̼�ͱ���ʳ��ˮ��
��5������ά��ȱ�㣺����CaCl2��;����NaCl������ֻ��70%��Լ��30%��NaCl����ĸҺ�У�
�����Ƽ���ŵ㣺�Ѻϳɰ��ʹ������ֲ�Ʒ���������������ʳ�������ʣ��������������̣������˶Ի�������Ⱦ�������˴���ijɱ��������˰�����ŵ㣬����������ȱ�㣬ʹʳ�ε���������ߵ�96%��NH4Cl�������ʣ�����ϳɰ������ϣ�ʹ�ϳɰ���ԭ����COת����CO2���������õ��Ȼ������ɣ�
�ʴ�Ϊ��ʹNH4Cl�������������ʣ��������õ�CaCl2���ɣ�ԭ��NaCl������ã�
���������
�����Ѷȣ�һ��
2������� ʵ�����Ʊ��������Ҫ�����ǣ��ٽ����ƺõı���NaCl��Һ�����ձ��м��ȣ�������
����30--35�棬�����·���������ϸ��NH4HC03���壬�ڼ�����Ϻ�������30���ӣ��۾��á����˵�NaHC03���壮������������ˮϴ�ӳ�ȥ���ʣ���ɺ�ת���������У����գ��Ƶ�Na2C03���壮
�������ڲ����¶��µ��ܽ�ȣ�g/l00gˮ����

| 0�� | 10�� | 20�� | 30�� | 40�� | 50�� | 60�� | 100��
NaCl
35.7
35.8
36.0
36.3
36.6
37.0
37.3
39.8
NH4HCO3
11.9
15.8
21.0
27.0
-��
NaHCO3
6.9
8.1
9.6
11.1
12.7
14.5
16.4
NH4Cl
29.4
33.3
37.2
41.4
45.8
50.4
55.3
77.3
|
�٣�35��NH4HC03���зֽ�
��ش�
��1����Ӧ�¶ȿ�����30-35�棬����Ϊ______��Ϊ���ƴ��¶ȷ�Χ����ȡ�ļ��ȷ���Ϊ______��
��2��������Ϻ�������30���ӣ�Ŀ����______�����ú�ֻ����NaHCO3Ʒ���ԭ����______��
��3��ϴ��NaHC03����IJ�����______��
��4���������õ�ĸҺ�к��е�����______���Ի�ѧʽ��ʾ����
��5��д����ʵ�����Ʊ�������йػ�ѧ����ʽ______��
��6�����Դ����Ʒ��NaHC03�����ķ����ǣ�ȷ��ȡ������ƷW?g��������ƿ�м�����ˮ�ܽ⣬��1-2�η�ָ̪ʾ���������ʵ���Ũ��Ϊc?��mol/L����HCl��Һ�ζ�����Һ�ɺ�ɫ����ɫ������HCl��Һ���ΪV1?mL���ټ�1-2�μ���ָʾ����������HCl��Һ�ζ�����Һ�ɻƱ�ȣ�����HC1��Һ�����ΪV2mL��д��������Ʒ��NaHCO3���������ļ���ʽ��______��
�ο��𰸣���1��̼�����10��20��ʱ�����ֽ⣬30��ʱ��ʼ�����ֽ⣮���¶ȹ��ͣ���Ӧ���ʽ������ʷ�Ӧ�¶ȿ�����30-35��֮��Ϊ�ˣ�ˮԡ�����ǰ�Ҫ���ȵ����ʷ���ˮ�У�ͨ����ˮ���ȴﵽ�����ʼ��ȵ�Ч����һ�㶼�ǰ�Ҫ��Ӧ�����ʷ����Թ��У��ٰ��Թܷ���װ��ˮ���ձ��У������ձ��в�һ���¶ȼƣ����Կ��Ʒ�Ӧ�¶ȣ�ˮԡ���ȵ��ŵ��DZ�����ֱ�Ӽ�����ɵĹ��Ⱦ������¶ȵIJ��ɿ��ԣ�����ƽ�ȵؼ��ȣ����෴Ӧ��Ҫ�ϸ���¶ȿ��ƣ�����Ҫˮԡ���ȣ�ˮԡ���ȵ�ȱ���Ǽ����¶����ֻ�ܴﵽ100�ȣ�
�ʴ�Ϊ��NH4HCO3�ֽ⣻��Ӧ���ʽ��ͣ�ˮԡ���ȣ�
��2��������Ϻ�������30���ӣ�����ʹ��Ӧ��ֽ��У�ʹ��Ӧ��ȫ��̼�����0��ʱ�ܽ��Ϊ11.3%��20��ʱΪ21%��40��ʱΪ35%��̼������0���ܽ��Ϊ6.9 g��5��Ϊ7.45 g��
10��Ϊ8.15 g��15��Ϊ8.85?g��20��Ϊ9.6 g��25��Ϊ10.35 g��30��Ϊ11.1g��35��Ϊ11.9 g��40��Ϊ12.7 g��45��Ϊ13.55 g��50��Ϊ14.45 g��55��Ϊ15.4g��60��Ϊ16.4g��30��ʱ̼�����Ƶ��ܽ�ȸ�С����̼���������������ʴ�Ϊ��ʹ��Ӧ��ֽ��У�NaHCO3���ܽ����С��
��3��������ˮϴ��NaHCO3�����Ŀ����Ϊ�˳�ȥ���ʣ��˷�Ӧ������Ϊ NaCl��NH4Cl��NH4HCO3��ϴ��NaHC03����IJ����ǣ�������ˮ���Ų�����ע�뵽������������û���������ô�����ˮ�˳����ظ�����2-3�Σ�
�ʴ�Ϊ��������ˮ���Ų�����ע�뵽������������û���������ô�����ˮ�˳����ظ�����2-3�Σ�
��4�����˳�ȥ������̼�����ƣ���Һ�л��в���̼������δ�����������ܽ�����Һ�е�NaCl��NH4Cl��NH4HCO3�����õ�ĸҺ��Ҫ�ɷ�ΪNaHCO3��NaCl��NH4Cl��NH4HCO3��
�ʴ�Ϊ��NaHCO3��NaCl��NH4Cl��NH4HCO3��
��5���ӷ�ָ̪ʾ������ɫ��ΧΪ8-10�������ʵ���Ũ��Ϊc��mol/L����HCl��Һ�ζ�����Һ�ɺ�ɫ����ɫ��ָʾCO32-+H+=HCO3-��Ӧ���յ㣬����HCl��Һ���ΪV1mL���ټӼ���ָʾ����������HCl��Һ�ζ�����Һ�ɻƱ�ȣ�ָʾHCO3-+H+=CO2��+H2O��Ӧ���յ㣬����HCl��Һ���ΪV2?mL���������������ӷ���ʽΪ��CO32-+H+=HCO3-��HCO3-+H+=CO2+H2O������Ʒ�к��е�̼�����Ʒ�Ӧ�����������Ϊ��V2-V1 ��mL��������������ʵ���Ϊc��V2-V1 ����1000 mol����̼�����Ƶ����ʵ���Ϊc��V2-V1����1000 mol��̼�����Ƶ�����Ϊc��V2-V1 ��M��1000 g��̼�����Ƶ���������Ϊc(v2-v1)M1000w��100%=c(v2-v1)1061000w��100%
�ʴ�Ϊ��c(v2-v1)1061000w��100%
���������
�����Ѷȣ�һ��
3������� ̼��������ֽ����������֯���Ƹ����ҵ����Ҫԭ�ϡ���ҵ̼����(����Լ98%)�к���Ca2+��Mg2+��Fe3+ ��Cl-��SO42-�����ʣ��ᴿ����·�����£�
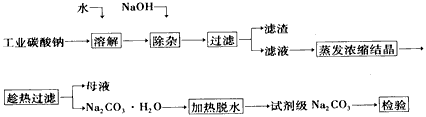
��֪̼���Ƶ��ܽ��(S)���¶ȱ仯����������ͼ��ʾ��
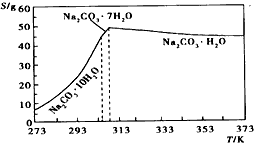
�ش��������⣺
��1����������Ҫ�ɷ�Ϊ____��
��2�������ȹ��ˡ���ԭ����____��
��3������ʵ���ҽ��С����ȹ��ˡ����ɲ�ȡ�Ĵ�ʩ��____��д��1�֣���
��4������ĸҺ��ѭ��ʹ�ã����ܳ��ֵ����⼰��ԭ����____��
��5����֪��
Na2CO3��l0H2O(s)=Na2CO3(s) +10H2O(g) ��H1= +532. 36kJ��mol-1
Na2CO3��10H2O(s)=Na2CO3��H2O(s) +9H2O(g) ��H2= +473.63kJ��mol-1
д��Na2CO3��H2O��ˮ��Ӧ���Ȼ�ѧ����ʽ__________________________________��
�ο��𰸣���1��Fe(OH)3��CaCO3��Mg(OH)2
��2����ֹ�¶��½�ʱNa2CO3��H2O�ܽ⣬��������Na2CO3��10H2O����Na2CO3��7H2O
��3��Ԥ�ȹ���װ��
��4����Ʒ���Ƚ��ͣ���Ϊѭ��ʹ��ʱĸҺ��Cl-��SO42-�ۻ������²�Ʒ����Na2SO4����
��5��Na2CO3��H2O==Na2CO3+H2O ��H=+58.73KJ/mol
���������
�����Ѷȣ�һ��
4��ѡ���� �ҹ���ѧ�Һ�°����NaHCO3�ܽ�ȱ�NaCl��Na2CO3��NH4HCO3��NH4Cl��С�����ʣ�����CO2+NH3+H2O+NaCl=NaHCO3��+NH4Cl�ķ�Ӧԭ���Ʊ������������ʵ���ҽ���ģ��ʵ�����������ʾ��ͼ��
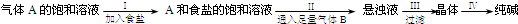
����������������ǣ�������
A��A������NH3��B������CO2
B���Ѵ���ڢõ��ľ�����ijЩ�����������ʣ����ʯ�ᣩ��Ͽ��Ƶ÷��ͷ�
C������ɹ㷺�����ڲ�������������ֽ����֯�ȹ�ҵ��
D���ڢ��������ǽ���������ˮ����ȡ��������ᾧ
�ο��𰸣�D
���������
�����Ѷȣ���
5������� �ҹ�����ר�Һ�°�ġ������Ƽ����Ϊ�����Ƽҵ������ͻ�����ף�����NaCl��NH3��CO2��Ϊԭ�����Ƶ�NaHCO3����������������йط�Ӧ�Ļ�ѧ����ʽΪ��
NH3+CO2+H2O=NH4HCO3��
NH4HCO3+NaCl=NaHCO3��+NH4Cl��
2NaHCO3?
Na2CO3+CO2��+H2O
��1��̼������뱥��ʳ��ˮ��Ӧ��������̼�����ƾ����ԭ����______
a��̼������������ˮ
b��̼�����������ֽ�
c��̼�����Ƶ��ܽ����Խ�С����������Һ�����Ƚᾧ����
��2��ij̽���С����������Ƽ�ԭ��������̼�����Ƶ��Ʊ�ʵ�飬ͬѧ�ǰ�������Ƶķ���ʵ�飮
��һλͬѧ��������̼����ͨ�뺬���ı���ʳ��ˮ���Ʊ�̼�����ƣ�ʵ��װ������ͼ��ʾ��ͼ�мг֡��̶��õ�����δ��������
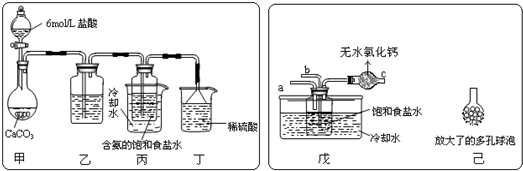
�Իش������й����⣺
������װ���е��Լ���______��
����װ����ϡ�����������______��
����ʵ����������NaHCO3?����IJ�����______���������������ƣ���
����һλͬѧ��ͼ����װ�ã�����װ��δ����������ʵ�飮
����ʵ��ʱ�����ȴ�______��ͨ��______?���壬�ٴ�______����ͨ��______���壻
������ͬѧ��������װ�õ�b���¶����Ӽ�װ�ã�������______��
��3��������д��һ��ʵ������ȡ����̼�����Ƶķ�����______��
�ο��𰸣���1��a��̼������������ˮ����A����
b��̼�����������ֽ⣬��������Һ�����Ƚᾧ�����أ���B����
c��̼�����Ƶ��ܽ��������Ȼ����˵̼�����Ƶ��ܽ�ȸ�СһЩ����������Һ�����Ƚᾧ��������C��ȷ��
��ѡC��
��2���٣�I������������ȡ������̼ʱ���������ӷ������ԣ�������̼�г��Ậ���Ȼ������壬̼�������������ᷴӦ���������̼��Ӧ������ͨ��̼�����Ƶ���Һ�ǿ��Գ���������̼�����е��Ȼ������壬�ʴ�Ϊ������̼��������Һ��
��II��ʵ������а���������ʣ�࣬��ϡ�������백����Ӧ������ϡ���������������ĩ��Ӧ��NH3���ʴ�Ϊ������δ��Ӧ��NH3��
��III�������NaHCO3����IJ����Ƿ��������Һ�壬�����õ�ʵ������ǹ��˲������ʴ�Ϊ�����ˣ�
�ڣ�I����ȡ̼������ʱ��Ҫ�õ������ı���ʳ��ˮ��������������ˮ��������̼������ˮ������Ӧ��ͨ�백��������a��ͨ�룬�Ӷ���֤�˴�bͨ�������̼ʱ��������̼����ַ�Ӧ���ʴ�Ϊ��a��NH3��b��CO2��
��II��װ�øĶ���Ӧ��Ķ�����̼����Һ�ĽӴ�����������˶�����̼�������ʣ��ʴ�Ϊ��������������Һ�Ӵ���������CO2�����ʣ�
��3���������ϢNH4HCO3+NaCl�TNaHCO3��+NH4Cl���ɵ���ȡ̼�����Ƶķ�����ͬʱҲ�ɲ����ռ���Һ��ͨ�����CO2��������Na2CO3 ��Һ��ͨ�����CO2 �ȵõ�̼�����ƣ�
�ʴ�Ϊ����̼���������������ʳ��ˮ��Ӧ�������ռ���Һ��ͨ�����CO2����������Na2CO3?��Һ��ͨ�����CO2?�ȣ�
���������
�����Ѷȣ�һ��