微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 湿润的蓝色石蕊试纸伸入盛有氯气的集气瓶中,观察到试纸变色的现象为( )
A.变红
B.变白
C.先变红后褪色
D.不变色
参考答案:氯气能与水反应生成盐酸和次氯酸,盐酸和次氯酸都具有酸性,使湿润的蓝色石蕊试纸变红,次氯酸具有强氧化性,有色物质为无色物质,所以现象为:先变红后变白,故选:C.
本题解析:
本题难度:简单
2、填空题 工业合成氨与制备硝酸一般可连续生产,流程如下:
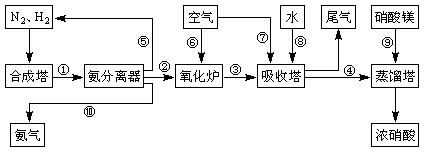
(1)工业生产时,制取氢气的一个反应为:CO+H2O(g) CO2+H2
CO2+H2
①t℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol・L-1。该温度下此反应的平衡常数K=_____(填计算结果)。
②保持温度不变,向上述平衡体系中再加入0.1molCO,当反应重新建立平衡时,水蒸气的转化率α(H2O)=________。
(2)合成塔中发生反应N2(g)+3H2(g) 2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中
2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中
T/K
| T1
| 573
| T2
|
K
| 1.00×107
| 2.45×105
| 1.88×103
|
T1____573K(填“>”、“<”或“=”)。
 (3)NH3和O2在铂系催化剂作用下从145℃就开始反应:
(3)NH3和O2在铂系催化剂作用下从145℃就开始反应:
4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H=-905kJ・mol-1
4NO(g)+6H2O(g) △H=-905kJ・mol-1
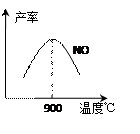
不同温度下NO产率如图所示。温度高于900℃时,
NO产率下降的原因?。
(4)吸收塔中发生反应的化学方程式为:
?。
(5)上述工业流程中,采用了循环操作工艺的是?(填序号)
(6)硝酸厂的尾气含有氮氧化物,如果不经处理直接排放将污染空气。目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);?△H=-574kJ・mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);?△H=-1160kJ・mol-1
则甲烷直接将NO2还原为N2的热化学方程式为:_____________________________。
参考答案:
(1)① 1(2分);?② 50%(2分);?(2)< (1分)
(3)温度高于900℃时,平衡向左移动。(1分)
(4)2NO+O2=2NO2,3NO2+H2O=2HNO3+NO(2分。1个方程式1分)
(5)⑤(1分)
(6)CH4(g)+2NO2(g)=CO2(g)+2H2O(g)+N2(g)?△H=-867kJ/mol(2分)
本题解析:略
本题难度:一般
3、计算题 不同卤素的原子互相可以共用电子对形成一系列化合物,这类化合物叫卤素互化物,现将4.66 g BrCln溶于水,再通入过量SO2,使其发生如下反应:BrCln+(n+1)H2O+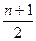 SO2====HBr+nHCl+
SO2====HBr+nHCl+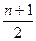 H2SO4
H2SO4
待反应完全后将所得溶液调至中性,再加入过量Ba(NO3)2溶液可生成11.65 g沉淀,试确定BrCln中的n值。
参考答案:n=3
本题解析:n(BaSO4)="0.05" mol
n(H2SO4)="0.05" mol
BrCln?―?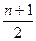 H2SO4
H2SO4
(80+35.5n)g 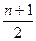 mol
mol
4.66 g? 0.05 mol
n=3
本题难度:简单
4、选择题 下列推断合理的是( )
A.新制氨水中共含有NH3和H2O两种分子
B.新制氯水光照后有气体逸出,该气体是Cl2
C.浓H2SO4有强氧化性,常温下能与Cu发生剧烈反应
D.由于浓硝酸具有强氧化性,故在常温下就可以将铁氧化
参考答案:A.氨气溶于水时,存在下列平衡NH3+H2O?NH3.H2O?NH4++OH-,所以溶液中存在NH3、H2O、NH3.H2O三种分子,故A错误;
B.氯气溶于水发生的反应为:Cl2+H2O=HCl+HClO,新制氯水光照时发生的反应为,2HClO?光照?.?2HCl+O2↑,所以生成的气体是氧气,故B错误;
C.浓硫酸具有强氧化性,但常温时和铜不反应,在加热时能和铜反应生成二氧化硫,故C错误;
D.常温时,浓硝酸和铁发生钝化现象从而阻止了进一步反应,故D正确;
故选D.
本题解析:
本题难度:一般
5、选择题 漂白粉的有效成分是(? )
A.次氯酸钙
B.氯化钙
C.次氯酸
D.次氯氯化钙和次氯酸钙
参考答案:A
本题解析:氯气和冷的消石灰反应即产生漂白粉,漂白粉是混合物,主要成分是氯化钙和次氯酸钙,有效成分是次氯酸钙。答案选A。
本题难度:简单