��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���������мȲ������Ӽ����ֲ������ۼ����У�������
A��ʳ��ˮ
B������
C������
D��NaOH
�ο��𰸣�A��ʳ��ˮ�к��Ȼ��ƺ�ˮ���Ȼ��������ӻ���������Ӽ���ˮ�ǹ��ۻ���������ۼ�����A����
B�����������ǵ�ԭ�ӷ��ӣ�ֻ���ڷ��Ӽ��������������ڻ�ѧ������B��ȷ��
C��������������ԭ�Ӻ���ԭ��֮����ڵĻ�ѧ���ǹ��ۼ�����C����
D���������������������Ӻ�������֮��������Ӽ�����ԭ�Ӻ���ԭ��֮����ڹ��ۼ�����D����
��ѡB��
���������
�����Ѷȣ���
2������� ��14�֣�NH3��һϵ�з�Ӧ���Եõ�HNO3��NH4NO3������ͼ��ʾ��
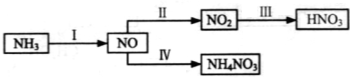
��1�����У�NH3��O2�ڴ��������·�Ӧ���仯ѧ����ʽ��_______________________��
��2�����У�2NO(g)��O2(g) 2NO2(g)��������������ͬʱ���ֱ���NO��ƽ��ת�����ڲ�ͬѹǿ(p1��p2)���¶ȱ仯������(��ͼ)��
2NO2(g)��������������ͬʱ���ֱ���NO��ƽ��ת�����ڲ�ͬѹǿ(p1��p2)���¶ȱ仯������(��ͼ)��
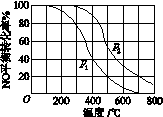
�ٱȽ�p1��p2�Ĵ�С��ϵ�� ��
�����¶����ߣ��÷�Ӧƽ�ⳣ���仯�������� ��
��3�����У������¶ȣ���NO2(g)ת��ΪN2O4(l)�����Ʊ�Ũ���ᡣ
����֪��2NO2(g) N2O4(g)��H1 2NO2(g)
N2O4(g)��H1 2NO2(g) N2O4(l) ��H2
N2O4(l) ��H2
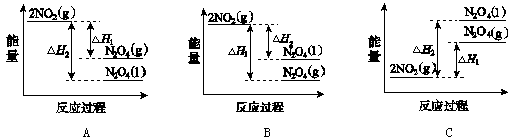
���������仯ʾ��ͼ�У���ȷ����(ѡ����ĸ) ��
��N2O4��O2��H2O���ϵĻ�ѧ����ʽ�� ��
��4�����У����NO�Ʊ�NH4NO3���乤��ԭ����ͼ��ʾ��
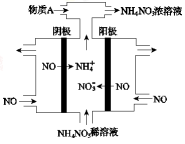
Ϊʹ������ȫ��ת��ΪNH4NO3���貹��A��A�� ��˵�����ɣ� ��
�ο��𰸣���14�֣�
��1��4NH3��5O2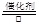 4NO��6H2O
4NO��6H2O
��2����p1��p2 �ڼ�С
��3����A ��2N2O4��O2��2H2O===4HNO3
��4��NH3���ݷ�Ӧ��8NO��7H2O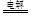 3NH4NO3��2HNO3����������HNO3��
3NH4NO3��2HNO3����������HNO3��
�����������1�����ڴ�������������������Ӧ����NO��ˮ���仯ѧ����ʽ��4NH3��5O2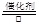 4NO��6H2O��
4NO��6H2O��
��2����2NO(g)��O2(g)  2NO2(g)���÷�Ӧ�����������С�Ŀ��淴Ӧ������ѹǿ��ƽ�������ƶ���NO��ƽ��ת�������ߣ�����p1��p2�Ĵ�С��ϵΪp1��p2���������¶ȣ�NO��ƽ��ת���ʽ��ͣ�˵��ƽ�������ƶ����������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ�����÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�����ڷ��ȷ�Ӧ�������¶ȣ���ѧ��Ӧƽ�ⳣ����С��
2NO2(g)���÷�Ӧ�����������С�Ŀ��淴Ӧ������ѹǿ��ƽ�������ƶ���NO��ƽ��ת�������ߣ�����p1��p2�Ĵ�С��ϵΪp1��p2���������¶ȣ�NO��ƽ��ת���ʽ��ͣ�˵��ƽ�������ƶ����������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ�����÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�����ڷ��ȷ�Ӧ�������¶ȣ���ѧ��Ӧƽ�ⳣ����С��
��3����2NO2(g) N2O4(g)��H1��2NO2(g)
N2O4(g)��H1��2NO2(g) N2O4(l)��H2���Ƿ��ȷ�Ӧ����Ӧ������������������������Cͼ����ͬһ������̬ʱ����������Һ��ʱ��������Aͼ��ȷ��Bͼ����ѡA��
N2O4(l)��H2���Ƿ��ȷ�Ӧ����Ӧ������������������������Cͼ����ͬһ������̬ʱ����������Һ��ʱ��������Aͼ��ȷ��Bͼ����ѡA��
��N2O4��O2��H2O��Ӧ�������ᣬ���ϵĻ�ѧ����ʽ��2N2O4��O2��2H2O===4HNO3��
��3�����ݵ��ʾ��ͼ��֪�����NO�Ʊ�����泥�������ӦΪ��NO-3e-+2H2O=NO3-+4H+��������ӦΪ��NO+5e-+6H+=NH4++H2O����������Ӧ�ɿ�����Ҫʹ���ӵ�ʧ�غ㣬����������NO3-������������������NH4+�������ܷ�ӦΪ8NO��7H2O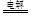 3NH4NO3��2HNO3��Ӧ���������İ�����������Ϊ���ݷ�Ӧ8NO��7H2O
3NH4NO3��2HNO3��Ӧ���������İ�����������Ϊ���ݷ�Ӧ8NO��7H2O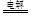 3NH4NO3��2HNO3����������HNO3�ࡣ
3NH4NO3��2HNO3����������HNO3�ࡣ
���㣺���黯ѧ��Ӧ����д��Ӱ�컯ѧƽ������أ���ѧͼ��ķ���������Ӧ�á�
�����Ѷȣ�����
3��ѡ���� ��8NH3+3Cl2�TN2+6NH4Cl��Ӧ�У���21.3�������μ��˷�Ӧ����������NH3��������
A.13.6��
B.10.2��
C.34��
D.3.4��
�ο��𰸣�D
�����������������8 H3+3Cl2�T
H3+3Cl2�T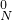 2+6
2+6 H4Cl��Ӧ�У��ɻ��ϼ۵ı仯��֪������3molCl2�μӷ�Ӧʱ��2molNH3����������������������ʵ��������ݷ�Ӧ�ķ���ʽ���㣮
H4Cl��Ӧ�У��ɻ��ϼ۵ı仯��֪������3molCl2�μӷ�Ӧʱ��2molNH3����������������������ʵ��������ݷ�Ӧ�ķ���ʽ���㣮
�����8 H3+3Cl2�T
H3+3Cl2�T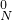 2+6
2+6 H4Cl��Ӧ�У��ɻ��ϼ۵ı仯��֪������3molCl2�μӷ�Ӧʱ��2molNH3��������
H4Cl��Ӧ�У��ɻ��ϼ۵ı仯��֪������3molCl2�μӷ�Ӧʱ��2molNH3��������
n��Cl2��=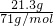 =0.3mol��
=0.3mol��
8NH3+3Cl2�TN2+6NH4Cl? ��������NH3
? 3mol? 2mol
? 0.3mol? 0.2mol
��������NH3��������0.2mol��17g/mol=3.4g��
��ѡD��
���������⿼��������ԭ��Ӧ�ļ��㣬��Ŀ�ѶȲ�����ע����ݷ���ʽ�ж�Ԫ�صĻ��ϼ۵ı仯���ж�NԪ���Ƿ�ȫ��������Ϊ������Ĺؼ���
�����Ѷȣ�һ��
4��ѡ���� ����ÿ���и������ڼ������Ӽ����й��ۼ���һ����
A��NaOH��H2SO4��(NH4)2SO4
B��MgO��Na2SO4��NH4HCO3
C��Na2O2��KOH��Na2SO4
D��HCl��Al2O3��MgCl2
�ο��𰸣�C
���������A��NaOH �������Ӽ��ͼ��Թ��ۼ��� H2SO4 ֻ���й��ۼ�����NH4��2SO4�������Ӽ����ۼ�����A����
B��MgO ֻ�����Ӽ���Na2SO4 �����Ӽ����ۼ���HNO3ֻ���й��ۼ�����B����
C��Na2O2��KOH��Na3PO4�����Ӽ����ۼ�����C��ȷ��
D��HClֻ�����ۼ���Fe2O3 ��MgCl2ֻ�����Ӽ�����D����
��ѡC��
������1�����ӻ������п��ܺ��м��Թ��ۼ�2����KOH��Ҳ���ܺ��зǼ��Թ��ۼ�����Na2O2��2�����ۻ�������һ���������Ӽ���
�����Ѷȣ���
5��ѡ���� �������ʼȺ����Ӽ��ֺ����ۼ�����
A��CO2
B��NaOH
C��CaCl2
D��C6H6
�ο��𰸣�B
���������A��ֻ�й��ۼ����ʴ���C��ֻ�����Ӽ����ʴ���D��ֻ�й��ۼ����ʴ�����ѡB��
���������⿼�黯ѧ������ȷ��ѧ����������ǽ����Ĺؼ�����Ŀ�ѶȲ���
�����Ѷȣ���