微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是
A.电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属
B.锅炉中沉积的CaSO4可用Na2CO3溶液浸泡后再用酸溶解去除
C.饱和Ca(OH)2溶液中加入一定量的生石灰,所得溶液的 pH 会增大
D.反应NH3(g)+HCl(g)=NH4Cl(s)△H<0在任何条件下均能自发进行
参考答案:B
本题解析:A:Zn、Fe等较为活泼的金属将失电子后转变了金属离子存在于溶液中,不正确
B:正确
C:生石灰可吸收水生成Ca(OH)2,仍为饱和溶液,pH不变(如果考虑温度影响,溶质浓度将减小,pH将减小),排除
D:反应的△S<0,△H<0,故在高温下将有可能不能自发进行,排除
答案为B
本题难度:简单
2、选择题 下列图示及其解释错误的是
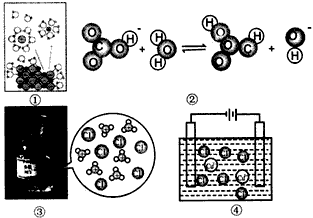
[? ]
A.图①表示NaCl在水中溶解和电离的示意图
B.图②表示碳酸氢根离子水解示意图
C.符合图③的电离方程式是:HCl+H2O=H3O++Cl-
D.图③表示用石墨电极电解氯化铜溶液的示意图
参考答案:D
本题解析:
本题难度:一般
3、选择题 用铂作电极电解500 mL含KNO3和Cu(NO3)2的混合蒲液一段时向后,在两极均生成11.2L标准状况下的气体,原溶液中Cu2+的物质的量浓度为?(?)
A.0.5 mol/L
B.1 mol/L
C.2 mol/L
D.无法确定
参考答案:B
本题解析:略
本题难度:简单
4、选择题 以铁为阳极、铜为阴极,对足量的NaOH溶液进行电解,一段时间后得到2molFe(OH)3沉淀,此时消耗水的物质的量共为( )
A.2mol
B.3mol
C.4mol
D.5mol
参考答案:根据铁原子守恒知,2molFe(OH)3→2molFe(OH)2,所以生成2molFe(OH)3需要2molFe(OH)2;
活泼金属铁作电解池阳极时,电解氢氧化钠溶液的电解方程式为Fe+2H2O?电解?.?H2+Fe(OH)2↓,
根据电解方程式得,生成2molFe(OH)2需要水的物质的量为4mol;
又氢氧化亚铁不稳定,能被氧气氧化成氢氧化铁沉淀,反应方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,
根据方程式得,生成2molFe(OH)3需要水的物质的量为1mol,
所以得到2molFe(OH)3沉淀消耗水的物质的量共为5mol.
故选D.
本题解析:
本题难度:简单
5、选择题 如图是模拟工业电解饱和食盐水的装置图,下列叙述正确的是

A.a 为电源的正极
B.通电一段时间后,石墨电极附近溶液先变红
C.Fe电极的电极反应是4OH-- 4e-=2H2O+O2↑
D.电解饱和食盐水的总反应是:
参考答案:D
本题解析:Fe极做阴极,a是负极,H+发生还原反应,产生H2和NaOH;石墨做正极,Cl-发生氧化反应,产生Cl2;答案选D。
本题难度:一般