| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ����ɡ�Ӱ�컯ѧ��Ӧ���ʵ����ء�����Ԥ�⣨2017��ǿ���棩(��)
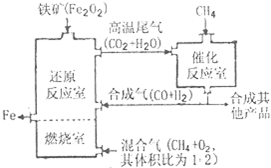 3��ʵ���� ��9�֣�ʵ������H2O2�ֽⷴӦ��ȡ����ʱ������������Լӿ췴Ӧ���ʣ�ij�о���ѧϰС��Ϊ�о�����FeCl3������O2�������ʵ�Ӱ�죬�������������ʵ�鷽�������±������������������Լ���һ�������Ϻ���з�Ӧ��
��1��������ͼװ�����Ƚϸ÷�Ӧ�ķ�Ӧ���ʿ���������Ӧ���Ũ�ȡ�����������Ӱ�����ʵ�����ȷ��֮����ͨ���� ��(��)�㷴Ӧ���ʡ� 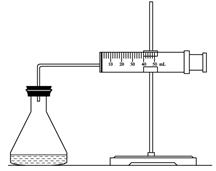 ��2��Ϊʵ��ʵ��Ŀ�ģ���V1= ��V2= �� V3= ��V4= �� ��3�������������յ�֪ʶ�жϣ�������ʵ���з�Ӧ�������Ŀ����� ���ʵ���š��� ��4����֪Fe3+��H2O2�ֽ�Ļ����ɷ�������Ӧ���У����е�һ����ӦΪ��2Fe3+ + H2O2 ==2Fe2+ + O2��+ 2H+����ڶ�����Ӧ�����ӷ���ʽΪ�� �� 4��ʵ���� ��18�֣�
��2��ʵ��١��ۿ�̽�� �Է�Ӧ���ʵ�Ӱ�죬���V4= ��V5= �� ��3�������йظõ����������ȷ���� A��ʵ��ǰ��Ӧ����һ�Ű�ֽ���ú�īˮ���ڰ�ֽ�ϻ���dzһ�µġ�+���֣�������ƿ�ײ���ʵ���м�¼��Ӧ��ʼ�������Ļ��ǽ���ƿ�ײ��ġ�+���ָպ���ȫ�ڸ������ʱ�� B����ʵ������ļ�����������Ͳ���¶ȼ� C��ʵ��ʱ��Ӧ�Ƚ���ȡ��Na2S2O3 ��H2SO4��Һ��ϣ�Ȼ��������Ӧ�¶ȵ���ˮԡ�з�Ӧ����¼ÿ�鷴Ӧ����ʱ�� D��ÿ��ʵ��������Ҫ��֧��Ͳ ��4��ʵ�������Ϊʲô���ò���һ��ʱ���ڷų�SO2�����������ʾ�÷�Ӧ�Ļ�ѧ��Ӧ���ʵĴ�С�� �� �����÷�Ӧ��I2+2Na2S2O3=Na2S4O6+2NaI���Զ����ⶨ�������������(Mr=158)�Ĵ��ȣ����ڳ�ȡWg��������ƹ�����Ʒ�����250mL����Һ��ȡ25.00mL������ƿ�У�����ָʾ�����ú���I2Ϊamol/L�ĵ�ˮ�ζ������ĵ�ˮbmL���� ��1��������еζ���Ӧ��ѡ����� ����ʽ���ʽ���ζ��ܣ��ζ�ǰ����ѡ�� ��ָʾ�����ζ��յ������Ϊ ��2�����ڸõζ�ʵ����йز�������������ȷ���� �� A���ζ�ǰ��Ӧ�Եζ��ܡ���ƿ������ϴ���� B���ζ������У���Һ�ε���ƿ�⣬��ʹ������ƫ�� C���ζ����ڵζ���ʼʱ���������ݣ��ζ���ɺ�������ʧ��������õĴ��Ƚ���ƫС D���ζ�ǰ���Ӷ������ζ�����ʱ���Ӷ�����������õĴ��Ƚ���ƫС ��3����Ʒ����������ƴ��ȵı���ʽΪ �� 5��ѡ���� ����˵������ȷ���� | ||||||||||||||||||||||||||||||||||||||||||||||||||
|
||
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | ||
| ��һƪ�����л�ѧ֪ʶ����ɡ���ѧʵ���.. | ||
| �����Ŀ |