��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��һ���������ܱ������и�������A��B��C��������һ�������·�����Ӧ�����Ļ�ѧƽ�⣺
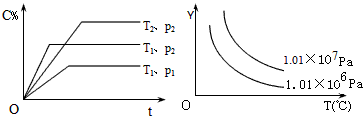
aA(g)+bB(g) xC(g)��������ͼ��ʾ�Ĺ�ϵ��c%��ʾƽ�������в� ��C�İٷֺ�����T��ʾ�¶ȣ�p��ʾѹǿ������ͼ�У�Y����ָ
xC(g)��������ͼ��ʾ�Ĺ�ϵ��c%��ʾƽ�������в� ��C�İٷֺ�����T��ʾ�¶ȣ�p��ʾѹǿ������ͼ�У�Y����ָ
[? ]
A����Ӧ��A�İٷֺ���
B��ƽ������������B�İٷֺ���
C��ƽ���������ܶ�
D��ƽ��������ƽ��Ħ������
2������� ��16�֣�CO���ִ����������Ļ���ԭ�ϣ������й����ⶼ��CO��ʹ���йء�
��1����������CO�����������Ӧ���������ʻ�����Ȼ�����ʻ����ֽ�Ӷ�ʵ�������ᴿ�������Եõ����ȴ�99��9%�ĸߴ��������巴ӦΪ��
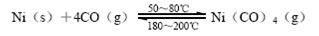
������Ӧ�Ħ�H 0��ѡ�����������������
��2����ҵ�Ͽ�����CO�����Ҵ�:2CO��g����4H2��g��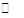 CH3CH2OH��g����H2O��g�� ��H1
CH3CH2OH��g����H2O��g�� ��H1
����֪��H2O��l��="==" H2O��g�� ��H2
CO��g����H2O��g��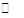 CO2��g����H2��g�� ��H3
CO2��g����H2��g�� ��H3
��ҵ��Ҳ������CO2��g����H2��g��Ϊԭ�Ϻϳ��Ҵ���
2CO2��g����6H2��g�� 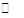 CH3CH2OH��g����3H2O��l�� ��H
CH3CH2OH��g����3H2O��l�� ��H
��H�릤H1����H2����H3֮��Ĺ�ϵ�ǣ���H��_______________________��
��3��һ�������£�H2��CO������̶����ܱ������з������·�Ӧ��
4H2��g��+2CO��g��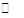 CH3OCH3��g��+H2O��g����
CH3OCH3��g��+H2O��g����
����ѡ�����жϸ÷�Ӧ�ﵽƽ��״̬�����ݵ���___ ��
A��2v��H2��= v��CO��
B��CO���������ʵ���CH3OCH3����������
C�������ڵ�ѹǿ���ֲ���
D�����������ܶȱ��ֲ���
E����������ƽ����Է�����������ʱ����仯
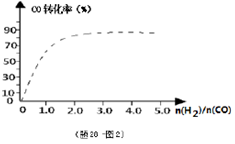
��4����ҵ�ɲ���CO��H2��Ӧ�ϳ�������Դ�״�����Ӧ:CO��g��+ 2H2��g��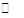 CH3OH��g��
CH3OH��g��
��һ�ݻ��ɱ���ܱ������г���10molCO��20mol H2���ڴ��������·�����Ӧ���ɼ״���CO��ƽ��ת���ʣ��������¶ȣ�T����ѹǿ��p���Ĺ�ϵ�磨ͼ28��-1����ʾ��
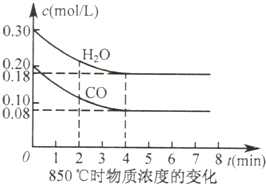
�ٺϳɼ״��ķ�ӦΪ__ __������ȡ������ȡ�����Ӧ��
��A��B��C�����ƽ�ⳣ��KA��KB��KC�Ĵ�С��ϵΪ___ ��
�����ﵽƽ��״̬Aʱ�����������Ϊ10L������ƽ��״̬Bʱ���������Ϊ__ __L��
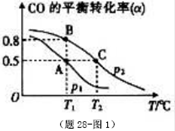
�ܣ���28-ͼ2��������Ϊ�÷�Ӧ��ʹ�ô��������¹�����ʼ������COͶ�ϱȺ�COƽ��ת���ʵĹ�ϵͼ������������ȫ��ͬʱ����ʵ������ʹ�ô��������COƽ��ת���ʵ�ʾ��ͼ��
��CO��ƽ��ת���ʣ��������¶ȣ�T����ѹǿ��p���Ĺ�ϵ�磨��28 -ͼ3����ʾ��ʵ������ʱ����������250 �桢1��3��104 kPa���ң�ѡ���ѹǿ��������________��

3��ѡ���� �Կ��淴Ӧ��A������+2B������?3C������+Q��������ͼ����a��Ӧ���̸ı�Ϊb��Ӧ���̣�����ȡ�Ĵ�ʩ�ǣ�������
A������B��Ũ��
B�������¶�
C���������
D������ѹǿ