| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点归纳《影响化学反应速率的因素》试题预测(2017年最新版)(十)
(2)现有反应③H2(g)+CO2(g)?H2O(g)+CO(g)写出该反应的平衡常数K3的数学表达式:K3=______. (3)根据反应①与②,可推导出K1、K2与K3之间的关系式______.据此关系式及上表数据,也能推断出反应③是“吸热”还是“放热”反应.问:要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有______(填写序号). A.缩小反应容器容积?B.扩大反应容器容积?C.降低温度 D.升高温度?E.使用合适的催化剂?F.设法减少CO的量 (4)图1、2表示该反应③在时刻t1达到平衡、在时刻t2分别因改变某个条件而发生变化的情况: 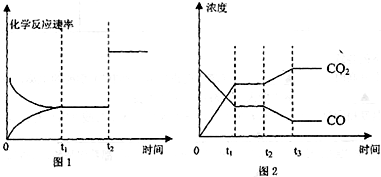 ①图1中时刻t2发生改变的条件是______ ②图2中时刻t2发生改变的条件是______. 参考答案:(1)由表中数据可知,温度升高,①的平衡常数增大,说明平衡向正反应方向移动,则正反应吸热, 本题解析: 本题难度:简单 4、选择题 反应:L(s)+aG(g) 参考答案:B 本题解析:根据图像可知,随温度的升高,G的含量逐渐降低,说明升高温度,平衡向正反应方向移动,因此正反应是吸热反应,A不正确,B正确。当温度相同时,压强越大G的含量越高,说明增大压强,平衡向逆反应方向移动,所以a小于b,选项CD不正确,答案选B。 本题难度:简单 5、选择题 为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位学生分别设计了如下A~D四个实验,你认为结论不正确的是 |
参考答案:A
本题解析:A.将铜片放入稀硫酸中,无现象。若再向所得的溶液中加入硝酸银溶液,Cu与AgNO3溶液会发生置换反应,产生Ag和Cu(NO3)2,而不是过程原电池,反应原理有误,错误。B.在相同条件下,等质量的大理石块和大理石粉与相同的盐酸反应,大理石粉由于与盐酸的接触面积增大,所以反应速率比块状的快,反应原理无误,正确;C.浓硝酸光照容易分解,所以将浓硝酸分别放在冷暗处和强光照射下,会发现光照可以加快浓硝酸的分解,反应原理无误,正确;D.两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,由于二氧化锰是氯酸钾分解的催化剂,因此产生氧气的速率加入少量二氧化锰的比没有加入的快,反应原理无误,正确。
考点:考查反应原理的正误判断的知识。
本题难度:一般
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:高中化学知识点总结《氯及其化合.. | ||