��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ����10�֣������������ʼ�ת���Ŀ�ͼ���ش��й����⣺

��1���ɷ�Ӧ�ٲ�����A��B�����Ĺ�ҵ������?��
��2��д����ͼ��D��E�Ļ�ѧʽ��D? ?��E??
?��E??
��3�����2mol Na2O2������ˮ������Ӧ���ɵñ�״�������������Ƕ���?L��ͬʱ��Ӧ��ת�Ƶ���������? ����NA��ʾ����ӵ�������
����NA��ʾ����ӵ�������
��4�������һ�������е�Сʵ�飬֤����Ӧ���Ƿ��ȷ�Ӧ��ʵ�鷽����?
��5�����A��B�������7.8g��ƽ��Ħ������10g��mol��1��������G��ַ�Ӧ��ͨ������Na2O2�㣬��ʹNa2O2����?g�����õ�O2?m ol��
ol��
�ο��𰸣���1��ˮú����1�֣�
��2��CO2? NaOH?����1�֣�?��3��2.24L? 2NA����1�֣�
��4��Na2O2�����������������CO2�ļ���ƿ�У���ȼ��˵���Ƿ��ȷ�Ӧ��ֱ��ͨCO2�ڱ�������Na2O2Ҳ�ɣ�����������Ҳ���֣���3�֣�
��5��7.8g? 0.39mol?����1�֣�
�����������
�����Ѷȣ���
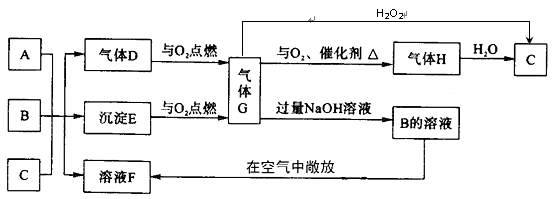
2������� (12��) A��B���������Σ��Ҷ������Σ�A�к�������Ԫ�أ�B�к�������Ԫ�أ�C��һ�ֳ�?���Ķ�Ԫǿ�ᣬ��A��B��C�нԺ���ͬһԪ�أ�D�г�������ζ��������ˮ��Һ��������ת����ϵ��
�Իش�
��1��A��D��G�Ļ�ѧʽ�ֱ�Ϊ?��?��?
��2��A��B��C��Ӧֻ����E��F�����ӷ���ʽΪ?��
��3��Ҫ��������ת����A��B���ʵ���֮�� Ӧ����Ĺ�ϵ��?��
Ӧ����Ĺ�ϵ��?��
��4������G��ʹ���������Һ��ɫ��������Ӧ�����ӷ���ʽΪ?��
�ο��𰸣�
��1��Na2S? H2S? SO2?��3�֣�?��2��2S2��+ SO32��+ 6H��=" 3S��+" 3H2O��3�֣�
��3��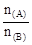 >
>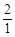 ?��3�֣�
?��3�֣�
��4��5SO2 + 2MnO4��+ 2H2O = 2Mn2��+ 5SO42��+ 4H����3�֣�
�����������
�����Ѷȣ���
3������� A��B��C��D��Ϊ��ѧ��ѧ�еij������ʣ������������Ϣ�ش����⡣
��1����֪���Ǵ������·�Ӧת����ϵ��A +B��C +D��δ��ƽ����Ӧ������ȥ����
�ٸ�ת����ϵ�����漰�ķ�ӦΪ�û���Ӧ����A�ǽ������ʣ�D�Ƿǽ������ʣ���A ԭ�ӵ���������Dԭ�ӵ�2������Ӧ�ķ���ʽ��?��
�ڸ�ת����ϵ�����漰�ķ�ӦΪ���û���Ӧ����A��D���ӵĺ������������Ϊ10����B��C�ܷ�����Ӧ����Ӧ�ķ���ʽ��?��
��2����֪���Ǵ������·�Ӧת����ϵ��A +B��C +D+H2O��δ��ƽ����Ӧ������ȥ����
�ٸ�ת����ϵ�����漰�ķ�ӦΪ������ԭ��Ӧ����C��D�����������ʹ����ʯ��ˮ����ǣ���A��Ħ������С��Bʱ������B������Ϊ?������C��D�������岻��ѡ�õ��Լ���?��
a��Ba(OH)2��Һ
b������KMnO4��Һ
c����ɫʯ����Һ
d��H2O2��BaCl2���Һ
e���ữ��Ba(NO3)2��Һ
�ڸ�ת����ϵ�����漰�ķ�ӦΪ��������ԭ��Ӧ����A���������ЧӦ����Ҫ����֮һ��C��D��Ϊ���Σ�D��B��Ӧ��ת��ΪC�����μӷ�Ӧ��A��B���ʵ���֮��Ϊ3��4ʱ����C��D���ʵ���֮��Ϊ?��
�ο��𰸣���1����2Mg + CO2 2MgO + C��2�֣�
2MgO + C��2�֣�
��4NH3+5O2 4NO+6H2O��2�֣�
4NO+6H2O��2�֣�
��2����Ũ���ᣨд������÷֣���2�֣�? ac��2�֣�
��1��2��2�֣�
�����������1����ֻ�н���þ������Ϊ̼ԭ����������һ����ӦΪþ�������̼��Ӧ����10��������ķ�Ӧ��������������Ӧ����һ��������ˮ���������������ȫȼ������һ����̼��ˮ�ȣ���2��CDΪ��������Ͷ�����̼����Ӧ��Ϊ̼��Ũ������������Ϊ������������Ba(OH)2��Һ��Ӧ���ɳ�������ʹʯ��ָʾ����Ӧ�ʺ�ɫ��������������л�ԭ���ܱ�����������������KMnO4��Һ��H2O2���ữ��Ba(NO3)2��Һ�����ᣩ������������ӴӶ��õ�����
�ڸ÷�ӦΪCO2+NaOH����Na2CO3+ NaHCO3+H2O����Na2CO3��NaHCO3���ʵ����ֱ�Ϊx��y��������ԭ���غ��2x+y=4?����̼ԭ���غ��x+y=3�����x=1��y=2��
�����Ѷȣ�һ��
4������� ij��ɫ����Һ���ܺ����������ӣ�K+��Al3+��Fe3+��Ba2+��NO3-��SO42-��HCO3-��Cl-��ȡ����Һ��������ʵ�飺
������ɫʯ����ֽ������Һ����ֽ�Ժ�ɫ��
��ȡ��Һ����������ͭƬ��ϡ���Ṳ�ȣ�������ɫ���壬������������������Ϊ����ɫ��
��ȡ��Һ���������백ˮ�а�ɫ�������ɣ��������������ˮ����������ʧ��
��ȡ��Һ�����������Ȼ�����Һ������ɫ������
��ȡʵ��?�ܺ�ij�����Һ��������������Һ������ɫ�������ټ��������ϡ���ᣬ��������ʧ��
��ش��������⣺
��1����ʵ��?���У���ͼ��ʾ�IJ�������ȷ����______������ţ���
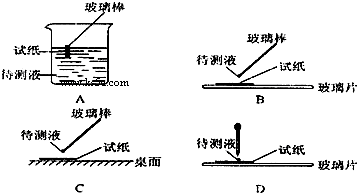
��2����������ʵ���ж�ԭ��Һ�п϶����ڵ�������______���϶������ڵ�������______��
��3��д����ڢ�����ʵ���йص����ӷ���ʽ��
��______
��______��
�ο��𰸣���1������ֽ������Һ�������ʱ��Ӧ�ò�����պȡ������Һ���ڷ��ڲ���Ƭ����ֽ�ϼ��飬�ʴ�Ϊ��B��
��2��������ɫʯ����ֽ������Һ����ֽ�Ժ�ɫ��˵����Һ�����ԣ���һ��������HCO3-����Һ��ɫ������Fe3+��
��ȡ��Һ����������ͭƬ��ϡ���Ṳ�ȣ�������ɫ���壬������������������Ϊ����ɫ��������ΪNO��˵����Һ�д���NO3-����
��ȡ��Һ���������백ˮ�а�ɫ�������ɣ��������������ˮ����������ʧ��˵������Al3+���ӣ���
��ȡ��Һ�����������Ȼ�����Һ������ɫ�������ó���Ϊ���ᱵ������˵������SO42-����һ�����Ậ��Ba2+��
��ȡʵ��?�ܺ�ij�����Һ��������������Һ������ɫ�������ټ��������ϡ���ᣬ��������ʧ������֤���Ƿ���Cl-���ӣ�����м����Ȼ�����
�ʴ�Ϊ��Al3+��NO3-��SO42-��Fe3+��Ba2+��HCO3-��
��3���ڷ�ӦΪ����ͭ����������������������ӷ���������ԭ��Ӧ����ͭ���Ӻ�һ���������壬��Ӧ�����ӷ���ʽΪ3Cu+8H++2NO3-�T3Cu2++2NO��+4H2O��
�ʴ�Ϊ��3Cu+8H++2NO3-�T3Cu2++2NO��+4H2O��
�۸���Al��OH��3������������ں�Al3+��Һ�м��백ˮֻ����Al��OH��3����Ӧ�����ӷ���ʽΪAl3++3NH3?H2O�TAl��OH��3��+3NH4+��
�ʴ�Ϊ��Al3++3NH3?H2O�TAl��OH��3��+3NH4+��
���������
�����Ѷȣ�һ��
5������� ���������ʵ�ת����ϵ�У�A��һ�ֵ��ʹ������ʣ�E��һ�ְ�ɫ�������ݴ���д���пհף�
��1��B�Ļ�ѧʽ��______��
��2��B��a��Һ��Ӧ�����ӷ���ʽ��______��
��3��G��������Һ��Ӧ�Ļ�ѧ����ʽ��______��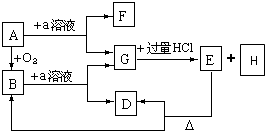
�ο��𰸣�BΪ�����E��һ�ְ�ɫ������E��
���������
�����Ѷȣ���