微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 有A、B、C、D四种化合物,其中A、C、D为盐且焰色反应均为黄色,而B是碱且透过钴玻璃观察焰色反应为紫色,A、C和盐酸反应均得到D的溶液,将固体C加热可得到A,若在A的溶液中通入一种无色无味气体,又可制得C,若B的溶液滴加到硫酸铜中溶液会出现蓝色沉淀E.试推断(写化学式)A:______、B:______、C:______、D:______、E:______.
参考答案:A、C、D为盐且焰色反应均为黄色,说明都含有钠元素的化合物;B是碱且透过钴玻璃观察焰色反应为紫色,判断为含K元素,A、C和盐酸反应均得到D的溶液,将固体C加热可得到A,若在A的溶液中通入一种无色无味气体,又可制得C,可以判断,无色无味的气体是CO2,A为Na2CO3,C为NaHCO3,D为NaCl,若B的溶液滴加到硫酸铜中溶液会出现蓝色沉淀E,说明B是KOH.综上所述可知A为Na2CO3,B为KOH,C为NaHCO3,D为NaCl,E为Cu(OH)2;
故答案为:Na2CO3;KOH;NaHCO3 ;NaCl;Cu(OH)2.
本题解析:
本题难度:一般
2、填空题 (8分) A-I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出)。已知H为主族元素的固态氧化物,F是红褐色难溶于水的沉淀,且A、B、C、D、E、F六种物质中均含同一种元素。

请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素在元素周期表中位置?
(2)写出C、H物质的化学式:C?;? H?[来源:
(3)写出反应①、⑥的化学方程式和③、⑦的离子方程式:
反应①:________________________________
反应⑥:________________________________
反应③:_______________ _________________
_________________
反应⑦:________________________________
(4)反应⑥过程中的现象是??。
参考答案:(8分)(1)第四周期第Ⅷ族(2) C: F eCl2、H: Al2O3
eCl2、H: Al2O3
(3)① 8Al+3Fe3O4 4Al2O3+9Fe;⑥ 4Fe(OH)2+O2+2H2O=4Fe(OH)3
4Al2O3+9Fe;⑥ 4Fe(OH)2+O2+2H2O=4Fe(OH)3
③Fe3O4+8H+=Fe2++2Fe3++4H2O;⑦2Al+2OH-+2H2O=2AlO2-+3H2↑
(4)有白色沉淀迅速变成灰绿色,最终变为红褐色
本题解析:略
本题难度:一般
3、推断题 (14分)下图所示物质(部分产物和反应条件未标出)中,只有A是单质,常温下B和C呈气态,且B是导致酸雨的大气污染物,D是氧化物,W是淡黄色固体。
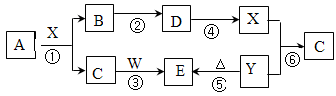
据此回答下列问题:
(1)B、C、D的化学式分别为:B?、C?、D?;从物质分类角度,上图所给物质中属于钠盐的是?(填写化学式)。
(2)上图所给物质在6个反应中只做还原剂的有?(填写化学式)。
(3)上图反应中不属于氧化还原反应的有?(填写序号)。
(4)写出A和X反应的化学方程式?;若生成的B在标准状况下的体积为22.4L,则参加反应的A的物质的量为?,反应中转移的电子数目为?。
(5)请写出C和W反应的化学方程式:?。
(6)请写出X和 Y反应的离子方程式:?。
参考答案:(1)SO2? CO2? SO3(各1分)? Na2CO3、NaHCO3 ?(全部选对得1分)
(2)C、SO2?(全部选对得1分)
(3)④ ⑤ ⑥(全部选对得1分)
(4)C+2H2SO4(浓) CO2↑+2SO2↑+2H2O(2分);0.5mol? 1.204×1024(各1分)
CO2↑+2SO2↑+2H2O(2分);0.5mol? 1.204×1024(各1分)
(5)2Na2O2+2CO2=2Na2CO3+O2(2分)
(6)H++HCO3-=CO2↑+H2O(2分)
本题解析:由题意“B是导致酸雨的大气污染物,D是氧化物,W是淡黄色固体”可推知B为二氧化硫,D为三氧化硫,X为硫酸,W为过氧化钠,再由“只有A是单质,常温下B和C呈气态,”可推知C为二氧化碳。则E为碳酸钠,Y为碳酸氢钠,A为碳。
(1)SO2? CO2? SO3? Na2CO3、NaHCO3 ?
(2)整个过程只有①②③属于氧化还原反应,①中C做还原剂,②中二氧化硫做还原剂,③中过氧化钠既做氧化剂又做还原剂。
(3)④ ⑤ ⑥属于非氧化还原反应。
(4)A和X反应为C与浓硫酸反应,方程式为:C+2H2SO4(浓) CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
根据方程式可知生成1mol二氧化硫需反应0.5molC,转移电子数为2mol即2NA。
(5)C和W反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2
(6)请写出X和 Y反应的离子方程式:H++HCO3-=CO2↑+H2O
点评:本题不难,根据题目的信息,结合所掌握的物质的特性,可推出相关物质。
本题难度:困难
4、填空题 A、B、C、D为四种由短周期元素形成的化合物,它们的焰色反应均为黄色,并有下列转化关系。A中既含有离子键又含有非极性共价键,D含四种元素。
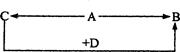
(1)A的电子式是?。
(2)把1 molCO2通入含2 molC的溶液后,溶液中各离子浓度由大到小的顺序是?。
(3)1 molA与2 molD固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体是??(用化学式表示)。
参考答案:
(1)Na+ Na+
Na+
(2)c(Na+)> c (CO32-)> c (OH-)> c (HCO3-)> c (H+)
(3)Na2CO3
本题解析:
本题考查元素的推断。关键在于找到题眼进行突破,本题的题眼有它们的焰色反应均为黄色――说明是由Na的化合物,在钠的化合物中只有Na2O2中既含有离子键又含有非极性共价键,故可确定A是Na2O2,Na2O2能与H2O生成NaOH,与CO2反应生成Na2CO3,而1 molCO2只能与含1 mol Na2CO3的溶液,故C应该是NaOH,B为Na2CO3,D是四种元素组成,和NaOH反应生成Na2CO3,故D应为NaHCO3。
本题难度:一般
5、填空题 中学化学中常见的几种物质存在如下关系,其中甲是黑色非金属单质,乙是生活中常见的金属单质,D是红棕色气体.(图中部分产物和反应条件已略去)
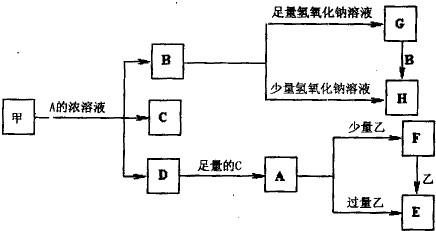
回答下列问题:
(1)写出甲与A的浓溶液反应的化学方程式______.
(2)将等体积等浓度的G溶液和H溶液混合后得到的溶液中的离子浓度大小关系为______.
(3)除去G固体中含有H杂质采用的方法是______.
(4)A溶液与一种能使湿润的红色石蕊试纸变蓝色的气体反应,生成一种盐,该盐的溶液呈酸性,其原因是(用离子方程式表示)______.
(5)写出向E溶液中加入少量稀硫酸后反应的离子方程式______.将溶液F加热蒸干、灼烧到质量不再减少时所得固体物质的化学式为______.
(6)确定E中阳离子实验的方法为______.
参考答案:D是红棕色气体,说明D是二氧化氮;甲是黑色非金属单质,且和A的浓溶液反应生成二氧化氮,说明甲是碳,A溶液是浓硝酸,则B是二氧化碳,C是水;二氧化碳和足量氢氧化钠溶液反应生成碳酸钠和水,而二氧化碳和少量氢氧化钠溶液反应生成碳酸氢钠和水,所以G是碳酸钠,而H是碳酸氢钠;二氧化氮和水反应生成硝酸;由硝酸和少量乙反应生成F,和过量乙反应生成E,F和乙又可生成E,可知乙为金属铁,而F为硝酸铁,E为硝酸亚铁,
(1)D是红棕色气体,说明D是二氧化氮;由甲是黑色非金属单质,且和A的浓溶液反应生成二氧化氮,说明甲是碳,A溶液是浓硝酸,则B是二氧化碳,C是水,反应的化学方程式为:C+4HNO3(浓)?△?.??CO2↑+4NO2↑+2H2O;故答案为:C+4HNO3(浓)?△?.??CO2↑+4NO2↑+2H2O;
(2)碳酸钠和碳酸氢钠的混合液中,碳酸根的水解程度大于碳酸氢根的水解程度,溶液显示碱性,离子浓度大小关系是:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),故答案为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+);
(3)碳酸氢钠受热分解为碳酸钠、水以及二氧化碳,而碳酸钠受热稳定,可以用加热法除去碳酸钠中的碳酸氢钠,故答案为:加热;
(4)能使湿润的红色石蕊试 91ExaM.org纸变蓝色的气体反应是氨气,硝酸和氨气反应生成硝酸铵,由于铵根水解导致溶液显示酸性,故答案为:NH4++H2O

NH3?H2O+H+;
(5)向硝酸亚铁中加入硫酸,相等于存在硝酸,硝酸可以将亚铁离子氧化,实质是:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,硝酸亚铁易被氧气氧化为硝酸铁,三价铁水解生成氢氧化铁,受热分解为氧化铁,故答案为:3Fe2++NO3-+4H+=3?Fe3++NO↑+2H2O;Fe2O3;
(6)亚铁离子易被氧化为三价铁,三价铁遇到硫氰酸钾显示红色,亚铁离子的检验方法:先加入KSCN溶液无变化再加入氯水(或盐酸等)溶液变红色,故答案为:先加入KSCN溶液无变化,再加入氯水(或盐酸等)溶液变红色.
本题解析:
本题难度:简单