微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 “烤蓝”是一种常用的铁器表面处理方法,可在铁器表面生成一层致密的四氧化三铁膜,增强铁器的抗腐蚀能力。其中常用的一种方法是采用发蓝溶液(如一种配方为:硝酸钠50-100克、氢氧化钠600-700 克、亚硝酸钠100-200克、水1000克)。下列说法不正确的是
[? ]
A.未作“烤蓝”和其他防腐蚀处理的铁器在空气中易发生电化学腐蚀
B.“烤蓝”后的铁器不易生锈
C.“烤蓝”过程中发生了氧化还原反应
D.“烤蓝”时铁作氧化剂
参考答案:D
本题解析:
本题难度:简单
2、选择题 下列措施不能有效防止钢铁腐蚀的是
A.在钢铁中加入铬
B.把钢铁零件放在机油中保存
C.在较小钢铁制品的表面包裹塑料
D.在大型铁壳船表面喷涂油漆并铆上铜块
参考答案:D
本题解析:铁比铜活泼,二者形成的原电池,铁是负极,加速铁的腐蚀,D不正确.其余是正确的.答案选D.
本题难度:简单
3、选择题 化学与社会、生产、生活息息相关,以下对化学知识应用合理的是
①向奶粉中添加三聚氰胺,提高蛋白质的含量.给婴幼儿健康带来危害,因此我们应尽量少食用含有食品添加剂的食品,以防中毒
②超市不再提供免费塑料袋,可以帮助控制“白色污染”
③纯铁比普通钢更耐腐蚀,应多用纯铁作材料
④多位科学家因研制出新型催化剂而获得诺贝尔奖.是因为催化剂可以最大限度的提
高反应物的转化率( )
A.①②正确
B.只有②③正确
C.只有②正确
D.①②③④均正确
参考答案:①食品添加剂是指用于改善食品口味、延长食品保存期甚至增加食品营养成分的一类天然或化学合成物质,但如果被过度使用,则会危害人的健康,但不是中毒,故①错误;
②超市不再提供免费塑料袋,减少了塑料袋的使用,可以帮助控制“白色污染”,故②正确;
③纯铁比普通钢更耐腐蚀,但纯铁质软,所以纯铁不能作材料,故③错误;
④催化剂只能改变反应速率,不能改变反应的限度提高反应物的转化率,故④错误;
故选C.
本题解析:
本题难度:简单
4、选择题 由化学能转变的热能或电能仍然是人类使用的主要能源。根据右图所示的装置,判断下列说法不正确的是
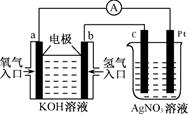
A.该装置中Pt极为阳极
B.当c极的质量变化了2.16g时,a极上消耗的O2的体积为1.12L
C.该装置中b极的电极反应式是:H2+2OH--2e-==2H2O
D.该装置中a极为正极,发生还原反应
参考答案:B
本题解析:左边是氢氧燃料电池,总反应为2H2+O2=2H2O,通氢气的一极为负极,电极反应式为2H2+2OH--2e-=2H2O,通氧气的一端为正极,电极反应式为O2+2H2O+4e-=4OH-。右边是电解池,c极为阴极,电极反应式为Ag++e-=Ag,Pt极为阳极,电极反应式为2H2O-4e-=4H++O2↑。由电子转移相等得:2H2~O2~4Ag,当c极增重2.16g时,a极消耗的O2为0.005mol,标准状况下为112mL,B错误。
点评:串联电路中,各个电极上通过的电子物质的量相等。
本题难度:一般
5、填空题 (12分)依据氧化还原反应:2Fe3+(aq)+Fe(s)=3Fe2+(aq),设计原电池并完成如图所示实验。请回答下列问题:

⑴电极X的材料是?;石墨电极为电池的?极。
⑵B装置中发生的电极反应方程式为?;表面皿中溶质Na2SO4的作用是?。
⑶铜丝b与滤纸接触处的现象为?;此处电极反应方程式为:?。
参考答案:(1)铁?正?(2)Fe3++e-=Fe2+?增强溶液的导电性
(3)滤纸变为红色? 2H2O+2e-=H2↑+2OH-或2H++2e-=H2↑
本题解析:(1)根据反应式可知,铁离子得到电子,是氧化剂。铁失去电子,是还原剂。由于A中溶液是氯化亚铁,所以X电极是铁,石墨电极是正极。
(2)原电池中正极得到电子,所以B中正极反应式是Fe3++e-=Fe2+;硫酸钠是强电解质,所以其作用是增强溶液的导电性。
(3)铜丝b和电源的负极相连,作阴极,溶液中的氢离子放电,生成氢气,电极反应式是2H++2e-=H2↑;由于氢离子放电,破坏了阴极周围水的电离平衡,所以阴极周围溶液显碱性,则滤纸变为红色。
本题难度:一般