微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 海水是镁资源的贮存库,从海水中提取MgCl2用于制取金属镁,以被广泛的应用于工业生产,其制取镁的方法是
[? ]
A.热分解法
B.用CO还原
C.电解法
D.湿法冶金
参考答案:C
本题解析:
本题难度:简单
2、选择题 水资源非常重要,海水淡化是海岛地区提供淡水的重要手段,所谓海水淡化是指除去海水中的盐分以获得淡水的工艺过程(又称海水脱盐),其方法较多,如反渗透法、水合物法、电渗透法、离子交换法和压渗法等。下列方法中也可以用来进行海水淡化的是
[? ]
A.过滤法
B.蒸馏法
C.分液法
D.萃取法
参考答案:B
本题解析:
本题难度:简单
3、简答题 海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.
(1)在光照条件下.氯气和氢气反应过程如下:
①Cl2→Cl+Cl?②Cl+H2→HCl+H?③H+Cl2→HCl+Cl?…
反应②中形成的化合物的电子式为______;反应③中被破坏的化学键属于______键(填“极性”或“非极性”).
(2)在短周期主族元素中,氯元素及与其相邻元素的原予半径从大到小的顺序是______.
(用元素符号表示).与氯元素同周期且金属性最强的元素位于周期表的第______周期______族.
(3)卤索单质及化合物在许多性质上都存在着递变规律.下列有关说法正确的是______.
a.卤化银的颜色按AgCl、AgBr、AgI的顺序依次加深
b?卤化氢的键长按H-F、H-Cl、H-Br、H-I的顺序依次减小
c?卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d?卤索单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
(4)卤素单质的键能大小如图.由图推断:
①非金属性强的卤素,其单质分子的化学键______断裂(填“容易”或“不容易”或“不一定容易”).
②卤素单质键能大小与键长的关系为:______.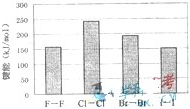
参考答案:(1)反应②中形成的化合物是氯化氢,氯化氢为共价化合物,一个氢原子核外为1个电子,1个氯原子核外最外层有7个电子,HCl分子中共用一对电子,所以电子式为

;反应③为氢原子和氯气反应,所以破坏的是氯气分子中的氯氯键,同一元素组成的双原子分子为非极性分子,所以破坏的是非极性共价键,
故答案为:

;非极性;
(2)短周期主族元素中与氯元素相邻的有F和S,根据同周期和同主族元素原子的半径变化规律同一周期,从左到右,原子序数增大,半径在逐渐减小,所以原子半径S>Cl,同一主族,从上往下,半径在逐渐增大,所以原子半径Cl>F,综上可知,三者的原子半径从大到小的顺序是S>Cl>F;与氯同周期,金属性最强的元素位于该周期的最左侧,为Na元素,钠为第三周期,第IA,
故答案为:S>Cl>F;?三;IA;
(3)a.卤化银的颜色按AgCl为白色固体、AgBr为浅黄色固体、AgI为黄色固体,所以它们的颜色依次加深,故a正确;
b?同一主族,从上往下,半径在逐渐增大,所以原子半径I>Br>Cl>F,所以卤化氢的键长按H-F、H-Cl、H-Br、H-I的顺序依次增大,故b错误;
c?随着原子序数的增大,单质得电子能力逐渐减弱,所以其阴离子失电子能力逐渐增强,所以HF、HCl、HBr、HI的还原性按HF、HCl、HBr、HI的顺序依次增强,故C错误;
d?随着原子序数的增大,单质得电子能力逐渐减弱,所以单质F2、Cl2、Br2、I2中与氢气化合逐渐困难,故d错误;
故答案为:a;
(4)①从卤素单质的键能大小图可知,氯气分子中氯氯键的键能大于溴单质中溴溴键,而氯原子的得电子能力大于溴,所以非金属性强的卤素,其单质分子的化学键不一定容易断裂,
故答案为:不一定容易;?
②同一主族,从上往下,半径在逐渐增大,所以原子半径I>Br>Cl>F,所以卤化氢的键长按H-F、H-Cl、H-Br、H-I的顺序依次增大,从卤素单质的键能大小图可知,除F2外.键长增大,而键能与键长成反比,所以依次减小,
故答案为:除F2外.键长增大,键能减小;
本题解析:
本题难度:一般
4、选择题 下列有关资源的开发利用说法正确的是( ? )
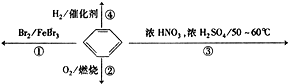
A.从海带中提取碘单质的过程一定涉及氧化还原反应
B.从海水中可以得到NaCl,电解NaCl溶液可制备Na和Cl2
C.天然气、乙醇和水煤气分别属于化石能源、不可再生能源和二次能源
D.Cu、Al、Hg可以分别用热还原CuO、电解AlCl3和热分解HgO冶炼得到
参考答案:A
本题解析:
本题难度:一般
5、填空题 镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的,主要步骤如下图所示
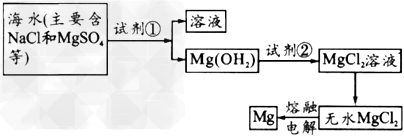
(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用__________________,MgSO4完全转化为沉淀,加入①的量应_______________。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是________。
(3)无水MgCl2在熔融状态下,如何得到单质镁?____________________。 ?
(4)写出①、②两个过程中发生反应的离子方程式:_____________________________。
参考答案:(1)Ca(OH)2;过量?
(2)过滤?
(3)电解法;MgCl2(熔融) Mg+Cl2↑?
Mg+Cl2↑?
(4)①Mg2++2OH-=Mg(OH)2↓、②Mg(OH)2+2H+=Mg2++2H2O
本题解析:
本题难度:一般