微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (16分)氨是一种重要的化工原料,氨的合成和应用是当前的重要研究内容之一。
(1)一定条件下,在一个密闭容器中充入气体:N2 2mol、H2 6mol,达平衡后N2的转化率为50%,同时放热92.3KJ。该反应的热化学方程式为:______________________________。
(2)传统哈伯法合成氨工艺中相关的反应式为:N2+3H2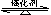 2NH3。
2NH3。
①该反应的平衡常数K的表达式为:K=______________。升高温度,K值______(填“增大”“减小”或“不变”)。
②不同温度、压强下,合成氨平衡体系中NH3的物质的量分数见下表(N2和H2的起始物质的量之比为1∶3)。分析表中数据,?(填温度和压强)。时H2转化率最高,实际工业生产中不选用该条件的主要原因是?。
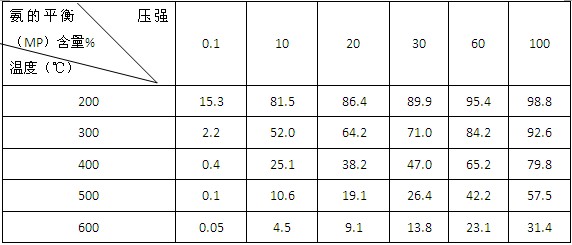
③下列关于合成氨说法正确是?(填字母)
A.使用催化剂可以提高氮气的转化率
B.寻找常温下的合适催化剂是未来研究的方向
C.由于ΔH<0、ΔS>0,故合成氨反应一定能自发进行
(3)最近美国Simons等科学家发明了不必使氨先裂化为氢就可直接用于燃料电池的方法。其装置为用铂黑作为电极,加入电解质溶液中,一个电极通入空气,另一电极通入氨气。其电池反应为4NH3+3O2=2N2+6H2O,你认为电解质溶液应显??性(填“酸性”、“中性"、“碱性”),写出负极电极反应式?。
(4)工业上净化处理铬污染方法之一是:将含K2Cr2O7酸性废水放入电解槽内,加入适量的NaCl,以Fe和石墨为电极进行电解。经过一段时间后,生成Cr(OH)3和Fe(OH)3沉淀除去(已知Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)。
已知电解后的溶液中c(Fe3+)为2.0×10-13mol/L,则溶液中c(Cr3+)为?mol/L。
2、选择题 反应NH4HS(s) NH3(g)+H2S(g)在一定温度下达到平衡。下列各种情况下,不能使平衡发生移动的是(?)
NH3(g)+H2S(g)在一定温度下达到平衡。下列各种情况下,不能使平衡发生移动的是(?)
A.温度、容积不变时,通入SO2气体
B.移走一部分NH4HS固体
C.容积不变,充入氮气
D.充入氮气,保持压强不变
3、选择题 能够说明H2(g)+I2(g) 2HI(g)(HI为无色气体)已达平衡状态的是(? )
2HI(g)(HI为无色气体)已达平衡状态的是(? )
A.一个H-H键断裂的同时有两个H-I键形成
B.v (H2)正= v (HI) 逆时的状态
C.恒温恒容时,反应混合物总质量保持不变的状态
D.恒温恒容时,体系的颜色不再发生变化的状态
4、选择题 在2 L的密闭容器中发生反应xA(g)+yB(g) zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
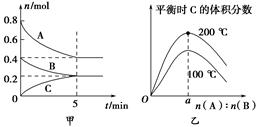
A.200 ℃时,反应从开始到平衡的平均速率v(B)=0.04 mol・L-1・min-1
B.200℃时,该反应的平衡常数为25 L2/mol2
C.当外界条件由200℃降温到100℃,原平衡一定被破坏,且正逆反应速率均增大
D.由图乙可知,反应xA(g)+yB(g) zC(g)的ΔH<0,且a=2
zC(g)的ΔH<0,且a=2
5、选择题 重铬酸钾溶液中存在如下平衡:Cr2O72-(橙红色)+H2O  2H++2CrO42-(黄色),向K2Cr2O7溶液中加入下列哪种试剂,溶液颜色会从黄色逐渐变为橙红色
2H++2CrO42-(黄色),向K2Cr2O7溶液中加入下列哪种试剂,溶液颜色会从黄色逐渐变为橙红色
A.NaHSO4
B.NaHCO3
C.Na2CO3
D.CH3COONa