��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��16�֣�����һ����Ҫ�Ļ���ԭ�ϣ����ĺϳɺ�Ӧ���ǵ�ǰ����Ҫ�о�����֮һ��
(1)һ�������£���һ���ܱ������г������壺N2 2mol��H2 6mol����ƽ���N2��ת����Ϊ50%��ͬʱ����92.3KJ���÷�Ӧ���Ȼ�ѧ����ʽΪ��______________________________��
(2)��ͳ�������ϳɰ���������صķ�ӦʽΪ��N2+3H2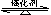 2NH3��
2NH3��
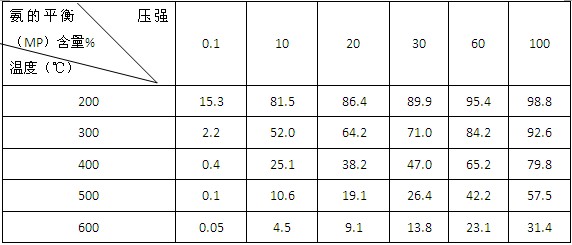
�ٸ÷�Ӧ��ƽ�ⳣ��K�ı���ʽΪ��K=______________�������¶ȣ�Kֵ______���������С�����䡱����
�ڲ�ͬ�¶ȡ�ѹǿ�£��ϳɰ�ƽ����ϵ��NH3�����ʵ����������±���N2��H2����ʼ���ʵ���֮��Ϊ1��3���������������ݣ�?�����¶Ⱥ�ѹǿ����ʱH2ת������ߣ�ʵ�ʹ�ҵ�����в�ѡ�ø���������Ҫԭ����?��
�����й��ںϳɰ�˵����ȷ��?������ĸ��
A��ʹ�ô���������ߵ�����ת����
B��Ѱ�ҳ����µĺ��ʴ�����δ���о��ķ���
C�����ڦ�H<0����S>0���ʺϳɰ���Ӧһ�����Է�����
(3)�������Simons�ȿ�ѧ�ҷ����˲���ʹ�����ѻ�Ϊ��Ϳ�ֱ������ȼ�ϵ�صķ�������װ��Ϊ�ò�����Ϊ�缫������������Һ�У�һ���缫ͨ���������һ�缫ͨ�백�������ط�ӦΪ4NH3+3O2=2N2+6H2O������Ϊ�������ҺӦ��??��(����ԡ���������"�������ԡ�)��д�������缫��Ӧʽ?��
(4)��ҵ�Ͼ�����������Ⱦ����֮һ�ǣ�����K2Cr2O7���Է�ˮ��������ڣ�����������NaCl����Fe��ʯīΪ�缫���е�⡣����һ��ʱ�������Cr(OH)3��Fe(OH)3������ȥ����֪Ksp[Fe(OH)3]=4.0��10-38��Ksp[Cr(OH)3]=6.0��10-31����
��֪�������Һ��c(Fe3+)Ϊ2.0��10-13mol/L������Һ��c(Cr3+)Ϊ?mol/L��
�ο��𰸣�(1) N2��g��+3H2��g��=2NH3��g�����SH= -92.3KJ/mol����2�֣�
��2����K=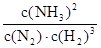 ��1�֣���С��1�֣���200�桢100MPa��2�֣�
��1�֣���С��1�֣���200�桢100MPa��2�֣�
ѹǿ̫�������豸��������ʵ�֣�2�֣�?��B��2�֣�
��3�����ԣ�2�֣�? 2NH3-6e- +6OH-=N2+3H2O��2�֣�
��4��3��10��6 (2)��
�����������1�����ĵ���������2mol��50����1mol�����Ȼ�ѧ����ʽΪN2��g��+3H2��g��
=2NH3��g�����SH= -92.3KJ/mol��
��2��ƽ�ⳣ����֪��һ�������¿��淴Ӧ�ﵽƽ��ʱ������Ũ�ȵ���֮���ͷ�Ӧ��Ũ
�ȵ���֮���ı�ֵ������Ӧ���ȣ������¶�ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С�����ݱ������ݿ�֪��200�桢100Mpaʱ���������ʵ�����࣬��������ת���������Ȼ��ѹ�������ṩ������ת���ʣ���ѹǿ̫�������豸��������ʵ�֡�����ֻ�ܸı䷴Ӧ���ʣ������ܸı仯ѧƽ��״̬�����ݡ�G����H��T��S֪������H<0����S>0ʱ��Ӧ�Է��������̵��Է���ֻ�������жϹ��̵ķ�����ȷ�������Ƿ�һ���ᷢ�����̷��������ʡ����Դ�ѡB��
��3���������ᷴӦ����NH4�������Ե������ҺӦ���Լ��ԡ��ڷ�Ӧ�а���ʧȥ����
���������ڸ���ͨ�룬�缫��Ӧʽ��2NH3��6e-��+6OH��=N2+3H2O��
��7������Ksp[Fe(OH)3]=4.0��10-38��Ksp[Cr(OH)3]=6.0��10-31����֪
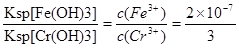 �����Ե���Һ��c(Fe3+)Ϊ2.0��10-13mol/Lʱ����Һ��c(Cr3+)Ϊ3��10��6 mol/L��
�����Ե���Һ��c(Fe3+)Ϊ2.0��10-13mol/Lʱ����Һ��c(Cr3+)Ϊ3��10��6 mol/L��
�����Ѷȣ���
2��ѡ���� ��ӦNH4HS��s�� NH3(g)+H2S(g)��һ���¶��´ﵽƽ�⡣���и�������£�����ʹƽ�ⷢ���ƶ����ǣ�?��
NH3(g)+H2S(g)��һ���¶��´ﵽƽ�⡣���и�������£�����ʹƽ�ⷢ���ƶ����ǣ�?��
A���¶ȡ��ݻ�����ʱ��ͨ��SO2����
B������һ����NH4HS����
C���ݻ����䣬���뵪��
D�����뵪��������ѹǿ����
�ο��𰸣�BC
���������Aѡ�����Ӧ��SO2+2H2S 3S+2H2O����С������Ũ�ȣ���ƽ�������ƶ���Bѡ�NH4HSΪ���壬�ʲ���ʹƽ���ƶ���Cѡ������ݻ����䣬ԭƽ���и����ʵ�Ũ��û�仯���ʲ������ƶ���Dѡ����벻�μӷ�Ӧ��N2���Һ�ѹ�����������Ũ�ȼ�С����ƽ�ⷢ���ƶ�����ѡBC��
3S+2H2O����С������Ũ�ȣ���ƽ�������ƶ���Bѡ�NH4HSΪ���壬�ʲ���ʹƽ���ƶ���Cѡ������ݻ����䣬ԭƽ���и����ʵ�Ũ��û�仯���ʲ������ƶ���Dѡ����벻�μӷ�Ӧ��N2���Һ�ѹ�����������Ũ�ȼ�С����ƽ�ⷢ���ƶ�����ѡBC��
�����Ѷȣ�һ��
3��ѡ���� �ܹ�˵��H2(g)��I2(g) 2HI(g)(HIΪ��ɫ����)�Ѵ�ƽ��״̬����(? )
2HI(g)(HIΪ��ɫ����)�Ѵ�ƽ��״̬����(? )
A��һ��H��H�����ѵ�ͬʱ������H��I���γ�
B��v (H2)���� v (HI) ��ʱ��״̬
C�����º���ʱ����Ӧ��������������ֲ����״̬
D�����º���ʱ����ϵ����ɫ���ٷ����仯��״̬
�ο��𰸣�D
���������A �����ڷ�Ӧ���κ�һ��ʱ����һ��H��H�����ѵ�ͬʱ������H��I���γɣ�B����v (H2)���� v (HI) ��ʱ��״̬Ϊ��Ӧ��һ�������ʱ������ƽ��״̬��C�����º���ʱ�����ڷ�Ӧ���κ�һ��ʱ���Ƿ�Ӧ��������������ֲ����״̬��D��ȷ��
���������⿼���˻�ѧƽ�⣬�Ǹ߿�������ȵ㣬����Ƚϼ�
�����Ѷȣ�һ��
4��ѡ���� ��2 L���ܱ������з�����ӦxA(g)��yB(g) zC(g)��ͼ�ױ�ʾ200 ��ʱ������A��B��C���ʵ�����ʱ��ı仯��ͼ�ұ�ʾ��ͬ�¶���ƽ��ʱC�������������ʼn(A)��n(B)�ı仯��ϵ�������н�����ȷ����
zC(g)��ͼ�ױ�ʾ200 ��ʱ������A��B��C���ʵ�����ʱ��ı仯��ͼ�ұ�ʾ��ͬ�¶���ƽ��ʱC�������������ʼn(A)��n(B)�ı仯��ϵ�������н�����ȷ����
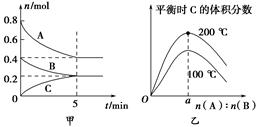
A��200 ��ʱ����Ӧ�ӿ�ʼ��ƽ���ƽ������v(B)��0.04 mol��L��1��min��1
B��200��ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ25 L2/mol2
C�������������200�潵�µ�100�棬ԭƽ��һ�����ƻ��������淴Ӧ���ʾ�����
D����ͼ�ҿ�֪����ӦxA(g)��yB(g) zC(g)�Ħ�H<0����a��2
zC(g)�Ħ�H<0����a��2
�ο��𰸣�B
���������A��200 ��ʱ����Ӧ�ӿ�ʼ��ƽ��B��Ũ�ȼ���0.2mol/2L=0.1mol/L������ƽ������v(B)��0.1mol/L/5min=0.02mol��L��1��min��1,����B������ͼ�����ݿ�֪�÷�Ӧ�Ļ�ѧ����ʽΪ2A(g)��B(g) C(g)��200��ʱ��A��B��C��ƽ��Ũ�ȷֱ���0.2mol/L��0.1mol/L��0.1mol/L�����ݻ�ѧƽ�ⳣ���Ķ����K=0.1mol/L/0.1mol/L��(0.2mol/L)2="25" L2/mol2����ȷ��C�������������200�潵�µ�100�棬ԭƽ��һ�����ƻ��������淴Ӧ���ʾ���С������D����ͼ�ҿ�֪�¶����ߣ�C�������������˵�������¶ȣ�ƽ�������ƶ�������Ϊ���ȷ�Ӧ����H>0��aֵ��ȷ��������ѡB��
C(g)��200��ʱ��A��B��C��ƽ��Ũ�ȷֱ���0.2mol/L��0.1mol/L��0.1mol/L�����ݻ�ѧƽ�ⳣ���Ķ����K=0.1mol/L/0.1mol/L��(0.2mol/L)2="25" L2/mol2����ȷ��C�������������200�潵�µ�100�棬ԭƽ��һ�����ƻ��������淴Ӧ���ʾ���С������D����ͼ�ҿ�֪�¶����ߣ�C�������������˵�������¶ȣ�ƽ�������ƶ�������Ϊ���ȷ�Ӧ����H>0��aֵ��ȷ��������ѡB��
�����Ѷȣ�һ��
5��ѡ���� �ظ������Һ�д�������ƽ�⣺Cr2O72-(�Ⱥ�ɫ)+H2O  2H++2CrO42-(��ɫ)����K2Cr2O7��Һ�м������������Լ�����Һ��ɫ��ӻ�ɫ��Ϊ�Ⱥ�ɫ
2H++2CrO42-(��ɫ)����K2Cr2O7��Һ�м������������Լ�����Һ��ɫ��ӻ�ɫ��Ϊ�Ⱥ�ɫ
A��NaHSO4
B��NaHCO3
C��Na2CO3
D��CH3COONa
�ο��𰸣�A
�����������Һ�ӻ�ɫ��Ϊ�Ⱥ�ɫ����Ӧ������С�A��HSO4�C�Ƕ�Ԫǿ���������ˮ��Һ��ˮ�������ϴ�HSO4-=H++SO42-��ʹ��Һ��H+Ũ������Cr2O72-(�Ⱥ�ɫ)+H2O  2H++2CrO42-(��ɫ)���淴Ӧ������У�����Һ��Ϊ�Ⱥ�ɫ��B��HCO3-����Һ�в���ˮ��HCO3-+H2O
2H++2CrO42-(��ɫ)���淴Ӧ������У�����Һ��Ϊ�Ⱥ�ɫ��B��HCO3-����Һ�в���ˮ��HCO3-+H2O H2CO3+OH-,H2O
H2CO3+OH-,H2O H++OH-��C��CO32-��ˮ��Һ�в���ˮ�⣬��Һ��CO32-+H2O
H++OH-��C��CO32-��ˮ��Һ�в���ˮ�⣬��Һ��CO32-+H2O  HCO3?+OH-,H++OH-?
HCO3?+OH-,H++OH-? H2O����Ӧ������У�D��CH3COO-+H+
H2O����Ӧ������У�D��CH3COO-+H+ CH3COOH����Ӧ������С�
CH3COOH����Ӧ������С�
�����Ѷȣ�һ��