微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某一个元素质量数是51,中子数是28,其基态原子未成对电子数为
A.4
B.1
C.2
D.3
参考答案:D
本题解析:因为质子数+中子数=质量数,所以某一个元素质量数是51,中子数是28,则其质子数=51-28=23。又因为质子数=核外电子数,所以根据构造原理可知,其核外电子排布是1s22s22p63s23p63d34s2,因此其基态原子未成对电子数为3个,答案选D。
本题难度:简单
2、选择题 下列叙述中,正确的是( )
A.一个基态多电子的原子中,可以有运动状态完全相同的电子
B.元素原子的最外层电子数等于元素的最高正价
C.凡是中心原子采取SP3杂化轨道成键的分子其立体构型都是正四面体
D.电子构型为[Ar]3d54s2的元素是过渡元素
参考答案:D
本题解析:A项:在多电子的原子中,电子填充在不同的能层,能层又分不同的能级,同一能级又有不同的原子轨道,每个轨道中最多可以填充两个电子,自旋相反,在一个基态多电子的原子中,不可能有两个运动状态完全相同的电子,故错;B项:主族元素,除氧和氟外,最外层电子数等于它的最高化合价,故错;C项:如果4个sp3杂化轨道的成键情况一样,就是正四面体型的,如甲烷分子、四氯化碳分子。但对于一氯甲烷这样的4个杂化轨道成键情况不同的分子(一个sp3杂化轨道与Cl成键,三个与H成键),会偏离正四面体,故错。故选D。
点评:本题考查核外电子排布规律与运动状态,难度不大,注意理解核外电子的运动状态的描述。
本题难度:一般
3、选择题 下列各组顺序的排列不正确的是 (? )
A.原子半径:Na<Mg<Al
B.热稳定性:HCl>H2S>PH3
C.酸性强弱:H2SiO4<H2CO3<H2SO4
D.沸点:H2O>H2Se>H2S
参考答案:A
本题解析:同周期自左向右,原子半径逐渐减小,则选项A不正确,应该是原子半径:Na>Mg>Al。根据元素周期律可知,选项B、C都是正确的。D中水分子间存在氢键,沸点最高,正确,答案选A。
点评:该题中等难度的试题,试题基础性强,注重考查学生对元素周期律了解掌握程度,有利于培养学生的逻辑推理能力,提高学生分析问题、解决问题的能力。该题需要注意的选项D中氢键对熔沸点的影响。
本题难度:一般
4、选择题  He可以作为核聚变材料。下列关于
He可以作为核聚变材料。下列关于 He的叙述中,正确的是(? )
He的叙述中,正确的是(? )
A.质子数为2
B.电子数为3
C.中子数为2
D.质量数为2
参考答案:A
本题解析:在表示原子组成时元素符号的左下角表示质子数,左上角表示质量数,所以选项A正确;又因为中子数+质子数=质量数,核外电子数=质子数,所以该微粒的电子数是2,中子数是1,即选项BCD都是错误的,答案选D。
点评:该题是基础性试题的考查,主要是考查学生对原子组成以及同位素判断的熟悉了解程度,意在培养学生灵活运用基础知识解决实际问题有的能力,难度不大。该题的关键是明确原子的组成微粒,以及有关微粒之间的数量关系,并能灵活运用即可
本题难度:简单
5、填空题 a、b、c、d是四种短周期元素,a、b、c同周期,c、d同主族。a的原子结构示意图为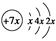 ,b与d形成的化合物的电子式为
,b与d形成的化合物的电子式为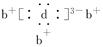 ,则下列叙述中正确的是
,则下列叙述中正确的是
( )。
A.原子序数:a>b>c
B.d单质最活泼
C.原子半径:a>c>d
D.最高价氧化物对应的水化物的酸性:d>a>c
参考答案:C
本题解析:根据核外电子排布规律知,x=2,a为Si,由b、d形成的化合物的电子式可知b为Na,d为N,c、d同主族,则c为P。原子序数:c>a>b,A错误;N2中含有N≡N键,性质很稳定,B错误;原子半径:a>c>d,C正确;最高价氧化物对应的水化物的酸性:d>c>a,D错误。
本题难度:一般