微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关钢材生锈的说法正确的是
A.红色铁锈的主要成分是Fe(OH)3
B.钢材在空气中的反应只有氧化反应、还原反应及化合反应
C.钢材在空气中的腐蚀主要为电化学腐蚀,其负极的反应为:Fe-3e-=Fe3+
D.空气中阳光、雨水、湿度对钢材的腐蚀有较大影响
参考答案:D
本题解析:A项,红色铁锈的主要成分是Fe3O4,;B项,钢铁在空气中生锈过程中会有Fe(OH)3进一步部分脱水形成疏松的Fe2O3・xH2O(x取值是任意正实数,一般不会超过1),属于分解反应;C项,其负极的反应为:Fe-2e-="==" Fe2+;D项正确。
本题难度:简单
2、选择题 下列叙述中,正确的是( )
①汽车尾气中的氮氧化物与光化学烟雾的形成有关
②大量燃烧含硫燃料是形成酸雨的主要原因
③棉、麻、丝、毛及合成纤维完全燃烧都只生成CO2和H2O
④减少CO2排放,可遏制全球气候变暖
⑤纯铁比碳素钢易生锈.
A.①③⑤
B.①②④
C.②④⑤
D.②③④
参考答案:①以一氧化氮和二氧化氮为主的氮氧化物是形成光化学烟雾和酸雨的一个重要原因.汽车尾气中的氮氧化物与氮氢化合物经紫外线照射发生反应形成的有毒烟雾,称为光化学烟雾.汽车尾气中的氮氧化物与光化学烟雾的形成有关,故①正确;
②酸性气体溶解于雨水中,降落到地面上,形成酸雨.所谓的酸性气体主要是硫氧化物和氮氧化物,它们主要是人类化石燃料(煤、天然气)的燃烧生成的,故②正确;
③棉麻是植物纤维,只含有C、H、O元素;丝毛是蛋白纤维,蛋白质由C、H、O、N元素组成,还可能含有S、P等,N、S、P燃烧是会生成其各自的氧化物,合成纤维种类可就多了,主要看其合成的单体组成了,合成纤维氨纶、氯纶、腈纶、醋酯纤维等等,顾名思义,肯定是含有其他元素存在,故③错误;
④人们焚烧化石矿物或砍伐森林并将其焚烧时产生的二氧化碳等多种温室气体,由于这些温室气体对来自太阳辐射的可见光具有高度的透过性,而对地球反射出来的长波辐射具有高度的吸收性,能强烈吸收地面辐射中的红外线,也就是常说的“温室效应”,导致全球气候变暖,故④正确;
⑤碳素钢中铁与极微小的碳形成了原电池,发生电化腐蚀,原电池反应速率远高于纯铁的化学腐蚀,碳素钢比纯铁易生锈,故⑤错误;
综上所述:①②④正确
故选B.
本题解析:
本题难度:一般
3、选择题 如图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,则下列叙述中正确的是
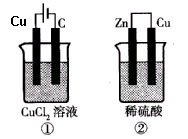
A.产生气体的体积:①>②
B.溶液的pH变化:①不变②增大
C.①和②中铜电极均失电子
D.电极反应式:①中阳极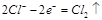 ②中负极
②中负极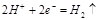
参考答案:B
本题解析:根据装置可判断,①是电解池,②是原电池。①中铜和电源的正极相连,作阳极失去电子。碳棒是阴极,溶液中的铜离子得到电子而析出。②中锌是负极,失去电子。铜是正极,溶液中的氢离子得到电子,生成氢气。所以A、C、D都是不正确的,选项B正确,答案选B。
本题难度:一般
4、选择题 分别放置在如图所示装置(都盛有0.1mol・L-1的H2SO4溶液)中的四个相同的纯锌片,腐蚀最慢的是
[? ]
A.
B.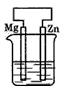
C.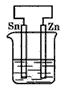
D.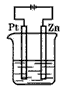
参考答案:D
本题解析:
本题难度:一般
5、选择题 在能源和环保的压力下,新能源电动汽车无疑将成为未来汽车的发展方向。如果电动汽车上使用新型钒电池,一次性充电3―5分钟后,续航能力可达1000公里;而成本造价只有目前锂电池的40%,体积和重量分别是锂电池的1/25和1/10。全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图所示:
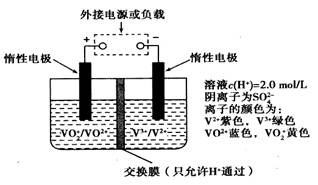
下列有关该钒电池的说法不正确的是:
A.该电池为可逆电池, 当左槽溶液逐渐由黄变蓝时,为充电过程,此时左槽溶液pH值升高
B.放电过程中,右槽溶液中溶液颜色由紫色变为绿色
C.充电过程中, H+可以通过质子交换膜向右移动,形成电流通路,并且参与电极反应
D.充电时若转移的电子数为3.01 1023个,左槽溶液中n(H+)增加了0.5mol
1023个,左槽溶液中n(H+)增加了0.5mol
参考答案:A
本题解析:A、根据装置图可知,当左槽溶液逐渐由黄变蓝,即VO2+转化为VO2+,V元素的化合价从+5价降低到+4价,此时该极上发生得电子的还原反应,其电极反应式为VO2++2H++e-=VO2++H2O,但该该过程是放电过程,故A不正确;B、放电过程中右槽是负极失去电子发生氧化反应,电极反应式为V2+-e-=V3+,所以放电过程中,右槽溶液中溶液颜色由紫色变为绿色,B正确;C、充电过程中右槽发生还原反应,电极反应式为V3++e-=V2+,因此为保持溶液的电中性,充电过程中, H+可以通过质子交换膜向右移动,形成电流通路,并且参与电极反应,C正确;D、充电时,左槽发生的反应为VO2++H2O-e-=VO2++2H+,当转移电子为3.01×1023个即为0.5mol电子时,生成氢离子为1mol,此时氢离子参与正极反应,通过交换膜定向移动使电流通过溶液,溶液中离子的定向移动可形成电流,通过0.5mol电子,则左槽溶液中n(H+)的变化量为1mol-0.5mol=0.5mol,故D正确,答案选A。
本题难度:一般