微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、推断题 有A、B、C、D、E、F、G、H、I九种常见物质,它们的转化关系(反应条件未注明)如图所示。其中B、C、D为单质,常温下D为固态,B、C、E、G为气态,F为淡黄色粉末,I的焰色反应为黄色。

请回答:
(1)写出F的电子式_________ ,其化学键类型有__________ 。
(2)写出反应⑤的化学方程式_____________________________。
(3)I的是溶液呈____性(填酸性、中性或碱性),原因(用离子反应方程式表示)_____________ 。
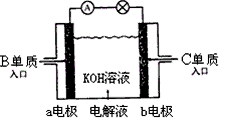
(4)B、C单质已被应用于字宙飞船的燃料电池中,如下图所示,两个电极均由多孔性碳构成,通入的两种单质由孔隙逸出并在电极表面放电。b是电池的_______ 极;a电极上的电极反应式是____________ 。
(5)在①、②、③、④、⑤五个反应中,△H>0的反应是__________(填序号)。
(6)在标准状况下,若将11.2L气体G通入350mL 2mol/L的H溶液中,反应后溶液中离子浓度由大到小的顺序是____________ 。
参考答案:(1)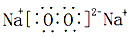 ;离子键和共价键
;离子键和共价键
(2)2Na2O2+2H2O ==4NaOH+O2↑
(3)碱?; CO32-+H2O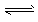 HCO3-+OH-
HCO3-+OH-
(4)正极; H2+2OH--2e-==2H2O
(5)①④
(6)c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
本题解析:
本题难度:困难
2、填空题 V、W、X、Y、Z是五种常见元素,其中V、W、X、Y四种短周期元素在周期表中的位置如下图所示:V、W的最简单气态氢化物M、N混合时有白烟生成,M能使湿润的pH试纸变蓝。Z是人体血红蛋白中存在的金属元素。请填写下列空白:

(1)W的原子结构示意图为?;
(2)二氧化钛(TiO2)与X的单质、Y的单质高温下反应生成两种化合物,这两种化合物均由两种元素组成。其反应的化学方程式为?;
(3)含X元素的一种化合物A与Y的最高价氧化物C之间有如下的反应关系:

若E为白色沉淀,则E物质的化学式为?;
(4)常温下,相同浓度 X、Z简单离子的溶液中滴加NaOH溶液,X、Z两元素先后沉淀,X(OH)n完全沉淀的pH是4.7,Z(OH)n完全沉淀的pH是2.8,则Ksp[X(OH)n]?(填“>”或 “<”) Ksp[Z(OH)n];
(5)Y与氢能形成多种化合物,其中一种为Y2H2。2.00g Y2H2完全燃烧生成液态水和二氧化碳,放出99.6kJ热量,写出Y2H2燃烧的热化学反应方程式________________________________________________________;
(6)同温同压下,将a L M气体和b LN气体通入水中,若所得溶液的pH=7,则a?b(填“>"或“<”或“=”)。
参考答案:(15分)(1) 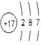 ?(2分)
?(2分)
(2)4Al? + 3 TiO2? +3C 2 Al2O3+3TiC? (3分)?
2 Al2O3+3TiC? (3分)?
(3)Al(OH)3?(2分)
(4)>(2分)
( 5)2C2H2 (g)+5O2(g) ==4CO2(g)+2H2O(l)?△H=-2589.6kJ/mol (3分)
(6) >(3分)
本题解析:(1)由题意可知,V、W、X、Y分别为氮、氯、铝、碳,M、N分别是氨气和氯化氢,Z是铁,氯原子核电荷数为+17,核外电子层结构为287;(2)铝由0价升为+3价,碳由0价将为―4价,由电子、原子守恒配平,该氧化还原反应方程式为4Al+3TiO2+3C 2Al2O3+3TiC;(3)碳酸的酸性比氢氧化铝强,由题意可知,该反应式为NaAlO2+CO2+2H2O==Al(OH)3↓+NaHCO3;(4)由题意可知,优先生成溶解度较小的沉淀,则Ksp[X(OH)n]>Ksp[Z(OH)n];(5)由m/M可知,n(C2H2)=1/13mol,由题意可知,1/13C2H2(g)+5/26O2(g)==2/13CO2(g)+1/13H2O(l)?△H=―99.6kJ?mol―1,或2C2H2 (g)+5O2(g) ==4CO2(g)+2H2O(l)?△H=-2589.6kJ/mol;(6)若a=b,则NH3与HCl恰好反应生成NH4Cl,NH4Cl中NH4+水解导致所得溶液呈酸性,要使所得溶液的pH=7,则氨气一定过量,得到氨水和氯化铵的混合溶液,则a>b。
2Al2O3+3TiC;(3)碳酸的酸性比氢氧化铝强,由题意可知,该反应式为NaAlO2+CO2+2H2O==Al(OH)3↓+NaHCO3;(4)由题意可知,优先生成溶解度较小的沉淀,则Ksp[X(OH)n]>Ksp[Z(OH)n];(5)由m/M可知,n(C2H2)=1/13mol,由题意可知,1/13C2H2(g)+5/26O2(g)==2/13CO2(g)+1/13H2O(l)?△H=―99.6kJ?mol―1,或2C2H2 (g)+5O2(g) ==4CO2(g)+2H2O(l)?△H=-2589.6kJ/mol;(6)若a=b,则NH3与HCl恰好反应生成NH4Cl,NH4Cl中NH4+水解导致所得溶液呈酸性,要使所得溶液的pH=7,则氨气一定过量,得到氨水和氯化铵的混合溶液,则a>b。
本题难度:一般
3、推断题 下图中,A是一种无色液体,G是极易溶于水的碱性气体,Y是胃酸的主要成分,K是不溶于稀硝酸的白色沉淀,反应⑤是工业制X的主要反应之一。
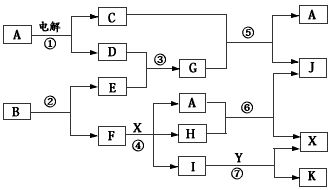
请按要求填空:
(1)写出下列物质的化学式:A:__________,E:__________F:__________,Y:__________。
(2)反应⑤的化学方程式为:____________________。
(3)1molB通过反应②得到1molF,B中F的质量分数为72%,则B的化学式为:__________。
参考答案:(1)H2O;N2;Ag;HCl
(2)4NH3+5O2 4NO+6H2O
4NO+6H2O
(3)AgN3
本题解析:
本题难度:一般
4、填空题 (8分)已知A、B、C、D组成的元素都属于短周期,它们之间的简单转化关系如图所示。

请按要求写出有关反应的化学方程式:
(1)若其中A、D为单质且同主族,B、C为氧化物: (该反应在工业上 有重要用途)?。
(2)若A、D为常态下的气体单质且不同主族,B、C为化合物且B为水:?。
(3)若A、B、C均为化合物且C为水,单质D常态下为固体:?。
(4) 若A、D为固体单质且不同主族,B、C为氧化物:?。
参考答案:(共8分)
(1)2C+SiO22CO↑+Si(2分)
(2)2F2+2H2O===4HF+O2(2分)或2Cl2+2H2O4HCl+O2
(3)SO2+2H2S===3S+2H2O(2分)
(4)2Mg+CO22MgO+C(2分)
本题解析:略
本题难度:一般
5、选择题 A~D是含有同一元素的四种物质,相互之间有如图所示的转化关系,其中A既可为单质.又可为气态氢化物,D是最高价氧化物的水化物,则A、B、C、D中共同含有的元素是( )
A.氯
B.铁
C.碳
D.氮