��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ����ʡ�����ؿ���ḻ������ˮ����Ʒ���������⣬��ʯ������ʯ�ȿ�ʯ������Ʒλ�ߣ�����ص��ͻ𡢱��¸��Ȳ��ϣ���Ҫ�ɷ�ΪMgO��Al2O3����ҵҲ�Ϸ��
ij��ѧ��ѧ̽��С��ͨ������������ϣ�����ʯ����ɽ�����ʵ��̽����
I��������ϣ�����ʯ�ijɷֿɿ�������MgO��Fe2O3��Al2O3��SiO2���
���������↑ʼ������������ȫʱ��pH
| �������� | Fe��OH��3 | Mg��OH��2 | Al��OH��3
������pH��Χ
1.5-4.1
9.4-12.4
3.3-5.2
|
�����ʵ�飺

��ʵ�����ݣ�
�ٿ�ʯ��Ʒ����Ϊ��8.22g?��ÿ��ת�����ù���ɷ�ֻ��һ��
��������������ݺ���ѧ��ѧ֪ʶ�ش���������
��1��д����D��һ�ֺ�ɫ���ϵĻ�ѧ����ʽ��______
��2����ҵ�ϵ��ͻ����ͨ����F����ҺE��һ��ת�����ɣ����������ҺE�п��ܺ��гɷ֣����һ������ҺE��ȡ�ͻ���ϵ�ʵ�鷽����______
��3����ҺB��NaOH��Һ��Ӧʱ��Ӧ������Һ��pH��7-8֮�䣬������Ϊ��______
��4��ͨ�����㣬д�������������ʽ��ʾ��ʯ��ɵĻ�ѧʽ______��
�ο��𰸣���ʯ�ijɷֿɿ�������MgO��Fe2O3��Al2O3��SiO2��ÿ��ת�����ù���ɷ�ֻ��һ�֣��ɹ�������ͼ��֪����AΪSiO2����ҺB�����Ȼ�þ���Ȼ������Ȼ����ȣ���ҺB��������������Һ��������������������þ������������ʼ������������ȫʱ��pHֵ��֪������DΪ������������ҺC�����Ȼ�þ��ƫ�����ơ��Ȼ��ƣ���ҺCͨ�������̼����֪����FΪ������������ҺE�����Ȼ�þ���Ȼ��Ƶȣ�
��1��DΪ�����������Լ��ȷֽ��Ʊ���������ɫ���ϣ���Ӧ����ʽΪ2Fe��OH��3?��?.?Fe2O3+3H2O��
�ʴ�Ϊ��2Fe��OH��3?��?.?Fe2O3+3H2O��
��2����ҺE�����Ȼ�þ���Ȼ��Ƶȣ������õ���ҺE�м���������NaOH��Һ���ٽ��й��ˡ�ϴ�ӡ������������þ�����������и�������������þ������������þ����ȡ�ͻ���ϣ�
�ʴ�Ϊ�������õ���ҺE�м���������NaOH��Һ���ٽ��й��ˡ�ϴ�ӡ���������и������գ�
��3�����ݱ������ݣ�������Һ��pH��7��8֮�䣬Mg2+û�б仯��Al3+ת��ΪAlO2-��ֻ��Fe3+��������֤����ֻ��Fe��OH��3��
�ʴ�Ϊ�����ݱ������ݣ�������Һ��pH��7��8֮�䣬Mg2+û�б仯��Al3+ת��ΪAlO2-��ֻ��Fe3+��������֤����ֻ��Fe��OH��3��
��4������AΪSiO2����Ϊ2.4g�����ʵ���Ϊ2.4g60g/mol=0.04mol��
DΪ��������������Ϊ2.14g�����ʵ���Ϊ2.14g107g/mol=0.02mol��������Ԫ���غ��֪���������ʵ���Ϊ0.01mol������Ϊ0.01mol��160g/mol=1.6g��
FΪ��������������Ϊ1.56g�����ʵ���Ϊ1.56g78g/mol=0.02mol��������Ԫ���غ��֪���������ʵ���Ϊ0.01mol������Ϊ0.01mol��102g/mol=1.02g��
������þ������Ϊ8.22g-2.4g-1.6g-1.02g=3.2g�����ʵ���Ϊ3.2g40g/mol=0.08mol��
����n��MgO����n��Al2O3����n��Fe2O3����n��SiO2?��=0.04mol��0.01mol��0.01mol��0.02mol=4��1��1��2��
���������������ʽ��ʾ��ʯ��ɵĻ�ѧʽΪ8MgO?Al2O3?Fe2O3?4SiO2��
�ʴ�Ϊ��8MgO?Al2O3?Fe2O3?4SiO2��
���������
�����Ѷȣ�һ��
2��ѡ���� Ҫ��ȥFeCl2�к��е�Fe3+��Cu2+��H+��Ӧѡ����Լ��ǣ�?��
A������
B��NaOH
C������
D����ˮ
�ο��𰸣�C
������������ۿɽ������ӻ�ԭΪ�������ӡ�ͭ���ӻ�ԭΪͭ���ʡ������ӻ�ԭΪ������ȥ��������������Ϊ�������ӣ���������µ��������ӡ�
�����Ѷȣ�һ��
3��ʵ���� ij�о���ѧϰС�����о���Fe2+�Ʊ�Fe(OH)2�� �����У����������ʵ�鷽����
�����У����������ʵ�鷽����
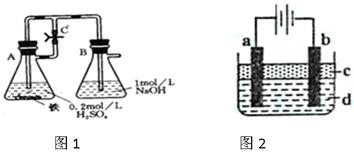
����һ������ͼ1����ʵ�飬����A�еķ�Ӧ��ʼʱ�����ɼ�C���ڴ�״̬��һ��ʱ��رյ��ɼ�C������A�еķ�Ӧ���ڽ��С�������_______�����й۲쵽��ɫ��������ʵ�����漰���Ļ�ѧ����ʽ�У�?
����������ͼ2����ʵ�飬���������������Һ�����ȹ۲쵽��ɫ������������ṩ���Լ���缫������ѡ����ȷ��������ں����ϣ�
�ٴ�ˮ?��NaCl��Һ?��NaOH��Һ?�����Ȼ�̼?��CuCl2��Һ?���Ҵ�?��Fe��?��ֲ����?��̼��
aΪ___________��bΪ___________��cΪ___________��dΪ___________��(�����)
�ο��𰸣����� һ��B��Fe+H2SO4=FeSO4+H2����FeSO4+2NaOH=Fe(OH)2��+Na2SO4��
һ��B��Fe+H2SO4=FeSO4+H2����FeSO4+2NaOH=Fe(OH)2��+Na2SO4��
H2SO4+2NaOH=Na2SO4��2H2O ���кͷ�Ӧ����ʽ��д���۷֣�
���������ߡ����ߡ��ࡢ��
�����������
�����Ѷȣ�һ��
4��ѡ���� ���и������ʷ�Ӧ���ٵ���KSCN��Һ���Ժ�ɫ����
A����������ϡ����
B��FeCl2��Һ����ˮ
C����������CuCl2��Һ
D����������FeCl3��Һ
�ο��𰸣�B
���������
��ȷ�𰸣�B
A��Fe��2HCl=FeCl2��H2����Fe3�� ������
B. FeCl2��Һ����ˮ��2Fe2����Cl2=2Fe3����2Cl�D��Fe3������
C.��������CuCl2��Һ��Fe��Cu2��=Fe2��Cu��Fe3�� ������
D.��������FeCl3��Һ?��2Fe3����Fe=3Fe2��?��Fe3�� ������
�����Ѷȣ���
5��ʵ���� (10��) ��������������Ԫ�أ�����ȱ����ƶѪ�ij��������Ƿ��ò���ҩ��������ơ�����Ҫ�ɷ֣��������������ʰ���ɫ�����г���һ�ֳ����IJ���ҩ���ҩƷ������ˮ�������������е�θ�ᡣijͬѧΪ�˼�⡰�����ơ�ҩƬ��Fe2+�Ĵ��ڣ���Ʋ�����������ʵ�飺

���Լ�1��?��
�Ƽ���KSCN��Һ����δ��������ˮ������£���Һ��Ҳ�����˺�ɫ������ܵ�ԭ����?��
����ʵ���з��ַ���һ��ʱ�䣬��Һ����ɫ������ȥ��Ϊ�˽�һ��̽����Һ��ɫ��ԭ�ס��ҡ�����λͬѧ���Ƚ����˲��룺
���
| ��?��
|
��
| ��Һ�е�+3��Fe�ֱ���ԭΪ+2��Fe
|
��
| ��Һ�е�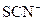 ����������ˮ���� ����������ˮ����
|
��
| ���Ƶ���ˮ����Ư���ԣ�������ҺƯ��
|
������ͬѧ�IJ��룬�����ʵ�鷽������֤��ͬѧ�IJ����Ƿ���ȷ��д���йص�ʵ�������Ԥ������ͽ��ۡ�����һ��������Ҳ���Բ��䣩
����һͬѧΪ�˼�⡰�����ơ�ҩƬ�����ĺ�������Ʋ�����������ʵ�飺
��ȡ�������飬����ȡ2.0g������������ᣬ����ʹ����ȫ�ܽ⣻
����������Һ���ȼ�������H2O2��Һ���ټ���������ˮ����ַ�Ӧ����˲�ϴ�ӳ�����
�۽����ù������������أ���0.8g����ɫ���塣
�ܼ��㣺�������ơ�ҩƬ��������������Ϊ?��
�ο��𰸣�(10��)
��ϡ���ᣨ��ϡ������Һ����2�֣�
��Fe2+������������������Fe3+����2�֣�
�ǣ�4�֣�
���
ʵ�����
Ԥ������ͽ���
��
ȡ������ɫ����Һ������KSCN��Һ
�����Һ���ɫ��˵����ͬѧ�IJ����Ǻ����ģ������Һ�����ɫ��˵����ͬѧ�IJ����Dz�������
��
ȡ������ɫ����Һ���� ��FeCl3��Һ
��FeCl3��Һ
�����Һ�Բ����ɫ��˵����ͬѧ�IJ����Ǻ����ģ������Һ���ɫ��˵����ͬѧ�IJ����Dz�������
�����������
�����Ѷȣ���