微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3e-=NO↑+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出该氧化还原反应的化学方程式:________。
(2)反应中硝酸体现了________、________。
(3)反应中若产生标准状况下11.2L气体,则转移电子的物质的量是________ mol。
(4)现称取含有杂质的甲样品(杂质与酸不反应)5.4 g,恰好与100 mL 1.4 mol・L-1的硝酸溶液完全反应,则该样品的纯度为________。
(5)若1 mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是________。
参考答案:(1)14HNO3+3Cu2O=6Cu(NO3)2+2NO↑+7H2O
(2)酸性;氧化性
(3)1.5
(4)80%
(5)使用了较浓的硝酸,产物中有NO2生成
本题解析:(1)由于NO3-+4H++3e-=NO↑+2H2O是还原过程,需要加入还原剂才能发生,而KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中具有较强还原性的只有Cu2O,Cu2O被氧化生成Cu2+,化学方程式为:14HNO3+3Cu2O=6Cu(NO3)2+2NO↑+7H2O;(2)硝酸在反应中体现了酸性和氧化性;(3)依据反应式:NO3-+4H++3e-=NO↑+2H2O,若产生标准状况下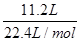 =0.5 mol气体,则转移电子的物质的量是0.5 mol×3=1.5 mol;(4)设5.4 g样品中含甲的物质的量为x,由化学方程式可得:
=0.5 mol气体,则转移电子的物质的量是0.5 mol×3=1.5 mol;(4)设5.4 g样品中含甲的物质的量为x,由化学方程式可得: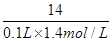 =
=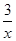 ,解得x=0.03 mol,则样品中甲的质量分数为
,解得x=0.03 mol,则样品中甲的质量分数为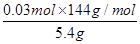 ×100%=80%;(5)若1 mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,则硝酸的还原产物的价态应比NO中氮元素的价态高,依据浓硝酸反应的规律知,应是使用了较浓的硝酸,产物中有NO2生成。
×100%=80%;(5)若1 mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,则硝酸的还原产物的价态应比NO中氮元素的价态高,依据浓硝酸反应的规律知,应是使用了较浓的硝酸,产物中有NO2生成。
本题难度:简单
2、选择题 在3Cl2+6KOH = 5KCl+3KClO3+3H2O反应中,还原产物是
[? ]
A.KClO3
B.KCl
C.H2O
D.KCl + H2O
参考答案:B
本题解析:
解析:
选项A.KClO3 为化合价升高后的产物,为氧化产物,故错;
选项B.KCl 为化合价降低后的产物,为还原产物,故正确;
选项C.H2O既不是氧化产物也不是还原产物,故错;
选项D.KCl为还原产物,?H2O既不是氧化产物也不是还原产物,故错。
故选:B
本题难度:简单
3、选择题 亚硝酸(HNO2)既可作氧化剂又可作还原剂,当它在反应中作氧化剂时,可能生成的产物是
[? ]
A.N2
B.N2O3
C.NH3
D.NO2
参考答案:AC
本题解析:解析:
氧化剂时生成的产物是指化合价降低之后的生成物,HNO2中氮元素为+3价,A、C选项中氮元素的价态均低于+3价,可能为HNO2作氧化剂时,可能生成的产物是,B、D选项中氮元素的价态均高于+3价,不可能为HNO2作氧化剂时生成的产物。故事故A、C正确,B、D错。
故选:A、C
本题难度:简单
4、填空题 下列4组物质均有一种物质的类别与其它3种不同
A.CaO、Na2O、CO2、CuO
B.H2、C、P、Cu
C.O2、Fe、Cu、Zn
D.HCl、H2O、H2SO4、HNO3
(1)以上四组物质中与别不同的物质依次是(填化学式)
A___________;B___________;C___________;D___________。
(2)这四种物质相互作用可生成一种新物质(碱式碳酸铜,化学式Cu2(OH)2CO3),该反应_______氧化还原反应(填“是”或“否”)。
参考答案:(1)A:CO2;B:Cu;C:O2;D:H2O
(2)是
本题解析:
本题难度:一般
5、选择题 在一定条件下,分别以高锰酸钾、氯酸钾和过氧化氢为原料制取氧气,当制得同温同压下相同体积的氧气时,三个反应中转移的电子数之比为( )
A.1:1:1
B.2:2:1
C.2:3:1
D.4:3:2
参考答案:B
本题解析:用高锰酸钾、氯酸钾制氧气,反应过程中O由-2价转化为0价,而用过氧化氢制氧气,O则由-1价转化为0价。现要制得同温同压下相同体积的O2,用过氧化氢制氧气的反应中转移的电子数是用高锰酸钾、氯酸钾制取氧气的反应中转移的电子数的一半。
本题难度:简单