微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 已知某浓度的硫酸在水中的电离方程式:
H2SO4====H++HSO-4,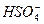
 H++
H++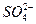 。
。
(1)Na2SO4溶液显________(填“酸性”“碱性”或“中性”),理由是(用离子方程式表示)_________。
(2)在25 ℃时0.1 mol・L-1的NaHSO4溶液中c(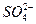 )="0.029" mol ・L-1,则25 ℃时,0.1 mol・L-1 H2SO4溶液中c(
)="0.029" mol ・L-1,则25 ℃时,0.1 mol・L-1 H2SO4溶液中c(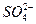 )________(填“大于”,“小于”或“等于”)0.029 mol ・L-1,理由是__________。
)________(填“大于”,“小于”或“等于”)0.029 mol ・L-1,理由是__________。
(3)在0.1 mol ・L-1 Na2SO4溶液中,下列粒子浓度关系正确的是(?)
A.c(Na+)+c(H+)=c(OH-)+c(HSO-4)+2c(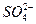 )
)
B.2c (Na+)=c(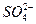 )+c(HSO-4)
)+c(HSO-4)
C.c(Na+)>c(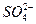 )>c (H+)>c (OH-)
)>c (H+)>c (OH-)
D.c(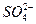 )+c(HSO-4)="0.1" mol・L-1
)+c(HSO-4)="0.1" mol・L-1
参考答案:(1)碱性?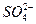 +H2O
+H2O
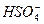 +OH-
+OH-
(2)小于? H2SO4一级电离出H+,对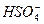 电离起抑制作用,而NaHSO4中不存在抑制作用
电离起抑制作用,而NaHSO4中不存在抑制作用
(3)AD
本题解析:本题以新型信息为前提,考查盐类水解的判断,外界因素对电离平衡的影响以及溶液离子浓度大小关系。由于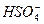 的电离是可逆的,所以
的电离是可逆的,所以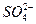 可以发生水解,Na2SO4溶液显碱性。溶液中存在的平衡体系有
可以发生水解,Na2SO4溶液显碱性。溶液中存在的平衡体系有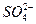 +H2O
+H2O
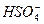 +OH-,H2O
+OH-,H2O H++OH-,溶液中各种离子浓度大小关系为:c(Na+)>c(
H++OH-,溶液中各种离子浓度大小关系为:c(Na+)>c(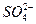 )>c (OH-)>c (
)>c (OH-)>c (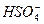 )>c(H+)。电荷守恒关系式:c(Na+)+c(H+)=c(OH-)+c(
)>c(H+)。电荷守恒关系式:c(Na+)+c(H+)=c(OH-)+c(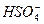 )+2c(
)+2c(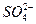 )。物料守恒关系式:c(
)。物料守恒关系式:c(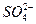 )+c(
)+c(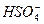 )="0.1" mol・L-1或c(Na+)=2c(
)="0.1" mol・L-1或c(Na+)=2c(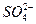 )+2c(
)+2c(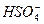 )。
)。
本题难度:简单
2、选择题 为配置NH4+的浓度与Cl-的浓度比为1:1的溶液,可在NH4Cl溶液中加入(?)
① 适量HCl?② 适量NaCl?③ 适量氨水?④ 适量NaOH
A.①②
B.③
C.③④
D.④
参考答案:B
本题解析:①②所加试剂会给溶液引入氯离子,使氯离子浓度增大.而加入④中的NaOH会与NH4+反应生成NH3・H2O,使NH4+浓度减小.所以应该选B.
本题难度:一般
3、选择题 下列事实不属于盐类水解应用的是( )
A.明矾、氯化铁晶体常用于净水
B.实验室制氢气时加CuSO4可加快反应速率
C.实验室配制FeCl3溶液时加入少量稀盐酸
D.实验室通常使用热的纯碱溶液去除油污
参考答案:B
本题解析:明矾常用于净水是因为明矾中含的铝离子发生了水解,氯化铁中由于铁离子的水解,形成了胶体所以其也可以用于净水,故A不能选;实验室制氢气时加CuSO4可加快反应速率,是因为形成了原电池,故加快了化学反应速率,故B正确,为本题的答案;实验室配制FeCl3溶液时加入少量稀盐酸,加入盐酸可以抑制铁离子的水解,故C不能选;实验室通常使用热的纯碱溶液去除油污,是因为纯碱是强碱弱酸盐,由于其水解,呈现碱性,所以可以除去油污,故D?不能选。
点评:本题考查了盐类水解,该考点是高考考查的重点和难点,本题侧重于考查该知识点的运用,该题难度中等。
本题难度:简单
4、选择题 为了使CH3COONa溶液中c(Na+)与c(CH3COO-)的比为1∶1,可以向溶液中加入下列物质中的()
A.CH3COOH晶体
B.NaOH溶液
C.KOH溶液
D.Na2CO3晶体
参考答案:A
本题解析:B、D选项中引入Na+,均会使c(Na+)增大。C项中加入KOH,可以使CH3COO-+H2O CH3COOH+OH-平衡左移,抑制CH3COO-的水解,但不能保证CH3COO-一点也不水解,只能说使c(Na+)与c(CH3COO-)之比接近1∶1,而不能是1∶1。A项中CH3COOH电离出CH3COO-,当加入CH3COOH使溶液呈中性时,即c(Na+)+c(H+)=c(CH3COO-)+c(OH-),可得到c(Na+)=c(CH3COO-)。故A正确。
CH3COOH+OH-平衡左移,抑制CH3COO-的水解,但不能保证CH3COO-一点也不水解,只能说使c(Na+)与c(CH3COO-)之比接近1∶1,而不能是1∶1。A项中CH3COOH电离出CH3COO-,当加入CH3COOH使溶液呈中性时,即c(Na+)+c(H+)=c(CH3COO-)+c(OH-),可得到c(Na+)=c(CH3COO-)。故A正确。
本题难度:简单
5、选择题 在Fe3++3H2O ?Fe(OH)3+ 3H+的平衡体系中,要使平衡向水解方向移动且使溶液的pH值增大,可采取的措施为(?)
A.加热
B.通HCl气体
C.加入FeCl3(固体)
D.加入CuO(固体)
参考答案:D
本题解析:本题为Fe3+的水解平衡,升高温度、减小浓度会使平衡右移。A加热使平衡右移H+浓度增大,pH减小;B能入HCl气体导致酸性增强,平衡左移,pH减小;C会增加Fe3+浓度,导致H+浓度增大,pH减小;D中CuO可消耗H+使平衡右移,同时pH值增大,故答案为D。
本题难度:一般