|
高中化学知识点归纳《物质的分离、提纯》试题巩固(2017年最新版)(二)
2017-03-05 13:49:20
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (8分)海藻中含有丰富的碘元素(以I-形式存在)。实验室中提取碘的流程如下:

(图一)
(1)实验操作③的名称是??,所用主要仪器名称为??。
(2)提取碘的过程中,可供选择的有机试剂是??(填序号)。
A.酒精(沸点78℃)
B.四氯化碳(沸点77℃)
C.甘油(沸点290℃)
D.苯(沸点80℃)
| (3)为使从含碘有机溶液中提取碘并回收溶剂顺利进行,采用水浴加热蒸馏(如上图一所示)。请指出图中实验装置中错误之处(有几处填几处,下列空白可不填满,也可补充)
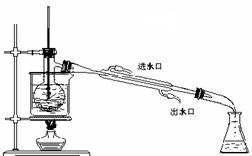
①??,②??,③???,④?,??。
(4)实验中使用水浴的原因是??,
参考答案:(8分)
(1)萃取(1分),分液漏斗(1分)?(2)BD(1分)
(3)(3分)①缺石棉网②温度计插到液体中③冷凝管进出水方向颠倒
(4) 有机溶剂沸点较低,控制温度不能过高,避免碘蒸气进入冷凝管(2分) ;
本题解析:考查物质的分离和提纯以及仪器的识别等。
(1)碘易溶再有机溶剂中,所以操作③是萃取,主要的仪器是分液漏斗。
(2)选用的萃取剂的原则:?①和原溶液中的溶剂互不相溶;?②对溶质的溶解度要远大于原溶剂,酒精和甘油与水都是互溶的,不能作为萃取剂,答案选BD。
(3)蒸馏时温度计测量的是气体的温度,所以错误之一温度计水银球的位置错误,应与蒸馏烧瓶的支管口相平;冷却水的流向和气体的流向应该是相反的,因此错误之二是冷凝水的方向错误,应为下进上出;错误之三是蒸馏烧瓶不能直接加热,需要垫石棉网、
(4)由于有机溶剂沸点较低,控制温度不能过高,避免碘蒸气进入冷凝管,因此采用水浴加热。
本题难度:简单
2、选择题 从海带中提取碘单质,成熟的工艺流程如下,下列关于海水制碘的说法,正确的是
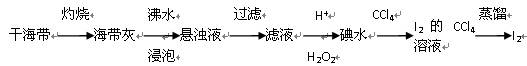
A.实验室在蒸发皿中灼烧干海带,并且用玻璃棒搅拌
B.含I―的滤液中加入稀硫酸和双氧水后,碘元素发生还原反应
C.在碘水中加入几滴淀粉溶液,溶液变蓝色
D.碘水加入CCl4得到I2的CCl4溶液,该操作为“萃取”
参考答案:CD
本题解析:略
本题难度:简单
3、填空题 某工厂用软锰矿(含MnO2约70%及Al2O3)和闪锌矿(含ZnS约80%及FeS),共同生产MnO2和Zn(干电池原料)。
已知:①A是MnSO4、ZnSO4、Fe2(SO4)3、Al2(SO4)3的混合液。
②IV中的电解反应式为MnSO4+ZnSO4+2H2O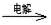 MnO2+Zn+2H2SO4。 MnO2+Zn+2H2SO4。
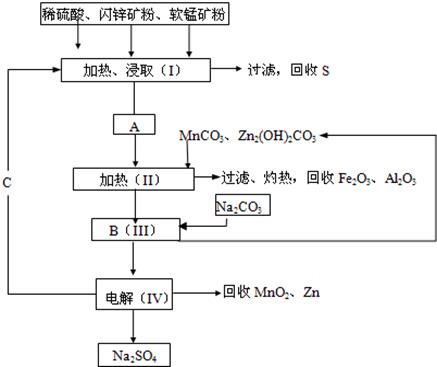
(1)A中属于还原产物的是?。
(2)MnCO3、Zn2(OH)2CO3的作用是?;Ⅱ需要加热的原因是?;C的化学式是?。
(3)Ⅲ中发生的离子方程式为?,?;
(4)如果不考虑生产中的损耗,除矿石外,需购买的化工原料是?。
参考答案:(1)MnSO4
(2)增大溶液的pH,使Fe3+和Al3+均生成沉淀;促进Fe3+、Al3+的水解;H2SO4
(3)Mn2++CO32-=MnCO3? 2Zn2++2CO32-+H2O=Zn2(OH)2CO3↓+CO2↑
(4)纯碱和硫酸
本题解析:(1)由已知信息条件知,Mn元素化合价由+4价降低为+2价,民以A中还原产物为MnSO4;
(2)由工艺流程图知,MnCO3、Zn(OH)2CO3的作用就是调节pH,使Fe3+和Al3+均生成沉淀。Fe3+、Al3+沉淀容易形成胶体,不利于氢氧化铝、氢氧化铁沉淀,所以Ⅱ加热的目的是加速沉淀生成,防止胶体出现,并使形成胶体的氢氧化铝和氢氧化铁也生成沉淀;操作Ⅰ加热、浸取需要硫酸,由②可知C为硫酸,循环利用。
(4)溶液B中含有Mn2+、Zn2+,根据流程图,加入Na2CO3后,生成MnCO3和Zn2(OH)2CO3,离子方程式是,Mn2++CO32-=MnCO3,2Zn2++2CO32-+H2O=Zn2(OH)2CO3↓+CO2↑。
本题难度:一般
4、选择题 下列叙述正确的是
A.1 mol H2O的质量为18g/mol
B.CH4的摩尔质量为16g
C.3.01×1023个SO2分子的质量为32g
D.标准状况下
E.1 mol任何物质体积均为22.4L
参考答案:C
本题解析:质量的单位是g,摩尔质量的单位是g/mol,所以选项A、B都是错误的;标准状况下,1mol任何气体的体积的体积均为22.4L,选项D不正确;根据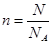 可知,选项C中SO2的物质的量是0.5mol,质量是0.5mol×64g/mol=32g,所以正确的答案选C。 可知,选项C中SO2的物质的量是0.5mol,质量是0.5mol×64g/mol=32g,所以正确的答案选C。
本题难度:困难
5、选择题 CH4中混有CH2=CH2,可将混合气通入下列物质而除去CH2=CH2的是
A.氢氧化钠溶液
B.水
C.溴水
D.浓硫酸
参考答案:C
本题解析:常温下,选项中只有溴水可吸收乙烯,答案为C
本题难度:简单
| 