微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列实验中,能获得成功的是( )
A.用高锰酸钾溶液来除去混在乙烷中的乙烯
B.苯、浓硝酸共热制硝基苯
C.用溴水除去混在苯中的己烯
D.苯、液溴、溴化铁混合制溴苯
参考答案:A.乙烯被高锰酸钾氧化为二氧化碳,引入了新的杂质,故A错误;
B.制取硝基苯需要用浓硫酸作催化剂,直接加热不反应,故B错误;
C.己烯和溴水能发生加成反应,但是加成产物仍然易溶解在苯中不能除去,故C错误;
D.苯和液溴在溴化铁催化下能发生取代反应,故D正确.
故选:D.
本题解析:
本题难度:简单
2、实验题 某待测液可能有Fe2+、Fe3+、Ag+、Ba2+、Al3+、Ca2+、NH4+等离子,进行了下述实验(所加酸、碱、NH3水、Br2水都是过量的)。
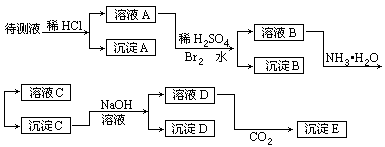
根据实验结果:
(1)判定待测液中有无Ba2+、Ca2+离子,并写出理由。答_________。
(2)写出沉淀D的分子式:_________。
(3)写出从溶液D生成沉淀E的离子反应方程式:_________。
参考答案:(1)含有Ba2+、Ca2+离子中的一种或两种,因为BaSO4不溶于水,CaSO4微溶于水
(2)Fe(OH)3
(3)AlO2-+CO2+2H2O====Al(OH)3↓+HCO3-
本题解析:沉淀A可判断为AgCl,所以Ag+已从溶液中除掉,溶液A中若含Fe2+已被溴水氧化为Fe3+。由于BaSO4难溶于水,CaSO4微溶于水,可判断沉淀B可能是二者之一,也可能是它们的混合物。
Al(OH)3,Fe(OH)3都难溶于水,沉淀C可能是二者之一,或是它们的混合物。若沉淀C中有Al(OH)3,加入过量NaOH溶液后生成NaAlO2进入溶液D,用过量NaOH溶液沉淀C后,仍剩余沉淀D,可判断沉淀D是Fe(OH)3。HAlO2是比H2CO3更弱的酸,其钠盐可被H2CO3沉淀为Al(OH)3,它就是沉淀E。
本题难度:一般
3、实验题 (14分)某学生为测定某烧碱样品中NaOH的质量分数,进行如下实验(已知该样品中含有少量Na2CO3杂质)
a.在250mL的容量瓶中定容,配制成250mL烧碱溶液。
b.用碱式滴定管量取25.00mL烧碱溶液于锥形瓶中,加入足量BaCl2溶液使Na2CO3完全转变成BaCO3后滴入几滴酚酞指示剂;
c.在天平上准确称取烧碱样品10.5g,在烧杯中用蒸馏水溶解;
d.将物质的量浓度为1.000mol/L的标准硫酸溶液装入酸式滴定管中,调节液面,记下开始时的读数然后开始滴定。
e.在锥形瓶下垫一张白纸,滴定至溶液恰好变为无色为止,记下读数。试填空:
(1)正确操作步骤的顺序是(用字母填空)_____→_____→_____→_____→_______.
(2)酸式(碱式)滴定管在使用前需进行的第一步操作是____________,中学化学实验常用仪器中使用前和滴定管使用有相同操作的不同类玻璃仪器还有?、_______。
(3)重复上述滴定操作,记录数据如下:
实验编号
| 标准溶液(H2SO4)(aq)
浓度(mol/L)
| 滴定完成时耗酸
体积V(mL)
| 待测溶液(NaOH)(aq)
体积V(mL)
|
1
| 1.000
| 11.00
| 25.00
|
2
| 1.000
| 12.04
| 25.00
|
3
| 1.000
| 12.18
| 25.00
|
①根据以上数据,可计算出该样品中NaOH的质量分数为__________(保留两位有效数字)。
②上述实验中,下列操作(其它操作正确)会造成结果偏低的有__________________。
A.a步操作中未将溶液冷却至室温就转移到容量瓶中定容。
B.c步操作中,称量药品时,砝码放在左盘,NaOH放在右盘。
C.滴定终点读数时俯视读数。
D.酸式滴定管使用前,未用标准H2SO4溶液润洗。
E.锥形瓶水洗后未干燥就直接盛待测溶液。
③有同学提出将原实验方案中的酚酞指示剂改为甲基橙指示剂,你认为是否可行?________(填“可行”或“不可行”)。如果改用甲基橙为指示剂,则测定结果如何?________(填“偏高” “偏低”或“正确”)
参考答案:(1)cabde(2分)
(2)检漏?分液漏斗?容量瓶(各1分)
(3)①92%(3分)?②C (2分)③BC(2分)④不可行?偏高(每空1分)
本题解析:(1)根据先配制溶液然后除去杂质,最后进行滴定排序;正确的操作顺序为:称量→溶解→定容→取液→除杂→滴定,所以操作步骤的顺序为:cabde ;(2)酸式(碱式)滴定管在使用前需进行的第一步操作是检查是否漏水(检漏),中学化学实验常用仪器中使用前和滴定管使用有相同操作的不同类玻璃仪器还有分液漏斗、容量瓶。(3)①分析表中数据知,实验1所用硫酸的体积偏差较大,应舍弃,滴定所用硫酸的体积应取实验2和3的平均值12.11mL。根据2c(H2SO4)V(H2SO4)=c(NaOH)V(NaOH)代入数据计算得c(NaOH)="0.97" mol/L,烧碱样品中NaOH的质量分数为:w(NaOH)=40g/mol×0.9688mol/L×0.25L/10.5g×100%=92%;②A、a步操作中未将溶液冷却至室温就转移到容量瓶中定容,会使所配NaOH溶液的浓度偏大,从而使质量分数偏高,错误;B、c步操作中,称量药品时,砝码放在左盘,NaOH放在右盘,会使所称药品的质量小于10.5?g,会使样品的质量分数偏低,正确;C、滴定终点读数时俯视读数,会使V(H2SO4)偏小,从而使样品的质量分数偏小,正确;D、酸式滴定管使用前,未用标准H2SO4溶液润洗,会使V(H2SO4)偏大,从而使样品的质量分数偏大,错误;E、锥形瓶水洗后未干燥就直接盛待测溶液,对测定结果无影响,错误,选BC;③甲基橙的变色范围3.1――4.4,达到滴定终点时,硫酸会与锥形瓶中的碳酸钡反应,造成所用硫酸的体积偏大,测定结果偏高,不可行。
本题难度:一般
4、选择题 关于某溶液所含离子检验的方法和结论正确的是
A.加入NaOH溶液,有白色沉淀生成,则原溶液一定有Al3+
B.加入AgNO3溶液有白色沉淀生成,加稀盐酸沉淀不消失,则原溶液一定有Cl-
C.加入盐酸产生能使澄清石灰水变浑浊的气体,则原溶液中可能有CO32-或SO32-
D.加入NaOH溶液并加热,产生使湿润的蓝色石蕊试纸变红的气体,则原溶液中一定含NH4+
参考答案:C
本题解析:略
本题难度:一般
5、选择题 下列试剂中,可用于硬水软化的是( )
A.明矾
B.液氯
C.漂白粉
D.磺化煤
参考答案:A.明矾溶解于水形成胶状物,能吸附不溶的杂质小颗粒沉降下来,而硬水与软水的区别是可溶性钙、镁化合物的含量不同,与不溶性杂质无关,故A错误;
B.液氯为单质,溶于水变成氯水,氯水中含有HClO,具有漂白性,能杀菌消毒,但与硬水与软水的区别是可溶性钙、镁化合物的含量不同无关,故B错误;
C.漂白粉的成分是氯化钙和次氯酸钙的混合物,漂白原理是次氯酸钙和弱酸性物质生成的次氯酸的漂白性,能杀菌消毒,但与硬水与软水的区别是可溶性钙、镁化合物的含量不同无关,故C错误;
D.磺化煤(NaR)是一种有效的离子交换剂,加入磺化煤,离子交换法中阳离子交换剂发生含H+、Na+固体与Ca2+、Mg2+离子交换,可将硬水软化,发生反应为2NaR+CaSO4→CaR2+NaSO4、2HR+CaSO4→CaR2+NaSO4,故D正确;
故选D.
本题解析:
本题难度:简单