| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《盐类水解的原理》在线测试(2017年最新版)(四)
参考答案:A 本题解析:水解方程式为CO32- + H2O 本题难度:一般 2、填空题 (1)①在配制FeCl3溶液时,常在溶液中加入一些_________________以抑制其水解;其水解反应的离子方程式为 |
参考答案:(1)①盐酸离子方程式为 Fe3++3H2O Fe(OH)3+3H+
Fe(OH)3+3H+
②离子方程式Al3++3HCO3=3Al(OH)3+3CO2
③离子浓度大小关系_c(Cl-)>c(NH4+).>c(H+)>COH-);NH4+与水电离出的OH-结合生成弱电解质NH3.H2O,破坏了水的电离平衡,导致c(H+)>COH-)
(2)①>(3)E>D>F>C>B>A
(4) Al(OH)3 ; Al2O3 ;(填化学式)
在AlCl3溶液中存在平衡AlCl3 +3H2O Al (OH)3+3HCl加热时, HCl不断挥发,使平衡右移,从而生成了Al (OH)3.灼烧时2Al(OH)3=Al2O3+3H2O
Al (OH)3+3HCl加热时, HCl不断挥发,使平衡右移,从而生成了Al (OH)3.灼烧时2Al(OH)3=Al2O3+3H2O
本题解析:略
本题难度:困难
3、选择题 常温下,0.1 mol/L氨水溶液中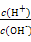 =1×10-8,下列叙述不正确的是( )
=1×10-8,下列叙述不正确的是( )
A.该溶液中氢离子的浓度:c(H+)=1×10-11 mol/L
B.0.1 mol/L氨水溶液与0.1 mol/L HCl溶液等体积混合后所得溶液中:c(N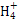 )+c(H+)=c(Cl-)+c(OH-)
)+c(H+)=c(Cl-)+c(OH-)
C.0.1 mol/L的氨水溶液与0.05 mol/L H2SO4溶液等体积混合后所得溶液中:c(N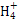 )+c(NH3)+c(NH3・H2O)=2c(S
)+c(NH3)+c(NH3・H2O)=2c(S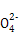 )
)
D.浓度均为0.1 mol/L的NH3・H2O和NH4Cl溶液等体积混合后,若溶液呈碱性,则c(N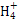 )>c(NH3・H2O)>c(Cl-)>c(OH-)>c(H+)
)>c(NH3・H2O)>c(Cl-)>c(OH-)>c(H+)
参考答案:D
本题解析:根据氨水中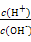 =1×10-8,结合水的离子积,可求得c(H+)=1×10-11mol/L,A项正确;氨水和盐酸恰好反应生成氯化铵,根据电荷守恒,可得c(N
=1×10-8,结合水的离子积,可求得c(H+)=1×10-11mol/L,A项正确;氨水和盐酸恰好反应生成氯化铵,根据电荷守恒,可得c(N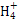 )+c(H+)=c(Cl-)+c(OH-),B项正确;氨水和硫酸恰好反应生成硫酸铵,根据物料守恒,可得c(N
)+c(H+)=c(Cl-)+c(OH-),B项正确;氨水和硫酸恰好反应生成硫酸铵,根据物料守恒,可得c(N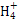 )+c(NH3)+c(NH3・H2O)=2c(S
)+c(NH3)+c(NH3・H2O)=2c(S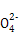 ),C项正确;由于混合后溶液显碱性,说明一水合氨的电离程度大于N
),C项正确;由于混合后溶液显碱性,说明一水合氨的电离程度大于N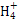 的水解程度,故c(Cl-)大于c(NH3・H2O),D项不正确。
的水解程度,故c(Cl-)大于c(NH3・H2O),D项不正确。
本题难度:一般
4、选择题 下列叙述不正确的是
A.在0.1 mol/LCH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)
B.在0.1 mol/L某二元弱酸强碱盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A)
C.CH3COOH和CH3COONa的混合溶液中,若c(CH3COO-)大于c(Na+),则溶液显酸性
D.10 mL0.02 mol/LHCl溶液与10 mL0.02 mol/LBa(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12
参考答案:B
本题解析:
本题难度:简单
5、选择题 Na2CO3水溶液中存在CO32-+H2O?HCO3-+OH-平衡。下列说法不正确的是( ? )
A.稀释溶液,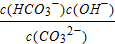 增大
增大
B.通入CO2,溶液pH减小
C.升高温度,此平衡常数增大
D.加入NaOH固体, 减小
减小
参考答案:A
本题解析:
本题难度:一般
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:高考化学知识点归纳《水的电离平.. | ||