微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 绿色化学实验是在绿色化学思想指导下的实验新方法,以减少污染,防止浪费等.下列实验不符合绿色化学的是( )
A.用铜与浓硝酸反应制取硝酸铜,并用水吸收尾气
B.在铜和浓硫酸反应的实验中,将铜片改为可调节高度的铜丝
C.用CCl4进行萃取操作练习时,用碘水代替溴水进行实验
D.测盐溶液的pH时,将pH试纸条剪成小块后使用
参考答案:A.铜与浓硝酸反应生成二氧化氮,二氧化氮能与水反应生成一氧化氮,一氧化氮有毒会污染空气,故A错误;
B.将铜片改为可调节高度的铜丝,可随时停止反应,能减少污染,故B正确;
C.溴水易挥发、溴蒸气有毒.练习萃取操作时用碘水代替溴水能减少对实验室的污染,故C正确;
D.将pH试纸条剪成小块后使用,可节约pH试纸,故D正确.
故选A.
本题解析:
本题难度:简单
2、选择题 下列各组物质中互为同系物的是(?)
A.丙烯酸和醋酸
B.甲酸和油酸
C.硬脂酸和软脂酸
D.软脂酸和油酸
参考答案:C
本题解析:油酸的分子式为C17H33COOH,其中烃基中有一个碳碳双键;丙烯酸的结构简式为
CH2==CH―COOH,与油酸互为同系物。硬脂酸为C17H35COOH,烃基为饱和的;软脂酸为C15H31COOH;甲酸为HCOOH,它们三者互为同系物。
本题难度:简单
3、简答题 HNO3是极其重要的化工原料.工业上制备HNO3采用NH3催化氧化法,将中间产生的NO2在密闭容器中多次循环用水吸收制备的.
(1)工业上用水吸收NO2生产硝酸,生成的尾气经过多次氧化、吸收的循环操作使其充分转化为硝酸(假定上述过程中无其它损失).
①试写出上述反应的化学方程式______.
②设循环操作的次数为n次,试写出NO2→HNO3转化率a与循环次数n之间关系的数学关系式.______.
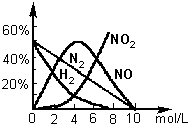
(2)用上述方法制备的HNO3为稀HNO3,将它用水稀释或蒸馏、浓缩可制得不同浓度的HNO3.实验证明:不同浓度的HNO3与同一金属反应可生成不同的还原产物.例如镁与硝酸反应实验中,测得其气相产物有H2、N2、NO、NO2,液液中有Mg(NO3)2、NH4NO3和H2O.生成这些产物的HNO3浓度范围为:H2:c<6.6mol/L;N2和NH4+:c<10.0mol/L;NO:0.10mol/L<c<10.0mol/L;NO2:c>2.0mol/L.各气体产物成分及含量随HNO3的浓度变化曲线如图所示.
①写出Mg与12mol/L的HNO3反应的化学方程式______.
②480mgMg与0.50L4.0mol/L的HNO3充分反应,收集到112mL气体(SPT).试通过计算写出反应化学方程式.______.
参考答案:(1)①NO2与水反应生成HNO3和NO,又NO能被O2氧化为NO2;所以上述反应的化学方程式为3NO2+H2O=2HNO3+NO,2NO+O2=2NO2;
故答案为:3NO2+H2O=2HNO3+NO,2NO+O2=2NO2;
②设起始时NO2物质的量为1 mol,经过nn次循环后生成HNO3的物质的量为:Sn=23+23×13+23×(13)2+23×(13)3+?+23×(13)nn-1,经等比数列求和可得:Sn=1-(13)nn,则NO2生成HNO3转化率为:1-(13)n1=a,即a=1-(13)nn;
故答案为:a=1-(13)nn;
(2)①根据图象可知当硝酸浓度大于10.0mol/L时,气体产物只有NO2,Mg+HNO3→Mg(NO3)2+NO2↑+H2O,反应中HNO3→NO2,N元素从+5价降到+4价得到1个电子,
Mg→Mg(NO3)2,Mg元素从0价升到+2价失去2个电子,所以Mg的计量数为1,NO2的计量数为2,再根据原子守恒配平:Mg+4HNO3=Mg(NO3)2+2NO2↑+2H2O;
故答案为:Mg+4HNO3=Mg(NO3)2+2NO2↑+2H2O;
②480mg Mg与0.50L 4.0mol/L的HNO3充分反应,Mg的物质的量比较少为0.02mol,HNO3的物质的量为2mol,反应中硝酸过量,
由图象可知:nn(NO):nn(N2):n(NO2):n(H2)=5:3:1:1,同时还原产物还有NH4+,
0.02molMg失去电子为0.04mol,反应生成气体为n=0.005mol,其中nn(NO)=0.005mol×510=0.0025mol,nn(N2)=0.0015mol,n(NO2)=0.0005mol,
n(H2)=0.0005mol,则气体得到电子数为0.0025mol×3+0.0015mol×5×2+0.0005mol×1+0.0005mol×2=0.024mol,
则生成NH4+时N元素得到的电子为0.04mol-0.024mol=0.016,所以生成NH4+的量为0.016×18=0.002mol,
所以n(NO):nn(N2):n(NO2):n(H2):n(NH4+):n(Mg)=5:3:1:1:4:40,
所以NO、N2、NO2、H2、NH4NO3、Mg的计量数分别为5、3、1、1、4、40,再由原子守恒得方程为:40Mg+100HNO3=5NO↑+3N2↑+H2↑+NO2↑+4NH4NO3+40Mg(NO3)2+41H2O;
故答案为:40Mg+100HNO3=5NO↑+3N2↑+H2↑+NO2↑+4NH4NO3+40Mg(NO3)2+41H2O.
本题解析:
本题难度:一般
4、填空题 (8分)某种混合物中可能含有甲酸、乙酸、甲醇及甲酸乙酯这些物质中的一种或几种。在检验时有以下现象:(1)有银镜反应;(2)加入新制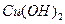 悬浊液,无变澄清的现象;
悬浊液,无变澄清的现象;
(3)与含碱的酚酞溶液共热,发现溶液中红色逐渐变浅以至无色。
根据上述现象,可以判断:
此混合物中一定含有?,
可能含有?,
一定没有?。(填结构简式)
参考答案:(各2分)HCOOC2H5; CH3OH;CH3COOH、HCOOH
本题解析:略
本题难度:一般
5、选择题 下列对实验现象的解释与结论正确的是( )
| 编号 | 实验操作 | 实验现象 | 解释与结论
A
向鸡蛋清溶液中,加入(NH4)2SO4溶液
有白色沉淀产生
蛋白质发生了变性
B
向某溶液中加入BaCl2溶液
有白色沉淀产生
生成难溶于水的BaSO4,该溶液中一定含有硫酸根离子
C
向苯中滴入少量浓溴水震荡,静置
溶液分层,上层呈橙红色,下层几乎无色
苯和溴水发生取代反应,使溴水褪色
D
向蔗糖中加入浓硫酸
变黑,放热,体积膨胀,放出刺激性味的气体
浓硫酸具有脱水性和强氧化性,反应中生成C、SO2和CO2等
|
A.A
B.B
C.C
D.D
参考答案:A、向鸡蛋清溶液中,加入(NH4)2SO4溶液,有白色沉淀产生,蛋白质发生了盐析不是变性,故A错误.
B、和氯化钡反应生成不溶于水的沉淀有氯化银、硫酸钡,所以该溶液中不一定含有硫酸根离子,故B错误.
C、苯和溴水不反应,只是苯萃取了溴水中的溴而使溴水褪色,故C错误.
D、浓硫酸具有强氧化性、吸水性和脱水性,向蔗糖中加入浓硫酸,蔗糖变黑,放热,体积膨胀,放出刺激性味的气体,是利用了浓硫酸的脱水性和强氧化性,且该反应中有C、SO2和CO2等生成,故D正确.
故选D.
本题解析:
本题难度:简单