微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 下图为某套实验装置示意图,无法看到实验说明,加热装置已经省略.
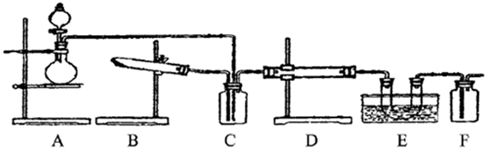
I.甲同学认为当D处盛放V2O5作催化剂时,此套装置可用于合成物质X,并预测E处冰水冷却的U型管中将有固体X出现.
(1)事实上此装置所附实验说明符合甲同学的推断,那么A中所发生的反应的化学方程式是______,C装置中盛放的液体药品的名称是______.
(2)甲同学方案中为了提高A装置产物的转化率,可以增大B装置产物的通入量,欲知A、B两装置中产物在D中的通入量,可通过观察______得知.
(3)本实验在设计上有无缺失之处?若有请答出改进方案______;(若无,此问可不答)
II.乙同学认为若D处盛放铂铑合金网作催化剂,则此套装置也可用于合成物质Y,并预测E处冰水冷却的U型管中将有红棕色气体生成,且越接近U型管底部颜色越浅.
(4)写出乙同学认为的D装置中发生反应的化学方程式______.
(5)对于A处,乙认为没有加热装置,请代乙阐述A中气体的产生原理______(6)若要用上述装置完成乙同学所认为的实验,且C处所起作用与合成X时所起作用基?本一致,那么C处的广口瓶应改为______,所装药品为______.
参考答案:(1)V2O5作催化剂时,是二氧化硫转化为三氧化硫时的反应条件,所以A是制取二氧化硫的装置,所发生的反应的化学方程式是:Na2SO3+H2SO4(浓)=Na2SO4+H2O+SO2↑;干燥二氧化硫用浓硫酸,
故答案为::Na2SO3+H2SO4(浓)=Na2SO4+H2O+SO2↑;浓硫酸;
(2)C装置的作用:干燥二氧化硫;调节二氧化硫和氧气的混合比例;可控制二氧化硫和氧气的产生速率,欲知二氧化硫和氧气在D中的通入量,可通过观察C中两导管口气泡的产生速率来判断,故答案为:C中两导管口气泡的产生速率;
(3)F装置进行尾气处理时,易导致倒吸现象的产生,所以应在EF之间连接一个防倒吸装置,故答案为:有,应在EF之间连接一个防倒吸装置;
(4)铂铑合金网作催化剂,是氨气的催化氧化时的反应条件,所以D装置是氨气的催化氧化反应,其发生反应的化学方程式为:4NH3+5O2?催化剂?.?4NO+6H2O,故答案为:4NH3+5O2?催化剂?.?4NO+6H2O(若多写2NO+O2=2NO2也可以);
(5)可以用浓氨水和固体NaOH(或生石灰或碱石灰)混合不加热的方法来制氨气,其原理是:化学平衡NH3+H2O?NH3?H2O?NH4++OH-的移动原理,故答案为:将分液漏斗中的浓氨水滴加至圆底烧瓶中的固体NaOH(或生石灰或碱石灰)中,反应放热溶液中c(OH-)增大氨水浓度增大,上述三个因素均导致氨水中的平衡:NH3+H2O?NH3?H2O?NH4++OH-向左移动致使NH3逸出;
(6)氨气是碱性气体,需用碱石灰干燥氨气,固体干燥剂放在干燥管中,故答案为:U形管或干燥管,碱石灰(其他合理答案亦可).
本题解析:
本题难度:一般
2、简答题 HNO3是极其重要的化工原料.工业上制备HNO3采用NH3催化氧化法,将中间产生的NO2在密闭容器中多次循环用水吸收制备的.
(1)工业上用水吸收NO2生产硝酸,生成的尾气经过多次氧化、吸收的循环操作使其充分转化为硝酸(假定上述过程中无其它损失).
①试写出上述反应的化学方程式______.
②设循环操作的次数为n次,试写出NO2→HNO3转化率a与循环次数n之间关系的数学关系式.______.
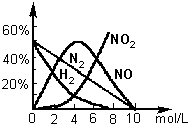
(2)用上述方法制备的HNO3为稀HNO3,将它用水稀释或蒸馏、浓缩可制得不同浓度的HNO3.实验证明:不同浓度的HNO3与同一金属反应可生成不同的还原产物.例如镁与硝酸反应实验中,测得其气相产物有H2、N2、NO、NO2,液液中有Mg(NO3)2、NH4NO3和H2O.生成这些产物的HNO3浓度范围为:H2:c<6.6mol/L;N2和NH4+:c<10.0mol/L;NO:0.10mol/L<c<10.0mol/L;NO2:c>2.0mol/L.各气体产物成分及含量随HNO3的浓度变化曲线如图所示.
①写出Mg与12mol/L的HNO3反应的化学方程式______.
②480mgMg与0.50L4.0mol/L的HNO3充分反应,收集到112mL气体(SPT).试通过计算写出反应化学方程式.______.
参考答案:(1)①NO2与水反应生成HNO3和NO,又NO能被O2氧化为NO2;所以上述反应的化学方程式为3NO2+H2O=2HNO3+NO,2NO+O2=2NO2;
故答案为:3NO2+H2O=2HNO3+NO,2NO+O2=2NO2;
②设起始时NO2物质的量为1 mol,经过nn次循环后生成HNO3的物质的量为:Sn=23+23×13+23×(13)2+23×(13)3+?+23×(13)nn-1,经等比数列求和可得:Sn=1-(13)nn,则NO2生成HNO3转化率为:1-(13)n1=a,即a=1-(13)nn;
故答案为:a=1-(13)nn;
(2)①根据图象可知当硝酸浓度大于10.0mol/L时,气体产物只有NO2,Mg+HNO3→Mg(NO3)2+NO2↑+H2O,反应中HNO3→NO2,N元素从+5价降到+4价得到1个电子,
Mg→Mg(NO3)2,Mg元素从0价升到+2价失去2个电子,所以Mg的计量数为1,NO2的计量数为2,再根据原子守恒配平:Mg+4HNO3=Mg(NO3)2+2NO2↑+2H2O;
故答案为:Mg+4HNO3=Mg(NO3)2+2NO2↑+2H2O;
②480mg Mg与0.50L 4.0mol/L的HNO3充分反应,Mg的物质的量比较少为0.02mol,HNO3的物质的量为2mol,反应中硝酸过量,
由图象可知:nn(NO):nn(N2):n(NO2):n(H2)=5:3:1:1,同时还原产物还有NH4+,
0.02molMg失去电子为0.04mol,反应生成气体为n=0.005mol,其中nn(NO)=0.005mol×510=0.0025mol,nn(N2)=0.0015mol,n(NO2)=0.0005mol,
n(H2)=0.0005mol,则气体得到电子数为0.0025mol×3+0.0015mol×5×2+0.0005mol×1+0.0005mol×2=0.024mol,
则生成NH4+时N元素得到的电子为0.04mol-0.024mol=0.016,所以生成NH4+的量为0.016×18=0.002mol,
所以n(NO):nn(N2):n(NO2):n(H2):n(NH4+):n(Mg)=5:3:1:1:4:40,
所以NO、N2、NO2、H2、NH4NO3、Mg的计量数分别为5、3、1、1、4、40,再由原子守恒得方程为:40Mg+100HNO3=5NO↑+3N2↑+H2↑+NO2↑+4NH4NO3+40Mg(NO3)2+41H2O;
故答案为:40Mg+100HNO3=5NO↑+3N2↑+H2↑+NO2↑+4NH4NO3+40Mg(NO3)2+41H2O.
本题解析:
本题难度:一般
3、选择题 下列对于H2SO4的分类,不正确的是
[? ]
A.酸
B.强酸
C.含氧酸
D.无氧酸
参考答案:D
本题解析:
本题难度:简单
4、选择题 如图是将SO2转化为重要的化工原料H2SO4的原理示意图,下列说法不正确的是( ? )
A.该装置将化学能转化为电能
B.催化剂b表面O2发生还原反应,其附近酸性增强
C.催化剂a表面的反应是:SO2+2H2O-2e-=SO42-+4H+
D.若得到的硫酸浓度仍为49%,则理论上参加反应的SO2与加入的H2O的质量比为8:15
